MIBC – neue Ära in der Erstlinientherapie: Durvalumab + Chemotherapie
Autorin:
Priv.-Doz. Dr. Mag. Melanie Hassler-Di Fratta, phD
Universitätsklinik für Urologie
Medizinische Universität Wien
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die NIAGARA-Studie markiert einen Wendepunkt in der systemischen Therapie des muskelinvasiven Urothelkarzinoms. Die Ergänzung von Durvalumab zur Standard-Chemotherapie verbessert signifikant das pathologische Ansprechen und eröffnet neue Perspektiven in der perioperativen Behandlung.
Keypoints
-
Die NIAGARA-Studie zeigt erstmals, dass der Zusatz von Durvalumab zur neoadjuvanten Chemotherapie bei MIBC die pathologische Komplettremission und das ereignisfreie Überleben signifikant verbessert bzw. verlängert.
-
Die neue Erstlinientherapie besteht nun aus Cisplatin + Gemcitabin + Durvalumab vor radikaler Zystektomie – gefolgt von einer Erhaltungstherapie mit Durvalumab.
-
Die positiven Effekte der Therapie sind unabhängig vom PD-L1-Status – damit ist der Ansatz breit anwendbar.
-
Mit NIAGARA beginnt eine neue Ära der immunonkologischen Therapie im kurativen Setting des muskelinvasiven Blasenkarzinoms.
Das muskelinvasive Urothelkarzinom der Harnblase (MIBC) stellt eine onkologische Herausforderung dar. Trotz radikaler Zystektomie und etablierter neoadjuvanter Chemotherapie bleibt das Risiko eines Rezidivs oder einer Metastasierung erheblich. Die Suche nach wirksameren multimodalen Ansätzen führte zur Entwicklung immunonkologischer Therapien, die das bestehende Behandlungsschema erweitern.
Mit der kürzlich publizierten NIAGARA-Studie wurde erstmals belegt, dass die Kombination von Durvalumab mit Cisplatin und Gemcitabin in der neoadjuvanten Situation vor Zystektomie einen klinisch bedeutsamen Vorteil bringt – und damit den Weg für eine neue Erstlinientherapie ebnet. Bislang galt die platinbasierte neoadjuvante Chemotherapie (meist MVAC oder Cisplatin + Gemcitabin) als Standard bei Cisplatin-fitten Patient:innen mit MIBC. Der Überlebensvorteil durch die neoadjuvante Therapie ist in mehreren randomisierten Studien und Metaanalysen belegt, bleibt jedoch begrenzt (absolute Verbesserung der Gesamtüberlebensrate um ca. 5–8%). Die Einführung immunonkologischer Therapien (Checkpoint-Inhibitoren) hat in der metastasierten Situation bereits signifikante Fortschritte erzielt – ihr Potenzial in der kurativen, neoadjuvanten Therapie war bislang jedoch unklar.
NIAGARA-Studie
Die NIAGARA-Studie ist eine randomisierte, multizentrische Phase-III-Studie, die den Zusatz von Durvalumab, einem PD-L1-Inhibitor, zur Standardchemotherapie in der perioperativen Situation untersucht hat. Eingeschlossen wurden über 1000 Patient:innen mit muskelinvasivem Blasenkarzinom (cT2–T4a, N0/1, M0), die für Cisplatin geeignet waren.
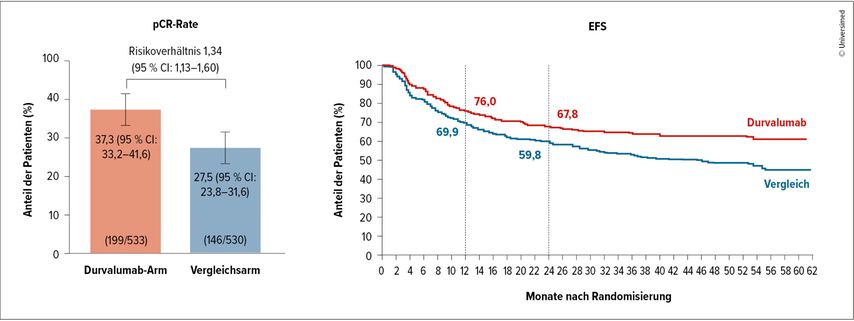
Die Patient:innen wurden in einen Kontrollarm und in einen Interventionsarm randomisiert. Im Kontrollarm erhielten die Patient:innen 4 Zyklen Cisplatin + Gemcitabin vor radikaler Zystektomie; im Interventionsarm wurden die Patient:innen mit 4 Zyklen Cisplatin + Gemcitabin sowie Durvalumab (1500mg q3w) vor der Operation und anschließender Erhaltungstherapie mit Durvalumab für 8 Zyklen behandelt. Die primären Endpunkte waren die Rate der pathologischen Komplettremission (pCR) sowie das ereignisfreie Überleben (EFS) (Abb.1). Es zeigten sich eine pCR-Rate im Interventionsarm von 37,3% vs. 27,5% im Kontrollarm (OR 1,60; 95% CI: 1,23–2,08; p=0,0005), eine EFS-Rate nach 2 Jahren von 67,8% mit Durvalumab vs. 59,8% im Kontrollarm (HR 0,68; 95% CI: 0,56–0,82; p<0;0001) sowie eine Gesamtüberlebensrate nach 2 Jahren von 82,2% vs. 75,2% (HR 0,75; 95% CI: 0,59–0,93; p=0,0106).
Abb. 1: Die Rate des pathologischen Ansprechens (links) sowie das ereignisfreie Überleben (rechts) zeigten sich im Studienarm mit Durva + Gem/Cis im Vergleich zu Gem/Cis signifikant verbessert bzw. verlängert (modifiziert nach Powles T et al. 2024)1
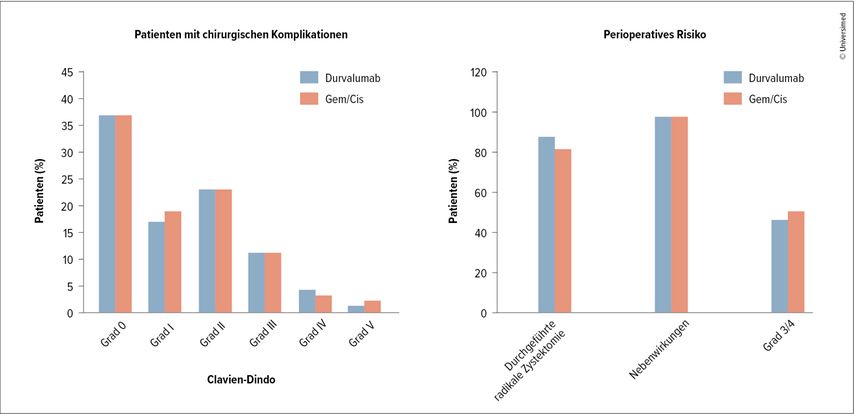
Damit stellt NIAGARA die erste Studie dar, welche einen Überlebensvorteil für MIBC-Patient:innen sowohl im neoadjuvanten wie auch im adjuvanten Setting zeigt. Bezüglich des Sicherheitsprofils und des perioperativen Risikos traten im Vergleich zur Monotherapie keine neuen signifikanten Nebenwirkungen auf, auch das Risiko perioperativer Komplikationen war nicht erhöht, und die Rate tatsächlich durchgeführter Zystektomien nach der systemischen Therapie war mit 88% im Durvalumab-Arm und 83% im Kontrollarm vergleichbar (Abb. 2).
Abb. 2: Die Rate an chirurgischen Komplikationen (links) und das perioperative Risiko (rechts) waren zwischen den Studienarmen Durva + Gem/Cis vs. Gem/Cis vergleichbar (modifiziert nach Powles T et al. 2024)1
Klinische Bedeutung und Konsequenzen für den Alltag
Die Ergebnisse der NIAGARA-Studie verändern den therapeutischen Standard in der Erstlinienbehandlung des MIBC fundamental. Durch den Zusatz von Durvalumab kann nicht nur die Rate der pathologischen Komplettremission gesteigert, sondern auch das rezidivfreie Überleben verlängert werden – ein bedeutender Schritt in Richtung personalisierter, effektiverer Therapie.
Im Rahmen der Therapieentscheidung sollte mit den Patient:innen eine perioperative Gabe von Durvalumab gegenüber einer adjuvanten Gabe von Nivolumab abgewogen werden. Die perioperative Kombination von Durvalumab mit Chemotherapie bietet potenziell einem breiteren Patient:innenkollektiv einen Zugang zur Immuntherapie, da die Studie CheckMate 274, auf der die adjuvante Gabe von Nivolumab basiert, ausschließlich Patient:innen mit Hochrisikomerkmalen nach radikaler Zystektomie einschloss. Zudem ist Nivolumab in Europa im adjuvanten Setting nur für PD-L1-positive Tumoren zugelassen. Auf der anderen Seite könnte die perioperative Strategie mit Durvalumab dazu führen, dass Patient:innen mit pathologischer Komplettremission (pCR) im adjuvanten Teil der Therapie überbehandelt werden, auch wenn rezente Daten zeigen, dass Patient:innen mit pCR und perioperativer Durvalumab-Gabe ein längeres EFS aufweisen als Patient:innen mit pCR, aber ohne Durvalumab-Gabe.
Für die klinische Praxis bedeutet dies:
-
Bei geeigneten Patient:innen (Cisplatin-fit, M0, cT2–T4a, cN0-cN1) sollte die Kombination aus Durvalumab + Chemotherapie als neue Standardtherapie diskutiert und angeboten werden.
-
Die zusätzliche Gabe von Durvalumab führt zu keiner Erhöhung des perioperativen Risikos im Vergleich zur Monotherapie mit Cisplatin/Gemcitabin.
-
Die perioperative Therapie mit Durvalumab könnte sich als neue Langzeitstrategie zur Reduktion von Rezidiven etablieren.
Offene Fragen und Ausblick
Trotz der überzeugenden Ergebnisse wirft die neue Therapieoption auch Fragen auf. Unklar ist der Stellenwert von Durvalumab bei Patient:innen mit eingeschränkter Nierenfunktion, welche nicht Cisplatin-fit sind.
Ebenfalls kann nicht erklärt werden, in welchem Ausmaß die beobachteten Vorteile dem neoadjuvanten und welche dem adjuvanten Einsatz von Durvalumab zuzuschreiben sind – ein methodisches Defizit, das zukünftige Studien mit komplexeren Mehrarm-Designs adressieren müssten. Die adjuvante Gabe von Durvalumab nach radikaler Zystektomie führt möglicherweise zu einer Überbehandlung von Patient:innen mit pCR, auch wenn aktuelle Daten darauf hinweisen, dass Patient:innen mit pCR unter perioperativer Durvalumab-Gabe ein verlängertes EFS im Vergleich zu Patient:innen mit pCR ohne Durvalumab erzielen.
Ein interessanter Marker für das Ansprechen auf eine systemische Therapie ist die ctDNA. Patient:innen, bei welchen die ctDNA unter Therapie nachweisbar bleibt, hatten in der Regel auch keine pCR – ctDNA-Monitoring ist jedoch noch nicht etablierter Standard in der Klinik. Interessanterweise zeigte die VESPER-Studie, dass die neoadjuvante Therapie mit „dose-dense“ MVAC eine höhere pCR-Rate als Gemcitabin-Cisplatin erzielt – ddMVAC könnte daher in Kombination mit Durvalumab zu einem noch stärkeren Effekt führen, dürfte jedoch auch mit einer erhöhten Nebenwirkungsrate einhergehen. Schließlich könnte die Kombination auch in der organerhaltenden Therapie (z.B. Trimodalität) Anwendung finden, dies muss jedoch noch in zukünftigen Studien (z.B. mit blasenerhaltenden Ansätzen) gezeigt werden.
Literatur:
1 Powles T et al.: Perioperative durvalumab with neoadjuvant chemotherapy in operable bladder cancer. N Engl J Med 2024; 391(19): 1773-86 2 Bajorin DF et al.: Adjuvant nivolumab versus placebo in muscle-invasive urothelial carcinoma. N Engl J Med 2021; 384(22): 2102-14 3 Eule C et al.: Neoadjuvant cisplatin-based chemotherapy in nonmetastatic muscle-invasive bladder cancer: A systematic review and pooled meta-analysis to determine the preferred regimen. Urology 2024; 188: 118-24 4 Pfister C et al.: Perioperative dose-dense methotrexate, vinblastine, doxorubicin, and cisplatin in muscle-invasive bladder cancer (VESPER): Survival endpoints at 5 years in an open-label, randomised, phase 3 study. Lancet Oncol 2024; 25(2): 255-64 5 Powles T et al.: Circulating tumor DNA (ctDNA) in patients with muscle-invasive bladder cancer (MIBC) who received perioperative durvalumab (D) in NIAGARA. J Clin Oncol 2025; 43(16): 4503 6 Galsky MD et al.: Additional efficacy and safety outcomes and an exploratory analysis of the impact of pathological complete response (pCR) on long-term outcomes from NIAGARA. J Clin Oncol 2025; 43(5): 659
Das könnte Sie auch interessieren:
Historische Momente aus Wiener urologischen Abteilungen
Der 51. Österreichische Urologenkongress in der Messe Wien vom 22. bis 25.5.2025, veranstaltet zusammen mit der bayrischen Schwestergesellschaft, fokussierte nicht nur wichtige ...
Zytoreduktive Nephrektomie im Jahr 2025 – ein evidenzfreier Raum?
Die zytoreduktive Nephrektomie (CN) ist heutzutage weiterhin ein fester Bestandteil der Therapie des metastasierten Nierenzellkarzinoms (mRCC). Doch ob und wann ein Patient einer CN ...
Blasenerhalt trotz BCG-Versagen bei High-Risk-Tumoren: intravesikale Strategien heute und morgen
Standard bei BCG-Versagen beim nichtmuskelinvasiven Blasenkarzinom ist die radikale Zystektomie. Alternativen mit Gemcitabin oder Mitomycin sind onkologisch unterlegen. Neue Ansätze wie ...
%20und%20das%20perioperative%20Risiko%20(rechts).jpg)