La radiothérapie adjuvante à l’ère des thérapies systémiques modernes
Auteure:
Prof. Dre méd. Mechthild Krause
Direktorin
Klinik für Strahlentherapie und Radioonkologie, Universitätsklinikum Dresden
E-mail: mechthild.krause@ukdd.de
La radiothérapie adjuvante demeure un élément central dans le traitement des tumeurs malignes cutanées, malgré les progrès réalisés avec les immunothérapies et les thérapies ciblées. Elle améliore le contrôle locorégional et offre des bénéfices fonctionnels et esthétiques, en particulier au niveau du visage et du cou, où elle est également utilisée comme option thérapeutique curative primaire. Les thérapies systémiques modernes complètent la radiothérapie par des effets systémiques. La réussite thérapeutique dépend de manière déterminante du choix du bon moment pour la combinaison de ces deux approches.
Keypoints
-
La radiothérapie adjuvante réduit le risque de récidive locorégionale chez les patient·es présentant des facteurs de risque; un bénéfice en termes de survie n’a jusqu’à présent été démontré que rétrospectivement pour les carcinomes épidermoïdes avec facteurs de risque.
-
Les immunothérapies et les «targeted therapies» induisent principalement des effets systémiques, mais également des effets locorégionaux.
-
Une intégration précoce des immunothérapies après la radiothérapie semble déterminante.
-
À l’avenir, des biomarqueurs seront nécessaires afin de sélectionner les patient·es pour une radiothérapie adjuvante seule, une radiothérapie associée à une thérapie systémique ou une thérapie systémique seule.
Données probantes sur la radiothérapie adjuvante
Mélanome malin
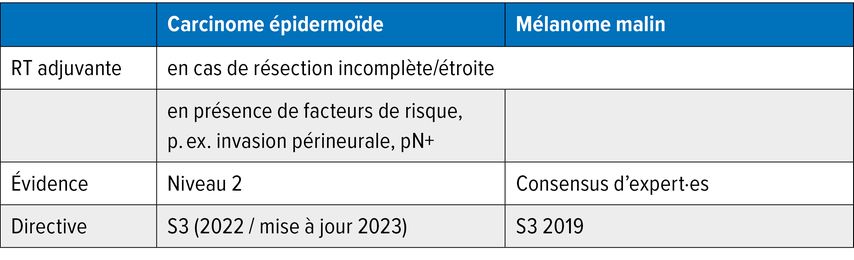
L’étude de phaseIII de Henderson et al.1 a randomisé des patient·es après lymphadénectomie entre une radiothérapie adjuvante et l’absence de radiothérapie adjuvante (observation). Une diminution significative des récidives nodales a été observée dans le groupe traité par radiothérapie, sans bénéfice démontré en termes de survie globale. En définitive, une indication à la radiothérapie adjuvante n’existe ici qu’en cas de résection incomplète ou étroite, sans possibilité de réexcision (Tab.1).
Tab.1: Indications conformes aux recommandations pour la radiothérapie adjuvante des carcinomes épidermoïdes cutanés et des mélanomes malins
Carcinome épidermoïde
Il n’existe pas d’études randomisées contrôlées évaluant la radiothérapie adjuvante dans le carcinome épidermoïde. Des analyses rétrospectives suggèrent des bénéfices dans des sous-groupes à haut risque, notamment en cas d’invasion périneurale ou d’atteinte ganglionnaire, comme le montre par exemple une étude de Harris et al.2 Des méta-analyses mettent même en évidence un avantage en termes de survie pour ces groupes de patient·es.3,4 Globalement, les données disponibles reposent jusqu’à présent sur des preuves de niveauII et soutiennent, outre la radiothérapie après une résection incomplète ou étroite, l’utilisation de la radiothérapie adjuvante chez les patient·es présentant des facteurs de risque tels que mentionnés ci-dessus (Tab.1).
Thérapies systémiques modernes en combinaison avec la radiothérapie
Mélanome malin
Une étude clé est celle de Long et al. portant sur le traitement adjuvant par dabrafénib/tramétinib, qui a montré, chez des patient·es atteint·es de mélanome de stadeIII porteur d’une mutation BRAF, une prolongation de la survie sans récidive ainsi qu’une tendance statistique en faveur d’une amélioration de la survie globale.5 La radiothérapie était autorisée en complément, mais ne faisait pas partie intégrante du protocole de l’étude. Il reste toutefois incertain de savoir si, et pour quel·les patient·es, une radiothérapie supplémentaire est nécessaire en plus de cette thérapie ciblée moderne. Dans les études randomisées portant sur l’immunothérapie adjuvante, des patient·es ayant bénéficié d’une résection R0 ont généralement été inclus·es, de sorte qu’aucune radiothérapie complémentaire n’a été administrée.
Carcinome épidermoïde
L’étude de phaseIII C-POST a montré que le cemiplimab, un anticorps anti-PD-1, prolongeait significativement la survie sans maladie après une chirurgie et une radiothérapie adjuvante (HR: 0,32; p<0,001).6 Le contrôle locorégional ainsi que l’absence de métastases à distance étaient également améliorés. Étant donné que tous·tes les patient·es ont reçu une radiothérapie avant l’immunothérapie en raison de leur profil de risque clinique, l’effet spécifique de la radiothérapie ne peut pas être évalué séparément.
Il est important de noter que l’étude KEYNOTE-630 évaluant un traitement adjuvant par pembrolizumab a donné des résultats négatifs. Cette étude se distinguait par une randomisation plus tardive (intervalle plus long entre l’immunothérapie et la radiothérapie) et par une sélection plus stricte des patient·es, incluant explicitement des patient·es présentant un risque de récidive locale, tandis que dans C-POST, de nombreux·ses patient·es présentaient un risque de récidive régionale.
Implications pratiques
La radiothérapie demeure un traitement adjuvant pertinent dans les mélanomes malins et les carcinomes épidermoïdes cutanés. Elle constitue un outil ciblé pour le contrôle locorégional. Lors de l’ajout de thérapies systémiques modernes, le moment de leur administration semble déterminant; les données suggèrent que l’immunothérapie devrait débuter le plus précocement possible après la radiothérapie afin de tirer parti des synergies potentielles.
Perspectives
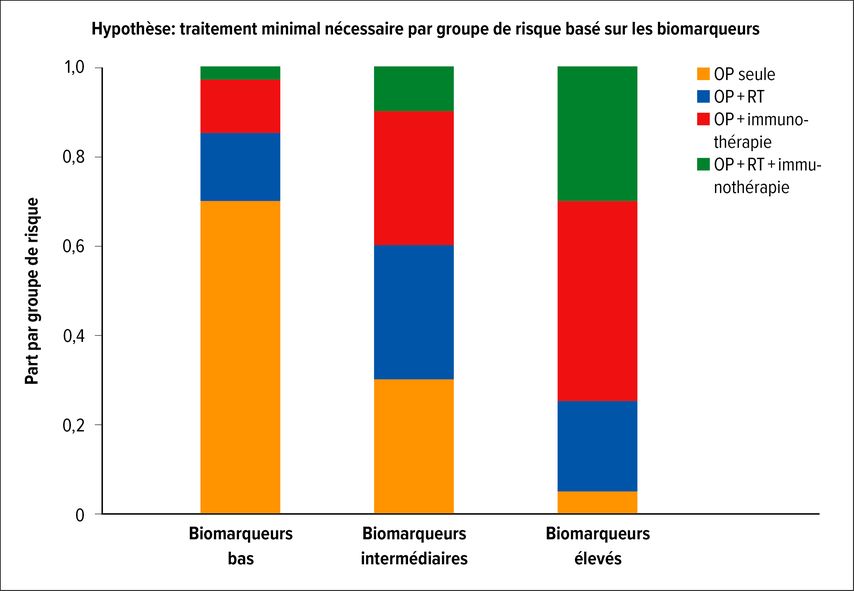
L’avenir du traitement adjuvant repose dans des stratégies multimodales. Le rôle de la radiothérapie adjuvante en association avec les thérapies systémiques modernes pourrait être mieux défini par des études randomisées, nécessitant la participation d’un grand nombre de centres. Le développement de stratégies thérapeutiques personnalisées robustes est essentiel afin d’éviter un surtraitement de certains groupes de patient·es dans le cadre d’approches multimodales, tout en garantissant un traitement optimal aux patient·es présentant un risque particulièrement élevé de progression tumorale (Fig.1 à titre d’exemple hypothétique). Parallèlement, des analyses ciblées de la rentabilité devront également être menées.
Fig.1: Illustration hypothétique d’un «traitement minimal nécessaire» après analyse des biomarqueurs. En cas de faible expression des biomarqueurs, de nombreux·ses patient·es bénéficient déjà de la chirurgie (OP); les traitements adjuvants apportent chacun un effet supplémentaire pour un groupe pertinent, effet qui ne peut plus être accru par une triple combinaison. Lorsque l’expression des biomarqueurs est plus élevée, l’effet de la thérapie multimodale augmente. Illustration réalisée avec le soutien de ChatGPT.
Dans l’ensemble, la radiothérapie reste un pilier important pour un sous-groupe de patient·es, en tant que partenaire des thérapies systémiques modernes.
Littérature:
1 Henderson MA et al.: Adjuvant lymph-node field radiotherapy versus observation only in patients with melanoma at high risk of further lymph-node field relapse after lymphadenectomy (ANZMTG 01.02/TROG 02.01): 6-year follow-up of a phase 3, randomised controlled trial. Lancet Oncol 2015; 16(9): 1049-60 2 Harris BN et al.: Association of adjuvant radiation therapy with survival in patients with advanced cutaneous squamous cell carcinoma of the head and neck. JAMA Otolaryngol Head Neck Surg 2019; 145(2): 153-8 3 Zhang J et al.: Efficacy and prognostic factors of adjuvant radiotherapy for cutaneous squamous cell carcinoma: a systematic review and meta-analysis. JEur Acad Dermatol Venereol 2021; 35(9): 1777- 87 4 Sahovaler A et al.: Outcomes of cutaneous squamous cell carcinoma in the head and neck region with regional lymph node metastasis: a systematic review and meta-analysis. JAMA Otolaryngol Head Neck Surg 2019; 145(4): 352-60 5 Long GV et al.: Final results for adjuvant dabrafenib plus trametinib in stage III melanoma. N Engl J Med 2024; 391(18): 1709-20 6 Rischin D et al.: Adjuvant cemiplimab or placebo in high-risk cutaneous squamous-cell carcinoma. N Engl J Med 2025; 393(8): 774-85
Das könnte Sie auch interessieren:
Gérer les effets indésirables de manière ciblée: pratique selon les directives S3 et internationales
Les thérapies systémiques contre le cancer prolongent la survie et permettent de contrôler les maladies tumorales. Il est déterminant que les patient·es tolèrent bien le traitement. Cela ...
Nouveaux résultats d’études à San Antonio
La prise en charge individualisée du carcinome mammaire est déjà très avancée dans la pratique clinique quotidienne. Néanmoins, des récidives tumorales surviennent et des patient·es ...
Mise à jour: comment éviter les transfusions?
Chez les patient·es à faible risqueatteint·es de syndromes myélodysplasiques (SMD), l’anémie nécessitant des transfusions constitue souvent le principal problème altérant la qualité de ...