Gérer les effets indésirables de manière ciblée: pratique selon les directives S3 et internationales
Auteur·es:
OA Dr méd. Hassan Naim
Prof. Dr méd. David Blum
PD Dre méd. Caroline Hertler
Universitätsspital Zürich
Klinik für Radio-Onkologie
Kompetenzzentrum für Palliative Care
Interdisziplinäres Zentrum für Hochpräzisionstherapie, Zürich
Correspondance:
E-mail: hassan.naim@usz.ch
Les thérapies systémiques contre le cancer prolongent la survie et permettent de contrôler les maladies tumorales. Il est déterminant que les patient·es tolèrent bien le traitement. Cela est possible grâce à des stratégies de soutien claires et anticipées: identifier précocement les risques, agir de manière prophylactique, traiter les effets indésirables selon leur gravité et assurer un suivi étroit – dans l’esprit de la directive S3 et des recommandations internationales complémentaires.1
Keypoints
-
Standardiser l’antiémèse, la prophylaxie des infections et l’information avant le début du traitement.
-
Gérer les toxicités liées à l’immunothérapie (irAE, «immune-related adverse events») selon l’organe concerné et le grade; définir des filières d’urgence claires.
-
Sous TKI (inhibiteur de tyrosine kinase), prendre activement en charge en particulier l’hypertension, l’HFSR (réaction main-pied-peau) ainsi que la diarrhée et le QTc (intervalle QT corrigé).
-
Documenter l’adhésion thérapeutique, les voies d’urgence, les adaptations posologiques et la réexposition.
Pourquoi agir maintenant?
Les effets indésirables constituent une cause fréquente de réduction de dose, d’interruption du traitement ou d’hospitalisations évitables. La directive S3 «Supportive Therapy» (032-054OL, Version 2.0; 2.4.2025) propose un cadre d’information allant de l’émèse à la myélosuppression et à la mucite, jusqu’aux thérapies ciblées. La mise en œuvre rigoureuse des recommandations stabilise la qualité de vie et l’adhésion thérapeutique; des SOP (procédures opératoires standard), des suivis précoces (p.ex. contact téléphonique <72 heures) et des plans d’urgence clairement définis y contribuent.1
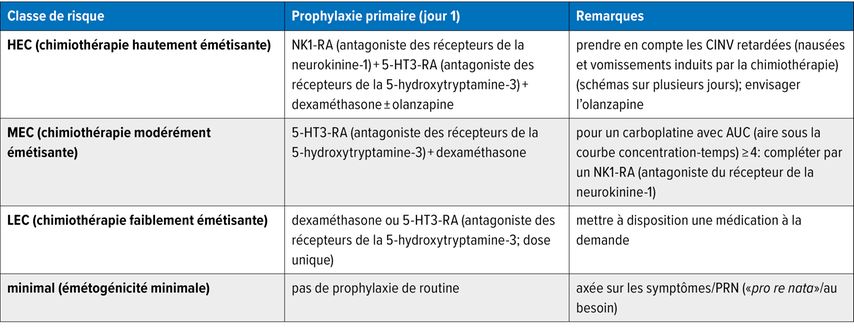
Tab.1: Antiémèse standard d’après la classe de risque émétogène (extrait; modifié selon les directives S3 et Jordan K et al.)1,2
Chimiothérapie: un classique de la prévention et de la prise en charge
Antiémèse: adapter selon la classe de risque émétogène
La prophylaxie primaire de l’émèse et des nausées dépend de facteurs spécifiques aux patient·es ainsi que de la classe de risque émétogène du schéma thérapeutique. On distingue quatre classes:
-
chimiothérapie hautement émétisante (HEC)
-
chimiothérapie modérément émétisante (MEC)
-
chimiothérapie faiblement émétisante (LEC)
-
émétogénicité minimale
En cas de HEC, le traitement antiémétique standard comprend:
-
antagoniste des récepteurs de la neurokinine-1
-
(NK1-RA)
-
+antagoniste des récepteurs 5-hydroxytryptamine-3 (5-HT3-RA)
-
+ dexaméthasone
-
±olanzapine
Pour une aire sous la courbe concentration-temps (AUC) du carboplatine ≥4, l’ajout d’un antagoniste des récepteurs de la neurokinine-1 (NK1-RA) est recommandé.
La mise à jour 2023/24 de la Multinational Association of Supportive Care in Cancer (MASCC)/European Society for Medical Oncology (ESMO) précise la classification – notamment pour les médicaments oncologiques oraux – et complète les recommandations S3. Concrètement, cela implique:1,2
-
une antiémèse intégrée de manière fixe au plan thérapeutique
-
augmenter ou modifier l’antiémèse en cas de nausées et vomissements induits par chimiothérapie de percée (CINV)
-
vérifier l’adhésion thérapeutique
Neutropénie fébrile – une urgence reste une urgence
Prophylaxie primaire par G-CSF
En cas de risque de neutropénie fébrile (NF) ≥20% (ou 10–20% en présence de facteurs de risque), une prophylaxie primaire par G-CSF (facteur de stimulation des colonies de granulocytes) est indiquée. En cas de fièvre, un bilan septique immédiat est requis; des hémocultures doivent être réalisées et un traitement antibiotique anti-pseudomonas par voie intraveineuse instauré sans délai. Une désescalade peut être envisagée après stabilisation. Les stratégies orales sont réservées à des patient·es sélectionné·es à faible risque.1
Facteurs de risque de neutropénie fébrile
-
âge ≥65 ans, mauvais état général (EG)/statut ECOG ≥2
-
neutropénie ou infiltration médullaire préexistante, ou antécédent de NF
-
dysfonction rénale ou hépatique, dénutrition/faible taux d’albumine
-
forte myélotoxicité ou schémas de chimiothérapie intensifs/denses
-
infection active, plaies ouvertes/interventions chirurgicales récentes, comorbidités multiples
-
maladie avancée, antécédents de chimiothérapie ou de radiothérapie
-
immunosuppression (p.ex. VIH, corticothérapie systémique)
En présence d’un risque de NF de 10 à 20%, une prophylaxie doit être envisagée si ≥1 facteur est présent.
Mucite, diarrhée, fatigue et NPIC – adopter une approche structurée
Mucite:
-
soins buccaux rigoureux
-
analgésie
-
soutien nutritionnel
-
envisager le palifermine dans certaines situations
Diarrhée associée à la chimiothérapie (surtout 5-FU [5-fluorouracile]/capécitabine/irinotécan]):
-
lopéramide à dose élevée
-
octréotide en cas de résistance
-
gestion active des liquides et des électrolytes
Fatigue:
-
information et sensibilisation
-
thérapie par l’activité physique ciblée
-
hygiène du sommeil
-
contrôle des symptômes (anémie/douleur/dépression)
NPIC (neuropathie périphérique induite par la chimiothérapie):
-
prévention par l’adaptation des doses et du calendrier
-
traitement axé sur les symptômes, notamment la duloxétine en cas de neuropathie douloureuse1
Immunothérapie: reconnaître, graduer et communiquer les irAE
Les inhibiteurs de points de contrôle immunitaires entraînent des effets indésirables multisystémiques (cutanés, digestifs, pulmonaires, hépatiques, endocriniens, cardiaques ou neurologiques).
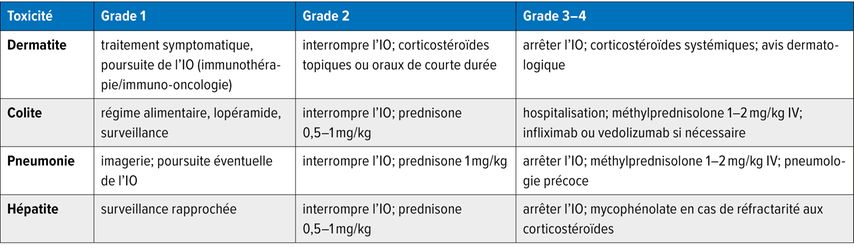
Les recommandations ESMO 2022 et ASCO (American Society of Clinical Oncology) 2021, sur la base du CTCAE («common terminology criteria for adverse events»), les grades de sévérité (1–4), les modalités diagnostiques et thérapeutiques, y compris l’introduction et la décroissance des corticoïdes ainsi que l’immunosuppression de deuxième ligne (p.ex. infliximab, mycophénolate).
Une démarche diagnostique à bas seuil est recommandée (analyses de laboratoire incluant l’axe TSH/cortisol, examens de selles, imagerie, endoscopie si nécessaire), ainsi qu’un passeport d’urgence avec une voie de contact disponible 24h/24 et 7j/7.3,4
Tab.2: Algorithme court de prise en charge des irAE («immune-related adverse events») (sélection; modifié selon Haanen JBAG et al. et Schneider BJ et al.)3,4
Recommandations pratiques
Immunothérapie/immuno-oncologie
-
En cas d’endocrinopathies (hypo-/hyperthyroïdie, hypophysite, insuffisance surrénalienne), une substitution est mise en place; la poursuite de l’IO(immunothérapie/immuno-oncologie) est possible après stabilisation.3,4
-
Une réexposition après un irAE («immune-related adverse event») de grade 2–3 est possible, mais doit être décidée au cas par cas (organe concerné, évolution, risque de récidive).3,4
-
La documentation et la formation (schéma corticoïde, signes d’alerte) réduisent les réhospitalisations.3,4
Inhibiteurs de tyrosine kinase: gérer la triade en toute sécurité au quotidien
Sous VEGF-(T)KI («Vascular endothelial growth factor-tyrosine kinase inhibitors»), l’hypertension constitue l’effet indésirable principal.
La Société européenne de cardiologie (ESC) 2022 recommande les «inhibiteurs de l’ECA» (enzymes de conversion de l’angiotensine), les antagonistes des récepteurs de l’angiotensine (ARA) ou les antagonistes calciques dihydropyridiniques (p. ex. amlodipine) comme antihypertenseurs de premier choix; le vérapamil et le diltiazem doivent être évités en raison des interactions. L’objectif est d’assurer la continuité du traitement oncologique sans complication cardiovasculaire.
Les toxicités cutanées (notamment la réaction main-pied-peau, HFSR) sont prises en charge par des soins à base d’urée, une diminution des pressions mécaniques et, en cas de grade 2–3, par des pauses ou des réductions de dose associées à des corticostéroïdes topiques. Une diarrhée persistante nécessite une gestion des électrolytes et un contrôle des interactions; en cas de diarrhée de grade ≥3, une adaptation de la dose ou une interruption du traitement est indiquée conformément à l’information professionnelle et aux directives.
Le monitoring du QTc (intervalle QT corrigé) est obligatoire pour certains ITK sélectionnés (p. ex. inhibiteurs de BCR-ABL).5
Littérature:
1 Leitlinienprogramm Onkologie (DKG/DKH/AWMF), S3-Leitlinie: Supportive Therapie bei onkologischen Patient:innen. Version 2.0; 02.04.2025. AWMF-Registernummer 032-054OL 2 Jordan K et al.: Emetic risk classification and evaluation of the emetogenicity of antineoplastic agents — updated MASCC/ESMO consensus recommendation. Support Care Cancer 2023/2024; 32(1): 53 3 Haanen JBAG et al.: Management of toxicities from immunotherapy: ESMO Clinical Practice Guideline. Ann Oncol 2022; 33(12): 1217-38 4 Schneider BJ et al.: Management of immune-related adverse events in patients treated with immune checkpoint inhibitor therapy: ASCO Guideline Update. J Clin Oncol 2021; 39(36): 4073-126 5 Lyon AR et al.: 2022 ESC Guidelines on cardio-oncology (EHA/ESTRO/IC-OS). Eur Heart J 2022; 43(41): 4229-361
Das könnte Sie auch interessieren:
Nouveaux résultats d’études à San Antonio
La prise en charge individualisée du carcinome mammaire est déjà très avancée dans la pratique clinique quotidienne. Néanmoins, des récidives tumorales surviennent et des patient·es ...
Mise à jour: comment éviter les transfusions?
Chez les patient·es à faible risqueatteint·es de syndromes myélodysplasiques (SMD), l’anémie nécessitant des transfusions constitue souvent le principal problème altérant la qualité de ...
La radiothérapie adjuvante à l’ère des thérapies systémiques modernes
La radiothérapie adjuvante demeure un élément central dans le traitement des tumeurs malignes cutanées, malgré les progrès réalisés avec les immunothérapies et les thérapies ciblées. ...