Le Pelargonium sidoides est-il une option thérapeutique chez les enfants atteints du syndrome mains-pieds-bouche?
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Une étude a examiné pour la première fois l’extrait de racine de Pelargonium sidoides EPs®7630 chez des enfants atteints du syndrome mains-pieds-bouche et a démontré une réduction significative de l’intensité des symptômes ainsi que de la durée de la maladie chez les enfants traités.1
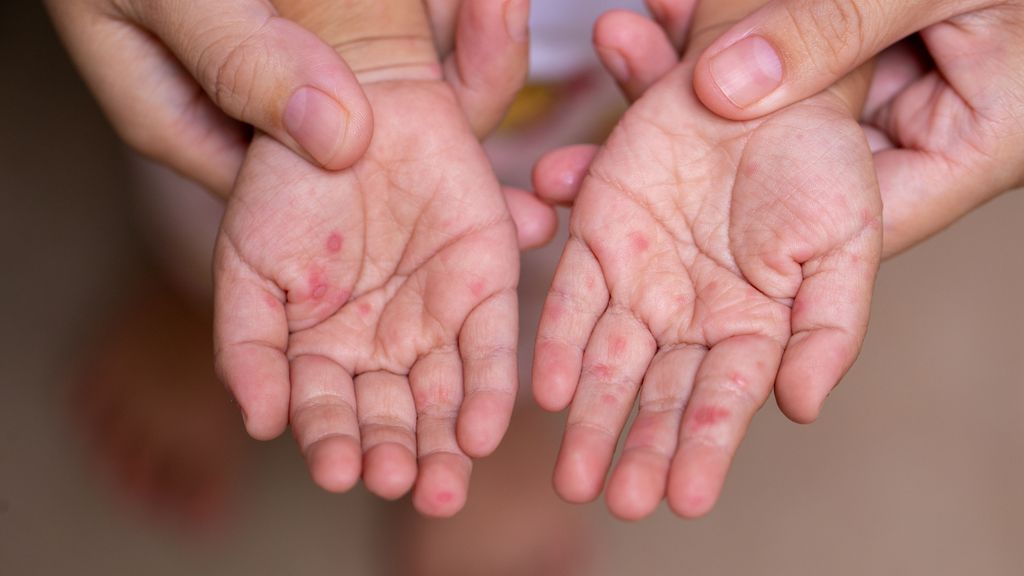
Le syndrome pieds-mains-bouche (HFMD) est une maladie infectieuse virale contagieuse très répandue chez les enfants, causée par des entérovirus humains et des virus Coxsackie. Il n’existe aucun traitement spécifique pour l’HFMD. Les propriétés antivirales, antibactériennes et immunomodulatrices de l’extrait de racine de Pelargonium sidoides EPs®7630 ont déjà été démontrées dans plusieurs études in vitro et in vivo2,3, ainsi que son efficacité contre les infections respiratoires.4–8 L’EPs®7630 s’est révélé particulièrement efficace contre les virus enveloppés, dont le VRS, le virus parainfluenza, le virus de la grippe A (H1N1, H3N2) et le coronavirus humain (HCoV-229E). Cependant, il a également été mis en évidence que l’EPs®7630 inhibe le virus Coxsackie non enveloppé.7 L’utilisation de ce médicament à base de plantes n’a toutefois pas encore été étudiée chez les enfants atteints d’HFMD.
EPs®7630 chez les enfants atteints d’HFMD
Sütçü et al. ont donc mené une étude clinique multicentrique, randomisée, prospective auprès de 208 enfants atteints d’HFMD. Le diagnostic a été posé par des pédiatres et les enfants ont été inclus dans l’étude dans les 48 heures suivant l’apparition des symptômes (première apparition de fièvre et de symptômes cutanés). Ils ont été répartis en deux groupes: un groupe sous EPs®7630 de 94 enfants et un groupe de contrôle de 96 enfants. L’âge moyen était de 27 mois (12–112) et le ratio garçons/filles de 0,98. Tous les enfants ont été évalués avant le début du traitement et ont fait l’objet de deux examens de suivi, 48 heures après la première admission et aux jours 5–7.
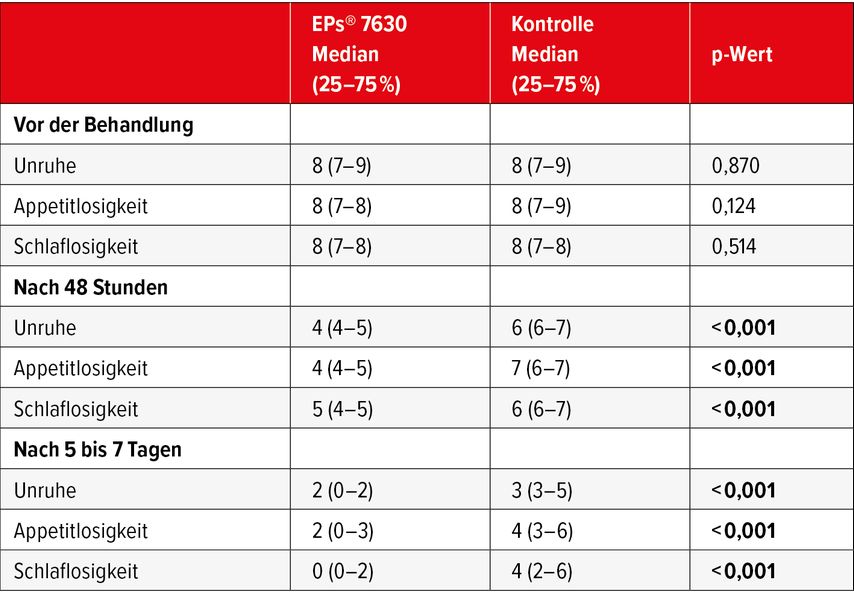
Lors des deux examens de suivi, l’intensité des symptômes était significativement plus faible dans le groupe sous EPs®7630 par rapport au groupe de contrôle (p<0,001; Tab.1). La durée moyenne de la maladie (± ET) était significativement plus courte dans le groupe sous EPs®7630 (6,07 ± 0,70 jours; IC à 95%: 5,92–6,21) par rapport au groupe de contrôle (8,58 ± 0,94 jours; IC à 95%: 8,39–8,77; p<0,001). En outre, le taux d’hospitalisation était significativement plus faible dans le groupe sous EPs®7630 (p=0,019). Aucun effet secondaire n’a été observé, à l’exception d’un goût désagréable rapporté par 5 enfants du groupe sous EPs®7630.
Tab.1: Intensité des symptômes, évaluée par les parents sur une échelle de 0 à 10, avant le traitement ainsi que 48 heures et 5 à 7 jours après le début du traitement1
Conclusion
L’étude montre que l’administration d’EPs®7630 dans les 48 heures suivant l’apparition des symptômes réduit significativement leur intensité chez les enfants atteints d’HFMD et est bien tolérée. Compte tenu de son profil d’efficacité et de sécurité, les auteur·es considèrent l’EPs®7630 comme une option thérapeutique à base de plantes possible pour les enfants atteints d’HFMD. Il·elles constatent toutefois également que des études supplémentaires sont nécessaires pour évaluer l’efficacité de l’EPs®7630 par rapport aux approches thérapeutiques conventionnelles et pour examiner son action antivirale contre les entérovirus. (red)
Littérature:
1 Sütçü M et al.: Hand, foot, and mouth disease: could EPs® 7630 be a treatment option? A prospective randomized open-label multicenter clinical study. Front Pediatr 2024; 12: 1274010 2 Timmer A et al.: Cochrane Database Syst Rev 2013; 22: CD006323 3 Matthys H et al.: J Lung Pulm Respir Res 2016; 3: 4-15 4 Careddu D, Pettenazzo A: Int J Gen Med 2018; 11: 91-8 5 Kolodziej H, Kiderlen AF: Phytomedicine 2007: 6: 18-26 6 Thäle C et al.: Planta Med 2017; 77: 718-25 7 Michaelis M et al.: Phytomedicine 2011; 18: 384-6 8 Theisen LL, Muller CP: Antiviral Res 2012; 94: 147-56
Das könnte Sie auch interessieren:
Gérer les effets indésirables de manière ciblée: pratique selon les directives S3 et internationales
Les thérapies systémiques contre le cancer prolongent la survie et permettent de contrôler les maladies tumorales. Il est déterminant que les patient·es tolèrent bien le traitement. Cela ...
Mise à jour: comment éviter les transfusions?
Chez les patient·es à faible risqueatteint·es de syndromes myélodysplasiques (SMD), l’anémie nécessitant des transfusions constitue souvent le principal problème altérant la qualité de ...
La radiothérapie adjuvante à l’ère des thérapies systémiques modernes
La radiothérapie adjuvante demeure un élément central dans le traitement des tumeurs malignes cutanées, malgré les progrès réalisés avec les immunothérapies et les thérapies ciblées. ...