Traitement hypolipémiant chez les personnes vivant avec le VIH
Auteure:
Dre méd. Anja Vogt
Medizinische Klinik und Poliklinik IV
Klinikum der Ludwig-Maximilians-Universität München
E-mail: anja.vogt@med.uni-muenchen.de
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Les personnes vivant avec le virus de l’immunodéficience humaine (VIH) présentent un risque accru de maladies cardiovasculaires athéroscléreuses. De plus, le traitement antirétroviral et le traitement antirétroviral hautement actif peuvent entraîner une détérioration des taux de lipides et donc une nouvelle augmentation du risque cardiovasculaire.1 La gestion individuelle des lipides est donc décisive pour la réduction du risque cardiovasculaire, et il existe un grand potentiel d’amélioration dans ce domaine.
Keypoints
-
Les personnes vivant avec le VIH présentent un risque nettement accru de maladies cardiovasculaires (CV).
-
Les facteurs de risque CV doivent être déterminés chez toutes les personnes concernées.
-
Le traitement doit être instauré précocement, axée sur les valeurs cibles et suivi de manière durable.
-
Les triglycérides, souvent élevés, sont réduits avant tout par l’adaptation des facteurs du mode de vie.
-
La réduction du C-LDL au moyen d’une statine, d’ézétimibe et d’inhibiteurs de PCSK9 est efficace et réduit significativement les événements CV. Les interactions doivent être évaluées.
-
On observe également un manque cruel de soins en matière de prévention CV chez les personnes vivant avec le VIH. Il existe un grand potentiel de réduction des événements CV grâce à un traitement hypolipémiant.
Des études montrent que le risque relatif de maladies cardiovasculaires est multiplié par 1,6 chez les personnes vivant avec le VIH par rapport aux personnes non infectées, et par deux sous traitement antirétroviral.2–4
Selon l’European AIDS Clinical Society (EACS), les taux de lipides doivent être contrôlés au moment du diagnostic du VIH, avant le début du traitement antirétroviral et régulièrement par la suite.5 En ce qui concerne les valeurs cibles du cholestérol-LDL (C-LDL), la directive EACS actuelle reprend les valeurs cibles de la directive de l’European Society of Cardiology/European Atherosclerosis Society (ESC/EAS): <3.0mmol/l pour un risque faible, <2,6mmol/l pour un risque modéré, <1,8mmol/l pour un risque élevé et <1,4mmol/l pour un risque très élevé.6 En revanche, les directives ESC/EAS recommandent systématiquement une valeur cible de C-LDL <1,8mmol/l chez les personnes vivant avec le VIH.6 Outre la recommandation de modifications du mode de vie et l’adaptation éventuelle du traitement antirétroviral (hautement actif) ([HA]ART), les deux directives conseillent d’utiliser en premier lieu des statines. Des médicaments sont en cours de développement pour réduire la lipoprotéine(a) (Lp[a]). En cas de Lp(a) élevée, il est actuellement recommandé d’améliorer tous les autres facteurs de risque, en particulier le C-LDL.7 Chez les patient·es à haut risque, l’aphérèse des lipoprotéines doit être envisagée.
L’optimisation des facteurs du mode de vie (sevrage tabagique, régime alimentaire et boisson, activité physique) est importante pour tou·tes les patient·es et notamment pour réduire les triglycérides (TG; valeur limite <1,7mmol/l) et améliorer consécutivement le cholestérol-HDL.
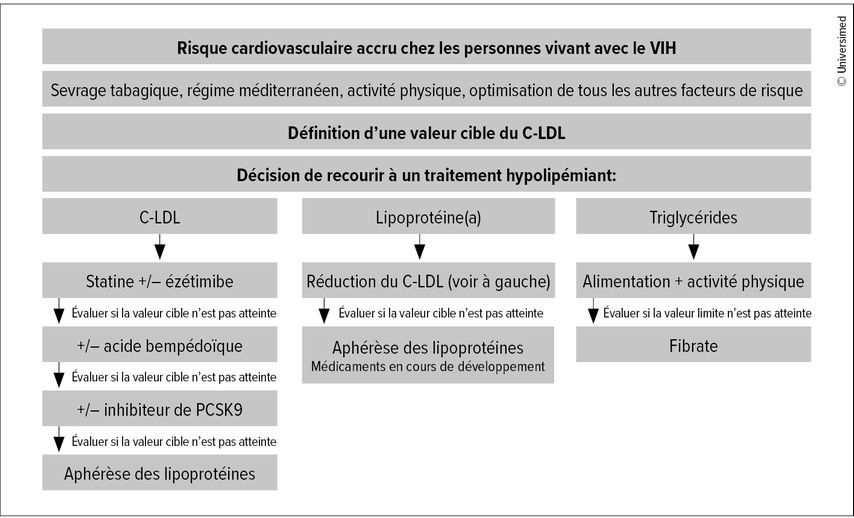
Plusieurs classes de substances sont disponibles pour réduire le C-LDL (Fig.1).Le traitement par un fibrate visant à faire baisser les TG est rarement nécessaire. Le choix et la posologie des hypolipémiants doivent être évalués afin d’éviter toute interaction avec l’(HA)ART (vérificateur d’interaction). La simvastatine et la lovastatine sont en principe contre-indiquées en raison de leur potentiel d’interaction. Pour l’atorvastatine et la rosuvastatine, la dose doit être adaptée en fonction du traitement du VIH spécifique. La pitavastatine est optimale, car elle ne présente aucun potentiel d’interaction et convient donc parfaitement au traitement des personnes vivant avec le VIH. Il s’agit de la septième statine commercialisée dans le monde. La dégradation se fait principalement par glucuronidation et élimination sous forme de lactone inactive, la dégradation par les enzymes du cytochrome P450 est insignifiante, ce qui explique l’excellent profil de tolérance pharmacocinétique chez les personnes vivant avec le VIH.8
Fig.1: Traitement hypolipémiant chez les personnes vivant avec le VIH (modifiée selon Mach F et al. 2019)6
Études récentes
L’étude de phase III «Pitavastatin to Prevent Cardiovascular Disease in HIV Infection» («Randomized Trial to Prevent Vascular Events in HIV»; REPRIEVE)9 souligne de manière impressionnante à la fois les avantages de la pitavastatine et le bénéfice du traitement hypolipémiant pour les personnes vivant avec le VIH présentant un risque cardiovasculaire nominal faible ou modéré. 7769 personnes vivant avec le VIH, âgées de 40 à 75 ans, sous traitement antirétroviral stable et présentant un risque cardiovasculaire athéroscléreux faible à modéré ont été incluses (score médian de maladie cardiovasculaire athéroscléreuse [ASCVD] à 10 ans: 4,5%). Les patient·es sous traitement par une statine ou atteint·es d’ASCVD ont été exclu·es. L’ensemble des patient·es ont obtenu des informations sur les modifications du mode de vie et ont reçu quotidiennement soit 4mg de pitavastatine, soit un placebo. L’adhésion thérapeutique était très bonne: elle était «excellente» ou «très bonne» chez >80% des patient·es et au moins «bonne» chez >95%. Le critère d’évaluation primaire était la survenue d’un événement indésirable cardiovasculaire majeur («MACE»), défini comme la combinaison d’un décès d’origine cardiovasculaire, d’un infarctus du myocarde, d’une hospitalisation pour angor instable, d’un accident vasculaire cérébral, d’un accident ischémique transitoire, d’une ischémie artérielle périphérique, d’une revascularisation ou d’un décès de cause indéterminée.
Après une durée de suivi médiane de 5,1 ans, l’étude a été arrêtée prématurément en raison d’une grande efficacité. Le bras sous pitavastatine a présenté un taux significativement plus faible de MACE (4,81 par rapport à 7,32 événements pour 1000 personnes-années; hazard ratio [HR]: 0,65). La cohorte sous pitavastatine a également obtenu des résultats significativement meilleurs dans l’analyse «MACE ou décès», avec un HR de 0,79. Ces effets ont persisté après ajustement selon les facteurs de risque cardiovasculaire, les caractéristiques démographiques des patient·es et les facteurs associés au VIH. Le C-LDL a été réduit de 2,77 à 1,91mol/l (médiane) sous pitavastatine, alors qu’il est resté pratiquement inchangé dans le bras sous placebo (de 2,74 à 2,72mmol/l). En ce qui concerne les effets indésirables, les deux bras de l’étude ont présenté un taux presque identique d’événements indésirables graves d’issue non fatale. Cependant, un taux légèrement plus élevé de diabète (défini comme un diabète diagnostiqué avec initiation d’un antidiabétique) a été observé dans le bras sous pitavastatine. En outre, les myalgies/myopathies étaient plus fréquentes sous pitavastatine, mais les myopathies/myalgies, les rhabdomyolyses ou les troubles de la fonction hépatique significatifs étaient très rares et comparables dans les deux bras.
Une étude sur la fréquence de prescription des statines révèle un manque cruel de soins chez les personnes vivant avec le VIH.10 Malgré le risque accru d’ASCVD connu depuis longtemps dans cette population, seules 38,8% des 440 personnes pour lesquelles le traitement par une statine est indiqué selon les directives (ASCVD, diabète et C-LDL élevé, C-LDL très élevé, score ≥7,5%) se sont vu prescrire des statines. Pour le groupe atteint d’ASCVD relativement facile à identifier (n=40), ce chiffre était tout de même, mais seulement, de 62,5%; il n’était plus que de 27,9% en cas de score élevé. Les patient·es présentant un risque faible à modéré d’ASCVD, pour lesquel·les l’étude REPRIEVE a également montré un bénéfice net, n’ont pas été étudié·es.
Réduction du C-LDL
Parmi les statines, la pitavastatine présente le profil d’interaction le plus favorable. En Allemagne, le montant fixe pris en charge par les caisses-maladie ne couvre qu’une fraction des coûts de la pitavastatine, de sorte que les patient·es doivent financer eux·elles-mêmes la majeure partie des coûts. Dans la pratique quotidienne, d’autres statines sont donc privilégiées. En cas de tolérance réduite aux statines ou si la valeur cible du C-LDL n’est pas atteinte, on ajoute l’ézétimibe et, en troisième option, l’acide bempédoïque. Si la valeur cible du C-LDL n’est pas atteinte, l’ajout (et non le remplacement par) d’un inhibiteur de PCSK9 (évolocumab et alirocumab) doit être envisagé.5 Il existe des données favorables sur l’efficacité et la tolérance de l’évolocumab chez les personnes vivant avec le VIH.11 Aucune interaction n’est attendue avec ces substances. L’étude des critères d’évaluation portant sur l’inclisiran (siRNA anti-PCSK9) est toujours en cours.
Ces excellentes options thérapeutiques pour la réduction des événements cardiovasculaires doivent être présentées de manière positive, surtout si des effets secondaires sont redoutés.12
Résumé
Les personnes vivant avec le VIH présentent un risque cardiovasculaire élevé, qui est encore accru par le traitement antirétroviral. Même en cas de risque cardiovasculaire nominal modéré ou faible, elles bénéficient nettement d’un traitement visant à réduire le C-LDL, et les directives recommandent aussi de réduire le C-LDL. Le traitement de première intention est une statine. Pour atteindre la valeur cible du C-LDL, le traitement doit être adapté individuellement en utilisant les différentes classes de substances.
Littérature:
1 Riddler SA et al.: JAMA 2003; 289: 2978-82 2 Bavinger C et al.: PLoS One 2013; 8: e59551 3 Hemkens LG, Bucher HC: Eur Heart J 2014; 35: 1373-81 4 Islam FM et al.: HIV Med 2012; 13: 453-68 5 Ambrosioni J et al.: HIV Med 2023; 24: 1126-36 6 Mach F et al.: 2019 ESC/EAS Eur Heart J 2020; 41: 111-88 7 Kronenberg F et al.: Eur Heart J 2022; 43: 3925-46 8 Baker WL, Datta R: Adv Ther 2011; 28: 13-27 9 Grinspoon SK et al.: N Engl J Med 2023; 389: 687-99 10 Wu PY et al.: J Microbiol Immunol Infect 2024; 57: 200-3 11 Boccara F et al.: Am Heart J 2020; 220: 203-12 12 Vogt A: Inn Med (Heidelb) 2023; 64: 622-8
Das könnte Sie auch interessieren:
Études actuelles sur le traitement de l’ILD
Le terme pneumopathie interstitielle (ILD) est un terme générique désignant un groupe important et hétérogène de maladies qui se manifestent principalement dans l’espace broncho- ...
Mise à jour 2026: vers la modification de la maladie
Un grand nombre de médicaments biologiques immunomodulateurs et de «small molecules» ont considérablement élargi l’éventail des options thérapeutiques dans les maladies inflammatoires ...
Schémas thérapeutiques de référence plus courts dans la tuberculose
La tuberculose (TB) constitue toujours un défi majeur à l’échelle mondiale. Malgré les progrès, le besoin de schémas thérapeutiques plus efficaces, plus courts et mieux tolérés reste ...