De nouvelles données sur le cancer du sein précoce qui améliorent la thérapie dans la pratique
Compte-rendu:
Dre Ine Schmale
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Les résultats présentés lors du congrès ESMO de cette année concernant le traitement du cancer du sein précoce vont modifier les standards thérapeutiques, tant pour les patient·es HER2-positif·ves que pour celles et ceux présentant un cancer HER2-négatif/HR-positif.
Traitement néoadjuvant par T-DXd en cas de risque élevé
Après plus d’une décennie sans nouvelles options thérapeutiques, un besoin persistant existe pour des traitements plus efficaces et mieux tolérés chez les patient·es à haut risque atteintes d’un cancer du sein précoce HER2-positif (HER2+). L’étude DESTINY-Breast11 a évalué si le trastuzumab deruxtecan (T-DXd) pouvait améliorer l’efficacité et la sécurité en situation néoadjuvante.1
Dans cette étude randomisée à trois bras, 927 patient·es ont reçu en néoadjuvant: 4 cycles de T-DXd suivis de 4 cycles de THP (paclitaxel, trastuzumab, pertuzumab), ou 4 cycles de doxorubicine-cyclophosphamide plus paclitaxel (ddAC) suivis de 4 cycles de THP, ou encore 8 cycles de T-DXd. Le troisième bras de l’étude a été interrompu de manière prématurée, la probabilité d’une supériorité par rapport au ddAC-THP étant faible et l’intégration temporelle de la chirurgie posant des difficultés. Le critère d’évaluation primaire de l’étude était la rémission complète pathologique (pCR: ypT0/is ypN0).
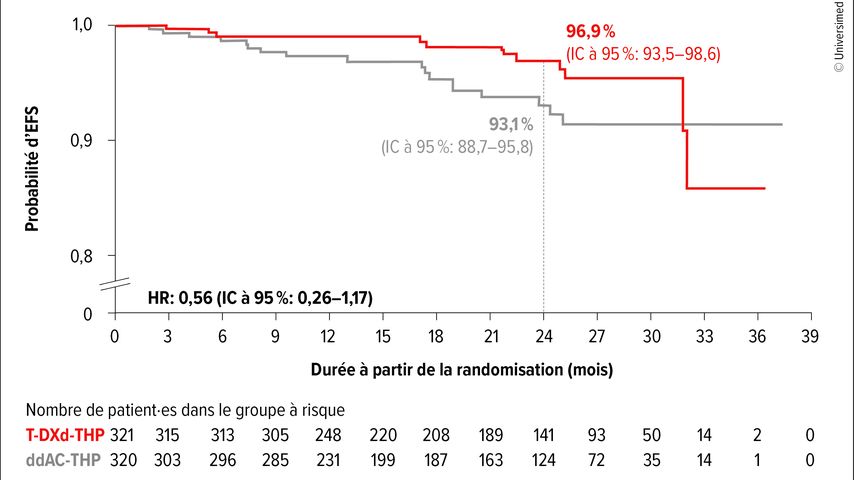
Dans les trois bras de l’étude, 99,7% vs 97,5% vs 99,0% des patient·es randomisé·es ont reçu le traitement de l’étude, et 97,2% vs 93,8% vs 95,8% ont finalement subi une résection. L’âge médian était de 50 ans; 72–73% présentaient une tumeur HR-positive et 88–89% un statut ganglionnaire positif. Dans la comparaison des bras de l’étude avec T-DXd-THP versus ddAC-THP, une pCR a été obtenue chez 67,3% versus 56,3% des patient·es. L’écart absolu était de 9,1% (61,4% vs 52,3%) dans le groupe HR-positif et de 16,1% (83,1% vs 67,1%) dans le groupe HR-négatif. L’avantage du T-DXd par rapport au ddAC en termes de survie sans événement (EFS) n’a pas encore atteint la signification statistique, avec un rapport de risque (HR) de 0,56 pour une maturité des données de 4,5% (IC à 95%: 0,26–1,17). Les courbes de Kaplan-Meier se séparaient précocement, avec des taux d’EFS à 24 mois de 96,9% contre 93,1% (Fig.1). Le profil de sécurité était plus favorable sous T-DXd-THP que sous ddAC-THP. Des effets indésirables de grade≥3 sont survenus chez 37,5% contre 55,8% des patient·es, et des effets indésirables cliniquement significatifs chez 10,6% contre 20,2%. Une pneumopathie interstitielle/pneumopathie liée au traitement a été observée chez 4,4% contre 5,1% des patient·es et un dysfonctionnement ventriculaire gauche chez 1,3% contre 6,1%. Les effets indésirables ont entraîné un retard opératoire chez 3,4% contre 2,6% des patient·es. L’arrêt d’au moins un médicament de l’étude est survenu chez 37,8% contre 54,5% des patient·es pour cause d’effets indésirables; 14,1% contre 9,9% ont interrompu l’ensemble du traitement.
Fig.1: Survie sans événement (EFS) avec T-DXd-THP en néoadjuvant versus ddAC-THP chez des patient·es à haut risque atteint·es d’un cancer du sein HER2+ (modifiée selon Harbeck N et al.)1
La comparaison du troisième bras de l’étude (T-DXd seul) par rapport au ddAC-THP a montré un taux de pCR plus faible (43,0% vs 56,3%), mais une EFS comparable (HR: 0,82; IC à 95%: 0,41–1,62) avec des taux à 24 mois de 94,4% vs 93,1%. Le profil de tolérance était du T-DXd était plus favorable que celui du ddAC-THP. Chez 6,4% des patient·es du bras T-DXd, la chirurgie a été reportée en raison d’effets indésirables.
Conclusion
Les résultats de l’étude DESTINY-Breast11 indiquent que le traitement néoadjuvant par T-DXd-THP est plus efficace et mieux toléré que ddAC-THP et pourrait devenir le schéma privilégié pour les patient·es à haut risque atteint·es d’un cancer du sein précoce HER2+.
T-DXd adjuvant: possible nouveau standard
Après un traitement néoadjuvant, les patient·es à HER2+ précoce à haut risque présentant une maladie résiduelle invasive nécessitent une stratégie adjuvante intensive et efficace. L’étude DESTINY-Breast05 est une étude mondiale, multicentrique, randomisée, ouverte, de phaseIII, qui a comparé l’efficacité et la sécurité du traitement adjuvant par T-DXd à celles du trastuzumab emtansine (T-DM1) dans cette population de patient·es.2 Au total, 1635 patient·es ont été randomisé·es pour recevoir 14 cycles (q3w) de T-DXd ou de T-DM1. Le critère d’évaluation primaire de l’étude était la survie sans maladie invasive (IDFS).
Avec un suivi médian de 30 mois, 72–76% des participant·es avaient complété le traitement. Le traitement a été interrompu chez 17,9% (T-DXd) et 12,7% (T-DM1) en raison d’effets indésirables, et chez 0,2% et 3,7% en raison d’une récidive. En termes d’efficacité, le T-DXd a entraîné une réduction significative de 53% du risque de rechute invasive de la maladie par rapport au T-DM1 (HR: 0,47; IC à 95%: 0,34–0,66; p<0,0001). À 3 ans, 92,4 contre 83,7% des patient·es étaient en vie sans rechute invasive de la maladie. Parmi les 42 cas de métastases à distance rapportés sous T-DXd, 17 étaient des métastases cérébrales et 25 concernaient d’autres localisations. Dans le bras T-DM1, 77 métastases à distance ont été observées au total, dont 25 au niveau cérébral et 52 dans d’autres organes. Une réduction de 53% du risque (HR: 0,47; IC à 95%: 0,34–0,66; p<0,0001) a été observée pour la survie sans maladie (DFS), avec des taux de DFS à 3 ans de 92,3% contre 83,5%. Pour la survie globale (OS), un signal en faveur d’un bénéfice associé au traitement adjuvant par T-DXd a été observé, sur la base de 47 événements et avec une maturité des données de 2,9%. Le HR pour l’OS était de 0,61 (IC à 95%: 0,34–1,10) et les taux d’OS à 3 ans étaient de 97,4% contre 95,7%. Les effets indésirables étaient globalement plus fréquents sous T-DXd que sous T-DM1, mais demeuraient généralement gérables. La différence observée dans les taux d’arrêt du traitement était liée aux cas de pneumonie/DLI sous T-DXd (10,8% vs 2,5% d’arrêts du traitement). Aucun nouveau signal de sécurité n’a été identifié.
Conclusion
Les données d’efficacité de l’étude DESTINY-Breast05 soutiennent l’utilisation du T-DXd comme nouveau standard de traitement adjuvant chez les patient·es atteint·es d’un cancer du sein précoce HER2-positif à haut risque présentant des résidus tumoraux invasifs après une thérapie néoadjuvante. Les effets indésirables étaient plus fréquents qu’avec le T-DM1, mais restaient gérables.
Conséquence adjuvante après évaluation du risque dans le cancer du sein HER2-/HR+
L’étude SOLTI-RIBOLARIS a été conçue pour examiner l’hypothèse selon laquelle un downstaging moléculaire obtenu grâce à une thérapie endocrinienne (ET) associée à un inhibiteur de CDK4/6 pourrait permettre à des patient·es atteint·es d’un cancer du sein HER2-/HR+ à haut risque d’éviter la chimiothérapie.3
Au total, 1100 patient·es pré- et post-ménopausées présentant un cancer du sein de stade cliniqueII, grade2 ou 3, ont été incluses. Le traitement reposait sur 24 semaines de ribociclib (600mg) associé au létrozole (± LHRH) suivies de la résection. La cohorte présentant un faible risque de progression («ROR low»), défini par un score ROR(«risk of recurrence») ≤30 points pour N0, ≤20 points pour N1mi et ≤10 points pour N1, a reçu en adjuvant du ribociclib (400mg) plus létrozole (± LHRH), puis une ET (± LHRH) pendant 2,5 ans. Les patient·es ayant un score ROR intermédiaire ou élevé ont également reçu une chimiothérapie adjuvante. Le critère d’évaluation principal de l’étude était la survie sans métastases à distance (DMFS) dans la cohorte à faible score ROR.
Les données postopératoires de 686 patient·es – dont 38,2% en pré- ou périménopause – ont été analysées. Parmi elles, 52,6% de ces patient·es présentaient un risque faible de récidive selon le score ROR. Comparé·es à la cohorte ayant un score ROR intermédiaire/élevé, les patient·es à faible risque étaient plus fréquemment en pré- ou périménopause (43,6% vs 32,1%), présentaient plus souvent un statut T pathologique (ypT1: 65,9% vs 48,9%), un statut N pathologique (ypN0: 69,5% vs 24,6%), et avaient plus souvent bénéficié d’une chirurgie conservatrice du sein (77,0% vs 70,2%). Les premiers résultats indiquent que 16,8% des patient·es ont interrompu le traitement en raison d’effets indésirables. Durant le traitement néoadjuvant, une progression tumorale a été observée chez 15 patient·es (2,19%).
Conclusion
Les résultats de l’étude RIBOLARIS suggèrent qu’une proportion substantielle de patient·es atteint·es d’un cancer du sein HER2-/HR+ à haut risque de récidive peut atteindre un faible score ROR après un traitement néoadjuvant par ribociclib et létrozole, permettant potentiellement d’éviter la chimiothérapie.
L’inhibiteur adjuvant de CDK4/6 prolonge la survie globale
Dans l’étude monarchE, 2 ans d’abemaciclib adjuvant, associé à une ET, ont significativement amélioré l’IDFS par rapport à l’ET seul chez des patient·es atteint·es d’un cancer du sein HER2-/HR+ avec atteinte ganglionnaire positive et risque élevé de récidive. Les premières données d’OS, présentées au congrès ESMO 2025, reposent sur un suivi médian de 76 mois.4
L’abemaciclib a réduit de 16% le risque de décès (HR: 0,84; IC à 95%: 0,72–0,98; p=0,027). Les courbes de Kaplan-Meier montrent une séparation croissante des courbes après 5 ans (Fig.2). Dans la population ITT, au moment de l’analyse, 2,8% contre 2,3% des patient·es étaient décédé·es d’une cause non liée au cancer, 7,9% contre 10,5% étaient décédé·es du cancer, et 6,4% contre 9,4% vivaient avec une maladie métastatique. Inversement, 85,7% contre 80,1% des patient·es étaient en vie sans maladie métastatique. Aucun nouveau signal de sécurité n’a été rapporté malgré l’allongement de la période d’observation.
Fig.2: Survie globale (OS) sous traitement adjuvant par abemaciclib+ET vs ET chez les patient·es à haut risque atteint·es d’un cancer du sein HER2-/HR+ (modifiée selon Johnston R et al.)4
Conclusion
L’abemaciclib a démontré un allongement statistiquement significatif de l’OS chez les patient·es atteint·es d’un cancer du sein HER2-/HR+, à haut risque et avec atteinte ganglionnaire positive.
Source:
Congrès annuel de l’European Society for Medical Oncology (ESMO), 17–21 octobre 2025, Berlin et en ligne
Littérature:
1 Harbeck N et al.: DESTINY-Breast11: neoadjuvant trastuzumab deruxtecan alone (T-DXd) or followed by paclitaxel + trastuzumab + pertuzumab vs SOC for high-risk HER2+ early breast cancer. ESMO 2025; Abstr. #291O 2 Geyer CE et al.: Trastuzumab deruxtecan vs trastuzumab emtansine in patients with high-risk human epidermal growth factor receptor 2-positive (HER2+) primary breast cancer with residual invasive disease after neoadjuvant therapy: interim analysis of DESTINY-Breast05. ESMO 2025; Abstr. #LBA1 3 Cottu PH et al.: Risk of recurrence after neoadjuvant ribociclib plus ET in clinically high-risk ER+/HER2- BC: preliminary analysis of the SOLTI-RIBOLARIS trial. ESMO 2025; Abstr. #296O 4 Johnston R et al.: monarchE: primary overall survival results of adjuvant abemaciclib + endocrine therapy for HR+, HER2-, high-risk early breast cancer. ESMO 2025; Abstr. #LBA13
Das könnte Sie auch interessieren:
Études actuelles sur le traitement de l’ILD
Le terme pneumopathie interstitielle (ILD) est un terme générique désignant un groupe important et hétérogène de maladies qui se manifestent principalement dans l’espace broncho- ...
Mise à jour 2026: vers la modification de la maladie
Un grand nombre de médicaments biologiques immunomodulateurs et de «small molecules» ont considérablement élargi l’éventail des options thérapeutiques dans les maladies inflammatoires ...
Schémas thérapeutiques de référence plus courts dans la tuberculose
La tuberculose (TB) constitue toujours un défi majeur à l’échelle mondiale. Malgré les progrès, le besoin de schémas thérapeutiques plus efficaces, plus courts et mieux tolérés reste ...
%20sous%20traitement%20adjuvant%20par%20abemaciclib.jpg)