Maladie cœliaque: état d’avancement des options thérapeutiques pharmacologiques
Auteur:
Pr Dr méd. Dr rer. nat. Detlef Schuppan
Direktor des Instituts für Translationale Immunologie, Ambulanz für Zöliakie, Dünndarmerkrankungen und Autoimmunität
Forschungszentrum für Immuntherapie (FZI)
Universitätsmedizin der Johannes Gutenberg Universität Mainz
Beth Israel Deaconess Medical Center
Harvard Medical School
Boston
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Nombre de patient·es atteint·es de la maladie cœliaque continuent à souffrir de troubles malgré un régime sans gluten. Plusieurs approches thérapeutiques innovantes sont actuellement en cours de développement: entre autres, un inhibiteur de la transglutaminase tissulaire (tTG) intestinale, des anticorps anti-interleukine (IL-)15 et le ligand d’OX40 (OX40L), un agoniste de la sirtuine 6 pour renforcer la barrière intestinale et des substances actives pour induire une tolérance au gluten.
Keypoints
-
Actuellement, plusieurs médicaments sont en cours de développement pour le traitement de soutien de la maladie cœliaque.
-
La sécurité et l’efficacité d’un certain nombre de ces médicaments ont déjà été testées dans le cadre d’études cliniques de phase I–II, certains d’entre eux étant efficaces contre les lésions muqueuses induites par le gluten dans la maladie cœliaque.
-
Le développement le plus avancé et le plus prometteur est celui d’un inhibiteur oral de l’enzyme endogène transglutaminase tissulaire (tTG), qui augmente le potentiel immunogène du gluten ingéré.
Avec une prévalence d’environ 1%, la maladie cœliaque est la maladie inflammatoire de l’intestin grêle la plus fréquente. La complexité de ses manifestations cliniques pose de nombreux défis diagnostiques. Outre les troubles gastro-intestinaux, environ 30% des patient·es présentent des symptômes extra-intestinaux et des associations avec d’autres maladies auto-immunes.1Le traitement de base reste le régime sans gluten (GFD) strict à vie. Néanmoins, ce dernier est difficile à suivre au quotidien pour nombre de patient·es: jusqu’à 40% continuent à présenter des troubles et/ou des signes histologiques de la maladie malgré une bonne observance du régime, notamment en raison des inévitables contaminations par des quantités minimes de gluten dans l’alimentation quotidienne.1L’éviction stricte du gluten peut conduire à un rétablissement complet de la muqueuse, mais la régénération prend souvent de nombreux mois, voire des années. Un traitement pharmacologique complémentaire pourrait aider à traiter les rémissions incomplètes, à réduire le risque de contamination par des quantités minimes de gluten et à faciliter le suivi du GFD. Les indications d’un traitement pharmacologique comprennent principalement la maladie cœliaque non-répondeuse («non-responsive coeliac disease», NRCD; environ 10–30%), les formes réfractaires (RCD1, RCD2), la protection dans les «situations à haut risque» et les urgences aiguës après une exposition involontaire.2
Pathogenèse et approches thérapeutiques rationnelles
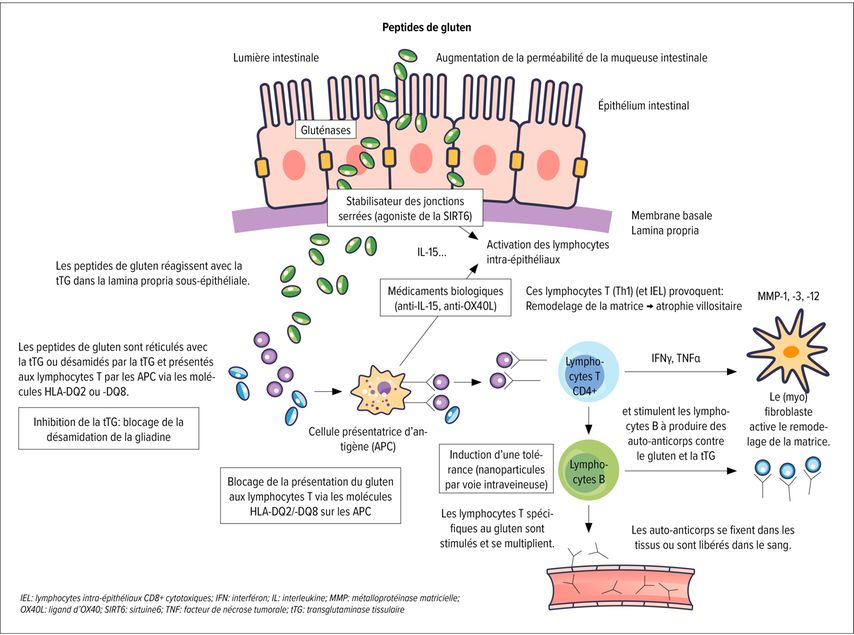
La pathogenèse de la maladie cœliaque est désormais bien comprise, ce qui constitue la base de stratégies pharmacologiques ciblées (Fig.1). L’accent est mis sur l’interaction entre les prédispositions génétiques, les facteurs environnementaux (infections, alimentation, microbiote intestinal, facteurs de stress psychologique, perturbation de la barrière intestinale) et l’activation du système immunitaire muqueux.2
Fig.1: Pathogenèse de la maladie cœliaque dans l’intestin grêle et approches des options thérapeutiques pharmacologiques (modifiée selon Schuppan D et al. 2025)2
Après l’ingestion d’aliments contenant du gluten, certains peptides de gluten partiellement digérés pénètrent dans la muqueuse proximale de l’intestin grêle. La présentation de ces peptides via les molécules HLA-DQ2/-DQ8 situées à la surface des cellules présentatrices d’antigènes (APC; p.ex. monocytes, macrophages, cellules dendritiques) est essentielle pour l’activation des lymphocytes T CD4+ spécifiques du gluten. L’auto-antigène de la maladie cœliaque tTG modifie (désamide) les peptides de gluten de manière à faciliter leur liaison avec les molécules HLA-DQ2/-DQ8. Cela renforce la stimulation et l’expansion des clones de lymphocytes T, ce qui active la réponse immunitaire et l’inflammation. Les lymphocytes intra-épithéliaux (IEL) CD8+ cytotoxiques sont également activés, en particulier sous l’influence de concentrations élevées d’IL-15 et d’IL-21 dans la muqueuse duodénale.
Ce processus complexe entraîne des modifications histologiques caractéristiques: atrophie villositaire, hyperplasie des cryptes et augmentation des lymphocytes intra-épithéliaux. Une exposition continue au gluten, même en quantités infimes, par exemple par contamination, perpétue cette inflammation.3 En cas de troubles malgré le suivi du GFD, le diagnostic différentiel doit prendre en compte la colite microscopique, la pullulation bactérienne de l’intestin grêle, le syndrome du côlon irritable ou d’autres intolérances alimentaires.
Pertinence clinique et indications du traitement pharmacologique
La nécessité de développer des médicaments de soutien découle, d’une part, du taux élevé de patient·es présentant des symptômes persistants/des lésions muqueuses actives malgré le DFG et, d’autre part, des situations à haut risque de contamination (repas hors du domicile, en voyage, etc.). Les médicaments qui permettent aux patient·es atteint·es de la maladie cœliaque de tolérer de faibles quantités de gluten dans leur alimentation amélioreraient considérablement leur qualité de vie.
Les principales indications du traitement pharmacologique (de soutien) sont les suivantes:4
-
Maladie cœliaque non-répondeuse avec exclusion d’autres étiologies
-
Maladie cœliaque réfractaire de type 1 (env. 1–2%)
-
Protection contre l’exposition inévitable au gluten dans des situations à haut risque (p.ex. repas à la cantine, en voyage)
-
Traitement d’urgence après ingestion accidentelle de gluten
-
Prévention des complications à long terme et de l’auto-immunité associée
-
Un GFD partiellement moins strict n’est pas une approche thérapeutique claire à l’heure actuelle, mais pourrait être discuté en combinaison avec un traitement pharmacologique.
Étude scientifique de nouvelles substances actives
Étant donné que les cultures cellulaires et les modèles animaux ne permettent pas de reproduire parfaitement la maladie cœliaque, des études cliniques sont notamment nécessaires pour démontrer l’efficacité et la sécurité des substances actives. Dans des études de phase Ib–II en double aveugle, des patient·es atteint·es de la maladie cœliaque en rémission clinique sont exposé·es au gluten pendant 4 à 12 semaines et traité·es par la substance active par rapport à un placebo. Le critère d’évaluation primaire est l’aggravation ou le maintien d’une histologie duodénale normale (rapport entre la hauteur des villosités et la profondeur des cryptes; dans un deuxième temps également les lymphocytes intra-épithéliaux). Si la substance active améliore significativement l’histologie par rapport au placebo, les résultats rapportés par les patient·es («patient-reported outcomes», PRO) gagnent en importance dans les études de phase IIb–III, notamment comme critères d’évaluation combinés avec l’évaluation histologique. Les PRO ne sont pas sans poser de problèmes, car les patient·es peuvent présenter des troubles de type maladie cœliaque pouvant, entre autres, se chevaucher avec les symptômes d’un syndrome du côlon irritable.
Options thérapeutiques actuelles
Approches thérapeutiques enzymatiques
L’objectif des traitements enzymatiques est de dégrader autant que possible les peptides de gluten immunogènes avant qu’ils ne pénètrent dans la muqueuse intestinale. Ces traitements peuvent réduire l’absorption de gluten, mais n’offrent pas une protection totale. Les approches suivantes ont été étudiées:
-
Latigluténase (ALV003, IMGX003): dans plusieurs études, cette combinaison d’enzymes a efficacement dégradé les protéines de gluten pertinentes, avec une réduction prouvée des symptômes et des effets sur la muqueuse après provocation au gluten.5
-
AN-PEP: une endopeptidase issue d’Aspergillus niger, qui peut également accélérer la dégradation intraluminale du gluten, mais de manière moins efficace. Une étude clinique a testé l’AN-PEP en tant que complément alimentaire.6
-
KUMA-30 (TAK-062): une gluténase optimisée in silico, qui a pu atteindre jusqu’à présent la plus grande activité in vitro contre les peptides de gluten.7 Une étude clinique de phase II est actuellement en cours aux États-Unis.
Modulation de la barrière intestinale
Une autre approche consiste à réduire la perméabilité intestinale, qui est en partie responsable de l’inflammation de l’intestin grêle observée dans la maladie cœliaque. Cela permettrait de minimiser la présence de peptides immunogènes dans la muqueuse.
-
Acétate de larazotide: le stabilisateur des jonctions serrées a montré une tolérance et une amélioration symptomatique dans les études de phase I/II, mais n’a atteint aucun critère d’évaluation histologique convaincant. Une étude de phase III sur l’octapeptide a été arrêtée faute de résultats significatifs.
-
IMU-856: l’activateur oral de la sirtuine 6 (SIRT6) de bas poids moléculaire a révélé une bonne tolérance et une réduction des lésions histologiques en cas de provocation au gluten dans une étude de phase Ib; d’autres études sont prévues.8
Modulation immunitaire
Ces traitements ont pour effet d’inhiber la réponse immunitaire médiée par le gluten dans l’intestin grêle.
-
Blocage du signal des cytokines (PRV-015/AMG714; Caly-002): l’anticorps anti-IL-15 AMG714 a démontré un succès modéré dans les études de provocation au gluten, portant sur la NRCD et la RCD2.9 Un anticorps de haute affinité (Caly-002) a atteint une efficacité supérieure en phase Ib.10
-
Anti-OX40L (amlitelimab): l’OX40L est exprimé par les cellules présentatrices d’antigènes et l’OX40 par les lymphocytes T CD4+, NK et NKT activés ainsi que par les neutrophiles. Le système OX40-OX40L est important, entre autres, pour le développement des lymphocytes T mémoires. L’anticorps anti-OX40L bloque le signal des lymphocytes T mémoires. Depuis mai 2024, des études de phase II menées sur des patient·es atteint·es de NRCD et portant sur l’administration par voie sous-cutanée sont en cours.11
-
Budésonide à libération entérique (gastro-résistant): n’ayant pas fait l’objet d’un essai randomisé contrôlé, le budésonide à libération entérique a montré un succès à court terme chez les patient·es atteint·es de NRCD/RCD1. Son utilisation pourrait être particulièrement utile en cas d’exposition involontaire au gluten.12,4
Blocage de la présentation de la gliadine et inhibition de la tTG
Un blocage de la reconnaissance spécifique par les lymphocytes T CD4+ des peptides de gliadine liés aux molécules HLA-DQ2.5/-DQ8 doit empêcher la réponse immunitaire inflammatoire (DONQ52). L’approche visant à inhiber la tTG a notamment donné des résultats prometteurs (ZED1227/TAK-227).
-
DONQ52: une étude de phase I a confirmé l’efficacité d’un anticorps qui bloque la liaison entre le complexe HLA-DQ2.5-peptide de gluten et le récepteur des lymphocytes T afin d’interrompre la réponse immunitaire nocive qui entraîne des lésions intestinales.13
-
Inhibition de la tTG intestinale (ZED1227/TAK-227): l’inhibiteur oral et spécifique de la tTG a révélé une nette prévention des lésions muqueuses induites par le gluten dans une étude de phase IIa. ZED1227 (TAK-227) fait actuellement l’objet d’une étude de phase IIb mondiale portant sur 400 patient·es atteint·es de NRCD clinique et histologique légère réparti·es dans 100 centres et est considéré comme l’approche thérapeutique la plus avancée. Dans le cadre de l’inhibition de la tTG, outre son efficacité, il est intéressant de noter le ciblage du mécanisme hautement spécifique à la maladie cœliaque, la disponibilité orale de TAK-227 sans exposition systémique élevée et l’effet protecteur prophylactique avant l’exposition au gluten.14,2
Induction d’une tolérance
L’approche préventive et potentiellement curative de l’induction d’une tolérance s’adresse à la mémoire immunitaire. La découverte clé est l’identification des épitopes de gliadine.
-
Immunothérapie spécifique à l’antigène (NexVax2): des études de phase précoce portant sur l’administration par voie sous-cutanée de peptides de gliadine synthétiques étaient prometteuses, l’étude de phase II a été arrêtée en raison d’effets secondaires et de son inefficacité.15
-
TAK-101: des nanoparticules contenant des peptides de gliadine administrées par voie intraveineuse dans le but d’induire une tolérance. Dans une étude de phase Ib, le nombre de lymphocytes T circulants produisant de l’IFNγ a pu être normalisé.16 Une étude de phase II est en cours.
-
KAN-101: un agent conjugué contenant un ligand spécifique au foie et un peptide désamidé d’alpha-gliadine qui se lie à HLA-DQ2.5. La tolérance a été mise en évidence avec une clairance rapide après une seule administration, une étude de phase II est actuellement en cours.17
-
TPM502 (TOPAS): des nanoparticules d’oxyde de fer recouvertes de polymère contenant des peptides antigéniques avec des épitopes centraux du gluten pour HLA-DQ2.5 font également l’objet d’études cliniques de phase IIa et pourraient induire de manière ciblée la réponse immunitaire tolérogène.18
Approches génétiques dans la sélection des céréales
La technologie CRISPR/Cas9 est utilisée pour réduire l’immunogénicité du blé. L’édition génomique a permis de supprimer les gènes centraux de la gliadine et les épitopes immunogènes sans modifier les propriétés de cuisson souhaitées. L’introduction sur le marché de blé génétiquement modifié n’est actuellement pas envisageable en Europe en raison de la réglementation, alors que les États-Unis et le Canada sont plus ouverts à cette idée.
Considérations thérapeutiques chez les enfants
Aucune approche thérapeutique n’est à l’étude à ce jour chez les enfants, car ils répondent généralement très bien au GFD et développent rarement des formes réfractaires. Les données d’études menées chez les adultes pourraient, le cas échéant, être rapidement transposées aux enfants sans qu’il ne soit nécessaire de mener d’autres vastes études cliniques, dans la mesure où le médicament utilisé s’adresse à un mécanisme clairement défini et, en particulier, est sûr.
Perspectives
Le développement de nouveaux médicaments est dynamique: de nombreuses substances sont sur le point d’être utilisées dans le cadre d’une application clinique régulière. En tant qu’option orale, les inhibiteurs spécifiques de la tTG, en particulier, ont le potentiel d’améliorer de manière significative la qualité de vie des patient·es atteint·es de la maladie cœliaque et de combler des lacunes thérapeutiques importantes. La possibilité de rendre tolérables de faibles quantités de gluten est perçue comme un grand soulagement et est approuvée par les patient·es, les sociétés savantes ainsi que les organismes de réglementation. À long terme, on s’attend à ce que des traitements fondés sur des preuves viennent compléter le GFD sur le plan clinique et histologique.
Littérature:
1 Roos S et al.: Gastroenterol Nurs 2019; 42: 496-503 2 Schuppan D et al.: Dtsch Med Wochenschr 2025; 150: 273-9 3 Verdu EF, Schuppan D: Gastroenterology 2021; 161: 1395-1411 4 Discepolo V et al.: Gastroenterology 2024; 167: 90-103 5 Murrray JA et al.: Gastroenterology 2022; 163: 1510-21 6 König J et al.: Sci Rep 2017; 7: 1310 7 Pultz IS et al.: Gastroenterology 2021; 161: 81-93 8 Daveson AJM et al.: Lancet Gastroenterol Hepatol 2025; 10: 44-54 9 Lähdeaho ML et al.: Lancet Gastroenterol Hepatol 2019; 4: 948-59 10 Schumann M: Gastroenterology 2024; 166: S194 11 Study on the effects of amlitelimab for adults with non-responsive celiac disease. https://clinicaltrials.eu/trial/study-on-the-effects-of-amlitelimab-for-adults-with-non-responsive-celiac-disease/ ; dernier accès le 24.2.2026 12 Therrien A et al.: Dig Dis Sci 2021; 66: 1989-97 13 Hardy MY et al.: Clin Immunol 2014; 264: 11025 14 Schuppan D et al.: N Engl J Med 2021; 385: 35-45 15 Tye-Din JA et al.: Lancet Gastroenterol Hepatol 2023; 8: 446-57 16 Kelly CP et al.:Gastroenterology 2021; 161: 66-80 17 Murray JA et al.: Lancet Gastroenterol Hepatol 2023; 8: 735-47 18 Press releases Topas Therapeutics 6.5.2025: https://topas-therapeutics.com/topas-therapeutics-tpm502-achieves-gluten-specific-tolerance-induction-positive-safety-profile-in-phase-2a-trial-in-celiac-disease-patients /; dernier accès le 24.2.2026
Das könnte Sie auch interessieren:
Coûts liés au climat dans le secteur de la santé: une retombée significativement sous-estimée du réchauffement climatique
Le changement climatique a des conséquences sur notre santé, même si beaucoup ne surviennent qu’à long terme. La santé et les coûts en matière de santé ne sont pourtant que partiellement ...
L’ivresse des profondeurs est une cause fréquente d’accident de plongée
Les gaz respiratoires subissent des modifications physiques en fonction de la profondeur de l’eau, ce qui peut avoir des conséquences physiologiques et médicales pour les plongeur·ses. L ...
Maladies cardiaques à l’heure des voyages dans des destinations lointaines
Les voyages représentent pour le système cardiovasculaire un stress mesurable, mais souvent gérable. Les patient·es dont la maladie est stable peuvent généralement voyager en toute ...