Nouvelles options thérapeutiques pour quatre organes
Auteures:
Prof. Dre méd. Anja Lorch
Reni Milerski
Dre méd. Franca Lisy
Klinik für Medizinische Onkologie und Hämatologie, Universitätsspital Zürich, Zürich
Correspondance:
E-mail: anja.lorch@usz.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Les tumeurs urologiques font partie des tumeurs solides les plus fréquentes dans le monde. Leur traitement dépend du stade, de la classification du risque correspondante, des marqueurs biologiques moléculaires et des caractéristiques individuelles des patient·es. Outre les traitements conventionnels tels que la chirurgie, la radiothérapie, la chimiothérapie ou l’hormonothérapie, on recourt de plus en plus aux immunothérapies et aux traitements ciblés dans le cadre de concepts thérapeutiques multimodaux.
Grâce à l’utilisation de ces traitements ciblés et de concepts de médecine personnalisée, la survie des patient·es, même à un stade avancé, s’est nettement améliorée au cours des dernières années, tout en leur permettant de conserver une bonne qualité de vie. Cet article propose une présentation synthétique des traitements de référence actuels ainsi qu’une mise à jour des nouveaux développements à différents stades de la maladie pour les cancers de la vessie, du rein, de la prostate et des cellules germinales chez l’homme.
Cancer de la vessie infiltrant le muscle
On distingue les tumeurs de la vessie n’infiltrant pas le muscle (NMIBC) et celles infiltrant le muscle (MIBC). Environ 70% des premiers diagnostics concernent des tumeurs n’infiltrant pas le muscle, dont le pronostic est relativement favorable, malgré un taux élevé de récidive locale. Toutefois, environ 30% des patient·es développent une tumeur infiltrant le muscle au cours de l’évolution de la maladie. Dans ce groupe, environ un cinquième des tumeurs sont déjà localement avancées au moment du diagnostic et 10% des patient·es présentent déjà un cancer métastatique. Ici, le pronostic reste défavorable. La classification infiltrant/n’infiltrant pas le muscle se base sur une biopsie obtenue par résection transurétrale (TUR-B). À partir du stade T2, on parle de tumeur infiltrant le muscle (MIBC, ≥T2).
Cancer de la vessie infiltrant le muscle localisé (≥T2 N0/N1 M0)
La MIBC localisée fait l’objet d’un traitement multimodal. Le traitement de référence actuellement établi comprend une chimiothérapie néoadjuvante (NAC) à base de platine avant la résection chirurgicale obligatoire. En règle générale, quatre cycles de chimiothérapie à base de cisplatine (p. ex. cisplatine+gemcitabine) sont administrés. De nombreuses études et méta-analyses ont montré que la NAC avant une cystectomie radicale (RC) prolongeait de manière significative la survie sans maladie (DFS) et la survie globale (OS).
L’étude de phaseIII randomisée NIAGARA a récemment démontré que l’ajout périopératoire de l’inhibiteur de point de contrôle durvalumab (anticorps anti-PD-L1) à la NAC de référence (cisplatine/gemcitabine) permettait de prolonger significativement la survie sans progression (PFS) et la survie globale (OS), et d’obtenir un taux de rémission complète pathologique (pCR) de 37%. Cette étude présente une innovation importante dans la prise en charge de la MIBC localisée et définit un nouveau traitement de référence.1
Les données de l’étude de phaseII SAKK 06/19, sont attendues; celle-ci évalue un concept similaire, mais utilise l’atézolizumab au lieu du durvalumab comme inhibiteur de point de contrôle et instille en outre le BCG localement dans le cadre du traitement néoadjuvant. L’étude SAKK renonce de surcroît à l’administration adjuvante d’un inhibiteur de point de contrôle une fois la pCR atteinte.2
Le traitement trimodal (TUR-B+radiothérapie+chimiosensibilisation) peut constituer une très bonne option thérapeutique, en particulier chez les patient·es non éligibles au cisplatine ou refusant une cystectomie, sous certaines conditions locales. La gemcitabine est souvent utilisée comme radiosensibilisateur, avec une très bonne tolérance.3
Pour les patient·es sans NAC ou sans traitement périopératoire avec le statut pT3–4 et/ou N+ en postopératoire, une monothérapie adjuvante par un agent immuno-oncologique doit être envisagée chez les patient·es atteint·es d’un cancer de la vessie après une RC. Il existe deux médicaments, le nivolumab et le pembrolizumab, qui ont chacun démontré une PFS significativement prolongée et une tendance à une OS prolongée par rapport au placebo ou au suivi seul dans des études de phaseIII.4,5
MIBC localement avancée et métastatique
Première ligne
La tumeur de la vessie localement avancée et métastatique présente toujours un défi thérapeutique. Le pronostic reste généralement défavorable, malgré les progrès récents dans le traitement systémique. Depuis l’autorisation du traitement combiné par le conjugué anticorps-médicament (ADC) enfortumab vedotin (ciblant la nectine-4) en combinaison avec l’inhibiteur du point de contrôle PD-1 pembrolizumab (EV+P), le choix du traitement de première ligne s’oriente sur l’éligibilité par rapport à la non-éligibilité à cette combinaison.
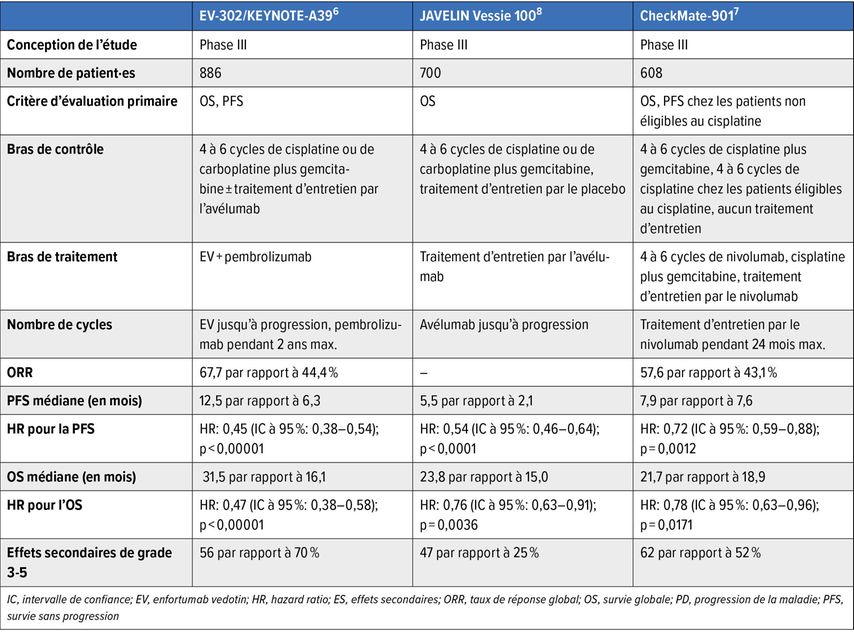
Ce traitement combiné a permis d’augmenter significativement l’OS médiane à près de 34 mois par rapport à 16 mois sous la chimiothérapie à base de platine ± immunothérapie d’entretien. L’étude comprenait également des patient·es ayant un mauvais état de santé (jusqu’à ECOG 2) et des patient·es atteint·es d’insuffisance rénale (DFG ≥30ml/min). Une mise à jour avec une durée de suivi de 2,5 ans montre que les patient·es qui obtiennent une rémission complète (CR) le restent de manière durable.6
En cas d’inéligibilité à l’EV+P, la combinaison cisplatine+gemcitabine+nivolumab, analogue à l’étude CheckMate-901, constitue une option pour les patient·es éligibles au cisplatine, avec également un avantage significatif en termes d’OS par rapport à la chimiothérapie seule. Pour les patient·es non éligibles au cisplatine, mais aptes à recevoir une chimiothérapie, il est possible d’utiliser la combinaison carboplatine+gemcitabine suivie d’un traitement d’entretien par l’avélumab, un inhibiteur du point de contrôle PD-1 (étude JAVELIN 100 Bladder).7
L’objectif fondamental de tout traitement est d’améliorer la qualité de vie tout en prolongeant la survie globale. Le régime thérapeutique doit donc être soigneusement choisi avec les patient·es en fonction des comorbidités, du profil d’effets secondaires des différents schémas thérapeutiques et de leurs souhaits.
Lignes suivantes
Selon le type de traitement préalable, différents schémas sont disponibles pour les lignes suivantes. Chez les patient·es présentant une aberration du FGFR3 («fibroblast growth factor receptor 3»), détectée chez 10 à 15%, l’inhibiteur sélectif du FGFR erdafitinib peut être utilisé.9 Pour les patient·es ayant connu un échec à une chimiothérapie à base de platine et à une immunothérapie d’entretien, l’EV est autorisé seul avec un bénéfice en termes de PFS et d’OS démontré dans une étude de phaseIII.10 Les traitements par un ADC anti-HER2 offrent de nouvelles approches thérapeutiques.8 Il est donc pertinent de réaliser un test correspondant.11
Carcinome rénal à cellules claires
Le carcinome rénal à cellules claires (ccRCC) est la forme histologique la plus fréquente de carcinome rénal, représentant environ 70 à 80%. L’apparition du ccRCC est souvent liée à des anomalies génétiques, notamment à l’inactivation du gène VHL (Von-Hippel-Lindau) sur le chromosome 3p, qui joue un rôle central dans la régulation de la réponse cellulaire au manque d’oxygène (hypoxie).
ccRCC localisé (stadeI–III de l’UICC)
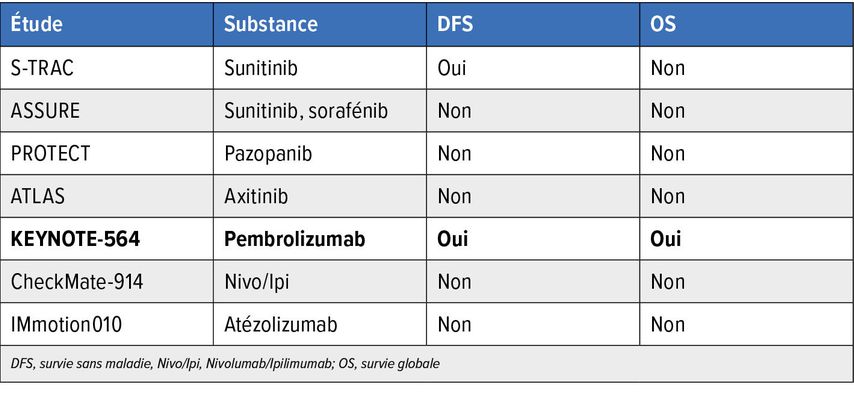
La résection chirurgicale de la tumeur est considérée comme le traitement de référence. Pour les patient·es présentant un risque élevé de récidive après l’opération, un traitement adjuvant par le pembrolizumab, un inhibiteur du point de contrôle PD-1, est autorisé pour une durée maximale de 17 cycles (=1 an): l’autorisation se base sur des prolongations significatives de la survie sans maladie avec une réduction du risque de récidive de 28% et de la survie globale avec un bénéfice de 5% à quatre ans, comme cela a pu être démontré par une grande étude de phaseIII randomisée. Cependant, près de deux patient·es sur dix ont présenté des effets secondaires de haut grade sous traitement adjuvant.12
Deux autres études portant sur les inhibiteurs de point de contrôle immunitaire (ICI) n’ont en revanche pas montré d’avantage significatif en termes de DFS et d’OS. La décision de recourir à un traitement adjuvant doit être prise individuellement, en tenant compte du risque de récidive, du profil d’effets secondaires et des souhaits des patient·es. Les patient·es présentant un contingent sarcomatoïde à l’histologie ainsi que ceux présentant une oligométastase initiale et un statut «no evidence of disease» (NED) après résection de la tumeur primitive et des oligométastases (jusqu’à 5 max.) devraient être encouragé·es à suivre un traitement adjuvant en l’absence de contre-indications, en raison du bénéfice important au sein des sous-groupes. La séquence thérapeutique ou l’efficacité d’un traitement par des ICI en cas de récidive après un traitement adjuvant par le pembrolizumab reste actuellement incertaine.
ccRCC métastatique (stade IV de l’UICC)
En cas de ccRCC métastatique, le traitement (combiné) médicamenteux constitue la référence. Il n’existe actuellement aucun biomarqueur validé pour orienter le traitement de première ligne du carcinome rénal métastatique. La procédure thérapeutique se base sur la charge tumorale, les symptômes cliniques, les comorbidités, les préférences des patient·es et la classification du risque de la tumeur selon le score IMDC (International Metastatic RCC Database Consortium) dans les groupes de risque «favorable», «intermediate» ou «poor».14
La néphrectomie cytoréductive n’est indiquée que dans certains cas, en particulier chez les patient·es à risque modéré ou élevé. Une évaluation interdisciplinaire est obligatoire.
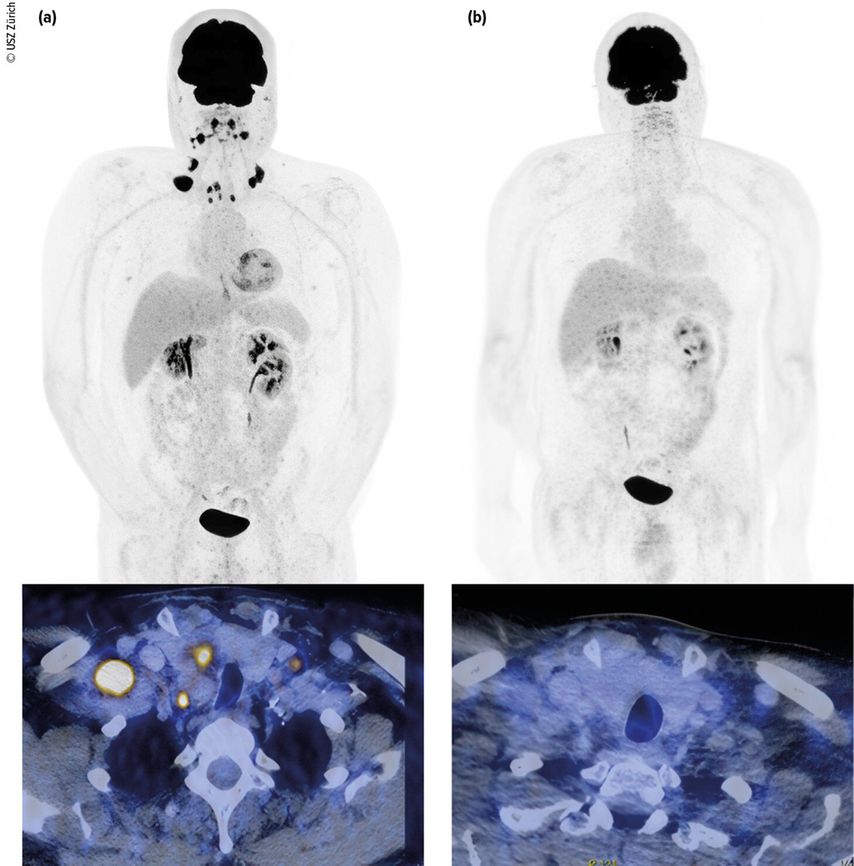
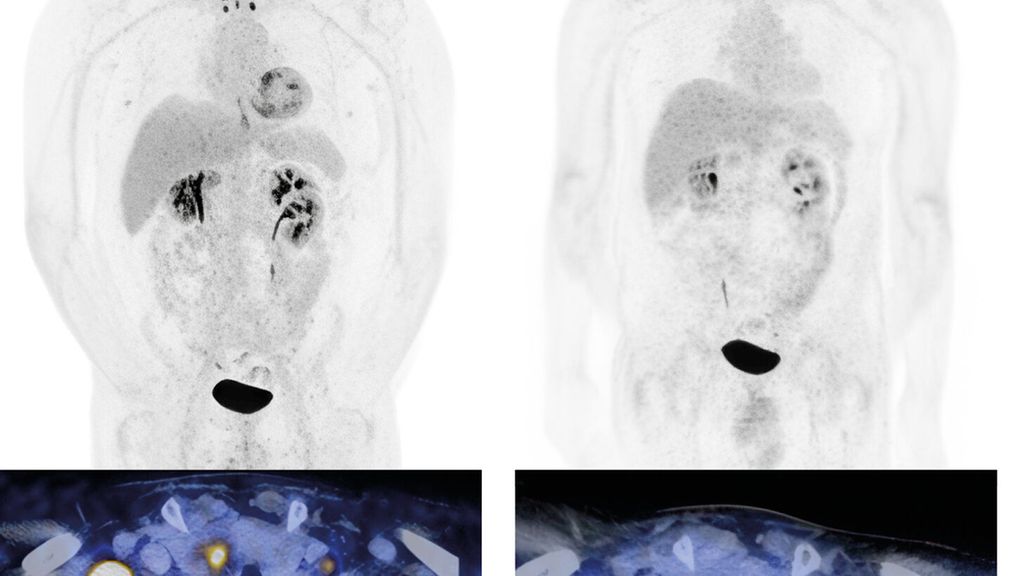
Fig.1: Carcinome urothélial de la vessie (initialement cT3 cN3 cM0) avec métastases lymphogènes métachrones. Classification par tomodensitométrie (TDM) avec diagnostic de métastases lymphogènes (a, à gauche). Première reclassification deux mois après le début du traitement par EV+P (b, à droite). L’image montre une rémission complète. Le patient est toujours en rémission durable. Images et patient de l’Hôpital universitaire de Zurich
Traitement de première intention
Outre les inhibiteurs de tyrosine kinase (TKI) classiques ciblant le VEGFR, tels que le sunitinib, le pazopanib, l’axitinib, le cabozantinib, le lenvatinib, ce sont surtout les ICI pembrolizumab et nivolumab qui sont actuellement utilisés.13
L’inhibiteur du CTLA-4 ipilimumab n’est autorisé en Suisse que pour le traitement des patient·es à risque modéré et élevé, en combinaison avec le nivolumab.15 Ce traitement combiné semble donner de meilleurs résultats à long terme par rapport aux combinaisons TKI/ICI. Les traitements combinés par axitinib/pembrolizumab, cabozantinib/nivolumab et lenvatinib/pembrolizumab sont également des schémas thérapeutiques établis; ils entraînent généralement une réponse rapide, en particulier chez les patient·es cliniquement symptomatiques et ceux·celles présentant une charge tumorale élevée, et sont privilégiés dans ces cas.16–18
Les combinaisons TKI/ICI ont été testées dans des études de phaseIII pour tous les groupes de risque selon le score IMDC. Une prolongation significative de la PFS et de l’OS a été constatée pour l’ensemble de la population, indépendamment de l’expression de PD-L1. Dans le groupe pronostique «favorable» selon le score IMDC, les données sont toutefois moins convaincantes, en particulier pour l’OS, de sorte que seules les monothérapies par TKI sont autorisées en Suisse pour ce groupe.
Une étude de phaseII portant sur une triple combinaison de nivolumab/ipilimumab et du TKI cabozantinib a certes été positive en termes de PFS, mais n’a montré aucun avantage significatif en termes d’OS, avec un taux d’effets secondaires nettement plus élevé; la combinaison n’est donc pas recommandée en première ligne.19
Traitement de deuxième ligne et lignes suivantes
Le choix de la séquence thérapeutique dépend en grande partie du traitement antérieur. En général, on utilise un TKI en monothérapie qui n’a pas été utilisé dans le traitement antérieur. Il est également possible d’utiliser la combinaison d’un TKI et d’un inhibiteur de mTOR (lenvatinib/évérolimus). Les patient·es ayant uniquement eu une monothérapie par TKI en première ligne doivent recevoir une immunothérapie (nivolumab) au plus tard en deuxième ligne.
Dans deux études publiées depuis, la réexposition à un ICI après l’échec du traitement de première ligne par une combinaison d’ICI n’a révélé aucun bénéfice en termes de PFS ou d’OS et ne doit donc pas être utilisée.13 L’inhibiteur de HIF-2α belzutifan s’est entre-temps établi comme nouvelle substance en monothérapie pour le rattrapage. Initialement autorisé en monothérapie pour les patient·es atteint·es de la maladie de Von Hippel-Lindau, il a montré une PFS prolongée et une bonne tolérance par rapport à l’évérolimus après un traitement préalable par un TKI ou un ICI en progression dans l’étude de phaseIII LITESPARK-005; il doit être proposé aux patient·es comme option.20
Cancer des cellules germinales métastatique chez l’homme
Le cancer des cellules germinales chez l’homme est une entité rare dans l’ensemble, mais c’est le plus fréquent chez les hommes jeunes. Un traitement adéquat et adapté au stade de la maladie est donc d’une grande importance. Les directives nationales et internationales donnent des recommandations thérapeutiques bien fondées sur des données. Outre l’utilisation appropriée de la chimiothérapie, de la chirurgie et de la radiothérapie, elles comprennent le choix des médicaments nécessaires ainsi que la durée de leur utilisation. Ces recommandations doivent être appliquées correctement à chaque cas clinique afin d’obtenir un succès thérapeutique maximal. Il faut éviter un surtraitement chez les patients ayant de bonnes chances de guérison, ainsi que des retards de traitement et des réductions de doses chez ceux dont la maladie est très avancée. Actuellement, le séminome métastatique de stade II en particulier fait l’objet d’un changement de paradigme.21
Séminome de stadesIIA et B
À partir d’un stadeII (mise en évidence de métastases dans les ganglions lymphatiques rétropéritonéaux), on parle de cancer métastatique. Il peut soit apparaître initialement, soit se développer dans 15 à 20% des cas à partir d’un résultat localisé (stade I).
Pendant longtemps, selon la taille des métastases ganglionnaires, le traitement de référence était soit une radiothérapie seule des ganglions lymphatiques para-aortiques ipsilatéraux (privilégiée au stadeIIA), soit une chimiothérapie comprenant trois cycles de cisplatine/étoposide/bléomycine (PEB) ou quatre cycles de cisplatine/étoposide (EP) (privilégiée au stadeIIB), avec un taux de survie à 5 ans de 99%. Dans le contexte d’une excellente survie à long terme, la réduction de la toxicité aiguë et à long terme chez ces patients, généralement très jeunes, est au premier plan.
Les résultats d’un total de trois études de phaseII sur la dissection des ganglions lymphatiques rétropéritonéaux (RPLND) primaire ont récemment été publiés. Avec 10 à 30%, les taux de récidive sont plus élevés que pour les méthodes susmentionnées, mais, à l’inverse, environ 70% des patients n’ont pas besoin de chimiothérapie, ce qui réduit la survenue de toxicités à long terme.21 Actuellement, la RPLND primaire ne constitue toutefois pas un traitement de référence en dehors des études. La sélection de patients appropriés pour un traitement éventuellement chirurgical, tout comme le choix de chirurgien·nes expérimenté·es, doit donc se faire exclusivement dans des centres spécialisés.
Une alternative actuellement mieux établie à la radiothérapie ou à la chimiothérapie seule est la radiochimiothérapie combinant l’administration d’un cycle de carboplatine avec une radiothérapie «involved node», comme dans l’étude SAKK 01/10. L’étude a montré un excellent taux de survie sans événement (EFS) de près de 94% à 3 ans dans l’ensemble de la population.22 Les résultats de l’étude de suivi SAKK 01/18 avec intensification de la chimiothérapie et administration d’un cycle d’EP au stadeIIB, ainsi que réduction de la dose de rayonnement aux stadesIIA et B sont attendus.23
En résumé, les patients au stadeII doivent obligatoirement être adressés à un centre spécialisé et le concept thérapeutique doit être défini conjointement. Il est également obligatoire de réévaluer un stadeII avéré avant le début du traitement si les résultats sont incertains.
Cancer de la prostate métastatique
Le cancer de la prostate est le cancer le plus fréquent chez l’homme et occupe la deuxième place des décès par cancer. On distingue le cancer de la prostate localisé et métastatique, ce dernier étant lui-même divisé en cancer hormonosensible et résistant à la castration. La prise en charge des formes métastatiques a considérablement évolué ces dernières années, notamment grâce aux nouveaux traitements systémiques qui ont permis de prolonger significativement la survie.
La base de tout traitement systémique reste la privation androgénique (ADT) médicamenteuse (ou, plus rarement, chirurgicale). Elle est complétée pour pratiquement tous les patients par un inhibiteur de la voie des récepteurs aux androgènes (ARPI).24
Cancer de la prostate hormonosensible métastatique
Des études publiées de haut niveau, telles que STAMPEDE, LATITUDE, TITAN, ENZAMET, ARCHES et, plus récemment, ARASENS, ont mis en évidence un avantage significatif de l’intensification du traitement par la combinaison d’une ADT et d’un ARPI, qui a permis de prolonger la survie sans progression radiographique (rPFS), la PFS et la survie globale (OS) par rapport à une monothérapie par ADT dans le cas d’un cancer de la prostate hormonosensible métastatique (mHSPC). Les médicaments utilisés à cet effet sont l’abiratérone/prednisone, l’enzalutamide, l’apalutamide et le darolutamide.
Le traitement systémique est complété par une radiothérapie locale de la prostate chez les patients présentant une faible charge tumorale. Une radiothérapie ciblée peut également être envisagée en cas d’oligométastases chez les patients présentant des métastases métachrones et une faible charge tumorale. Les patients présentant une charge tumorale élevée bénéficient également de l’ajout d’une chimiothérapie par le docétaxel.24,25
Lors du congrès de l’ASCO de cette année, des données ont été présentées pour la première fois sur les patients présentant des défauts dans les gènes de la recombinaison homologue (HRD) et recevant un inhibiteur de PARP en plus de l’ADT et de l’ARPI. L’étude AMPLITUDE a été positive sur le critère d’évaluation primaire rPFS. Les données relatives à l’OS sont attendues. Il convient d’effectuer un test génétique moléculaire le plus tôt possible chez tous les patients aptes à recevoir un traitement et présentant un cancer métastatique.
Tab.2: Études sur le traitement adjuvant en cas de ccRCC localisé à risque élevé de récidive (modifié selon les directives d’Onkopedia)13
Cancer de la prostate réfractaire à la castration métastatique
Plusieurs options sont disponibles pour les patients atteints d’un cancer de la prostate réfractaire à la castration métastatique (mCRPC). Après un traitement par un ARPI, il est préférable d’administrer une chimiothérapie à base de docétaxel. D’autres options thérapeutiques sont le cabazitaxel après un traitement préalable par le docétaxel, un traitement par le radioligand lutécium-177-PSMA ou radium-223, ou un inhibiteur de PARP.
Si les patients refusent la chimiothérapie ou ne sont pas assez en forme, le traitement par le lutécium-177-PSMA est privilégié à un changement d’ARPI en raison de la résistance croisée, bien que l’étude de phaseIII n’ait pas révélé de bénéfice significatif sur l’OS. En ce qui concerne l’utilisation d’un inhibiteur de PARP, son efficacité est indiscutable en présence d’une mutation BRCA1/2 et se révèle très bonne soit en monothérapie, soit en combinaison avec un ARPI, par exemple l’abiratérone ou l’enzalutamide, après une monothérapie par une ADT.
Entre-temps, les données de trois études ont été publiées. On ignore toujours si l’utilisation d’inhibiteurs de PARP en combinaison avec un ARPI est également justifiée chez les patients présentant des défauts dans d’autres gènes de la recombinaison homologue.25
Résumé
-
Au stade localisé du cancer de la vessie infiltrant le muscle, le traitement périopératoire analogue à celui de l’étude NIAGARA avec ajout de darolutamide à la chimiothérapie à base de cisplatine constitue la nouvelle référence.
-
Au stade métastatique du cancer de la vessie infiltrant le muscle, le traitement par l’enfortumab vedotin et le pembrolizumab s’est établi et montre également à long terme une prolongation significative de la survie globale par rapport à une chimiothérapie ± immunothérapie d’entretien.
-
Les données sur l’administration adjuvante de pembrolizumab révèlent un avantage significatif en termes de DFS et d’OS chez les patient·es atteint·es de ccRCC et présentant un risque élevé de récidive après résection au stade localisé.
-
L’administration de belzutifan présente un avantage significatif en termes de PFS dans le ccRCC métastatique chez les patient·es ayant reçu un traitement préalable, tout en étant bien tolérée.
-
Chez les patients atteints d’un séminome de stadeII, la radiochimiothérapie combinée a montré de très bons résultats en termes d’efficacité. Une dissection primaire peut également constituer une alternative pour les patients sélectionnés dans des centres spécialisés.
-
L’utilisation d’inhibiteurs de PARP dans le traitement des patient·es atteint·es d’un cancer métastatique est particulièrement efficace en présence d’une mutation BRCA1/2. Il convient donc d’effectuer un test génétique moléculaire le plus tôt possible chez tous les patient·es aptes à recevoir un traitement.
Littérature:
1 Powles TB et al.: Perioperative durvalumab with neoadjuvant chemotherapy in operable bladder cancer. NIAGARA Investigators. N Engl J Med 2024; 391(19): 1773-86 2 ClinicalTrials.gov: NCT04630730. Intravesical recombinant bcg followed by perioperative chemo-immunotherapy for patients with MIBC 3 Zlotta AR et al.: Radical cystectomy vs. trimodality therapy for muscle-invasive bladder cancer: a multi-institutional propensity score matched and weighted analysis. Lancet Oncol 2023; 24(6): 669-81 4Galsky MD et al.: Adjuvant nivolumab in high-risk muscle-invasive urothelial carcinoma: expanded efficacy from CheckMate 274. J Clin Oncol 2025; 43(1): 15-21 5Apolo A et al.: Adjuvant pembrolizumab vs. observation in muscle-invasive urothelial carcinoma. N Engl J Med 2025; 392(1): 45-55 6 Powles TB et al.: Enfortumab vedotin plus pembrolizumab in untreated locally advanced or metastatic urothelial carcinoma: 2.5-year median follow-up of the phaseIII EV-302/KEYNOTE-A39 trial. Ann Oncol 2025; S0923-7534(25)00762-8 7 Van der Heijden MS et al.: Nivolumab plus gemcitabin-cisplatin in advanced urothelial carcinoma. N Engl J Med 2023; 389(19): 1778-89 8Powles TB et al.: Avelumab first-line maintenance for advanced urothelial carcinoma: results from the JAVELIN Bladder 100 trial after >/=2 years of follow-up. JClin Oncol 2023; 41(19): 3486-92 9 Loriot Y et al.: Phase 3 THOR study: results of erdafitinib (erda) vs. chemotherapy (chemo) in patients (pts) with advanced or metastatic urothelial cancer (mUC) with select fibroblast growth factor receptor alterations (FGFRalt). J Clin Oncol 2023; 41(Suppl.17): Abstr. #LBA4619 10 Powles TB et al.: Enfortumab vedotin in previously treated advanced urothelial carcinoma. N Engl J Med 2021; 384(12): 1125-35 11Meric-Bernstam F et al.: Efficacy and safety of trastuzumab deruxtecan in patients with HER2-expressing solid tumors: primary results from the DESTINY-PanTumor02 phaseII trial. J Clin Oncol 2024; 42(1): 47-58 12 Choueiri TK et al.: Overall survival with adjuvant pembrolizumab in renal-cell carcinoma. N Engl J Med 2024; 390(15): 1359-71 13 Onkopedia Leitlinien: Nierenzellkarzinom (Hypernephrom) 2024 14 Heng D et al.: External validation and comparison with other models of the International Metastatic Renal-Cell Carcinoma Database Consortium prognostic model: a population-based study. Lancet Oncol 2013; 14: 141-8 15 Motzer RJ et al.: Nivolumab plus ipilimumab vs. sunitinib in advanced renal-cell carcinoma. NEngl J Med 2018; 378(14): 1277-90 16 Rini B et al.: Pembrolizumab plus axitinib vs. sunitinib for advanced renal-cell carcinoma. KEYNOTE-426 investigators. N Engl J Med 2019; 380(12): 1116-27 17 Motzer R et al.: Nivolumab plus cabozantinib vs. sunitinib in first-line treatment for advanced renal cell carcinoma (CheckMate 9ER): long-term follow-up results from an open-label, randomised, phase 3 trial. Lancet Oncol 2022; 23(7): 888-98 18 Motzer R et al.: Lenvatinib plus pembrolizumab or everolimus for advanced renal cell carcinoma. CLEAR trial investigators. N Engl J Med 2021; 384(14): 1289-300 19 Choueiri T et al.: Cabozantinib plus nivolumab and ipilimumab in renal-cell carcinoma. COSMIC-313 investigators. N Engl J Med 2023; 388(19): 1767-78 20 Choueiri T et al.: Belzutifan vs. everolimus for advanced renal-cell carcinoma. LITESPARK-005 investigators. N Engl J Med 2024; 391(8): 710-21 21 Onkopedia Leitlinien: Keimzelltumoren des Mannes (Gonadale Keimzelltumoren) 22 Papachristofilou A et al.: Single-dose carboplatin followed by involved-node radiotherapy for stageIIA and stageIIB seminoma (SAKK 01/10): a single-arm, multicentre, phase2 trial. Lancet Oncol 2022; 23: 1441-50 23 ClinicalTrials.gov: NCT03937843. Reduced intensity radio-chemotherapy for stage iia/b seminoma 24 Gillessen S et al.: Management of patients with advanced prostate cancer. Report from the 2024 Advanced Prostate Cancer Consensus Conference (APCCC). Eur Urol 2025; 87(2): 157-216 25PEAU Guideline Prostate Cancer. Online unter https://uroweb.org/guideline/prostate-cancer/
Das könnte Sie auch interessieren:
Normes thérapeutiques: développements actuels
Les standards thérapeutiques du lymphome à cellules du manteau (MCL) sont actuellement en pleine évolution: récemment, des inhibiteurs de la tyrosine kinase de Bruton (BTKi) ont été ...
Des avancées modifiant la pratique et des signaux déterminants pour l’avenir
Le congrès SOHC 2025 a illustré de manière impressionnante la diversité des dynamiques actuelles du progrès thérapeutique en oncologie. Le programme de la session «Highlights of the Year ...
«Mind Body Medicine»: un programme en oncologie ambulatoire
La «Mind Body Medicine» (MBM), composante de l’oncologie intégrative, est un concept qui relie le corps et l’esprit et transmet des compétences d’auto-prise en charge. Dans le cadre du « ...