Des avancées modifiant la pratique et des signaux déterminants pour l’avenir
Compte-rendu: Dre Therese Schwender
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Le congrès SOHC 2025 a illustré de manière impressionnante la diversité des dynamiques actuelles du progrès thérapeutique en oncologie. Le programme de la session «Highlights of the Year» couvrait ainsi un large spectre, allant d’innovations immédiatement pertinentes – notamment dans les cancers du sein et du poumon – à des concepts qui doivent, pour l’heure, être compris principalement comme des orientations pour les stratégies thérapeutiques futures.
Un point central de la présentation du Dr méd. Khalil Zaman, Centre hospitalier universitaire vaudois (CHUV), Lausanne, consacrée au cancer du sein, portait sur l’évolution de la thérapie endocrinienne (TE) dans le cancer du sein avancé à récepteurs hormonaux positifs (HR+). Après une longue période sans innovations majeures, les dégradeurs sélectifs oraux du récepteur des œstrogènes (SERD) sont récemment passés au premier plan. Des substances telles que l’élacestrant, le camizestrant et l’imlunestrant ont montré, dans des études cliniques dont EMERALD, une efficacité comparable à celle des thérapies endocriniennes établies, mais surtout une activité nettement supérieure chez les patient·es porteur·euses de mutations ESR1.1
Le girédéstrant constitue un autre représentant récent des SERD oraux. Lors de l’ESMO 2025, les résultats de l’étude de phaseIII evERA BC ont été présentés. Cette étude comparait le girédéstrant associé à l’évérolimus à une TE standard plus évérolimus chez des patient·es en progression après TE et inhibiteur de CDK4/6 (55% présentant une mutation ESR1).2 La combinaison girédéstrant-évérolimus s’est révélée supérieure en termes de survie sans progression (PFS), tant dans le sous-groupe avec mutation ESR1 (hazard ratio [HR] 0,38; intervalle de confiance à 95% [IC] 0,27–0,54; p<0,0001) que dans la population en intention de traiter (HR 0,56; IC à 95% 0,44–0,71; p<0,0001). Le Dr K. Zaman a également mentionné un communiqué de presse récemment publié concernant le girédéstrant, rapportant des résultats positifs en termes de survie sans maladie (DFS) en situation adjuvante.3 Si ces données se confirmaient, cela équivaudrait, selon lui, à une véritable révolution, aucune avancée substantielle n’ayant été réalisée en TE adjuvante depuis près de 20 ans.
L’inhibition ciblée de la cascade de signalisation PI3K/AKT/mTOR joue également un rôle majeur. Dans ce contexte, les données de l’étude INAVO-120 ont été particulièrement discutées. Dans cette étude, la triple association de fulvestrant, palbociclib et inavolisib a montré un signal d’efficacité significatif chez les patient·es présentant des tumeurs mutées PIK3CA.4 Outre une prolongation de la PFS par rapport à fulvestrant-palbociclib-placebo, un avantage significatif en survie globale (OS) a également été observé (OS médiane 34,0 vs 27,0 mois; HR 0,67, p=0,02).
Données actualisées de monarchE etNATALEE
Les études monarchE et NATALEE ont évalué l’ajout d’un inhibiteur de CDK4/6 (abémaciclib ou ribociclib) à la TE en situation adjuvante. Des mises à jour récentes des deux études ont été présentées à l’ESMO, permettant une appréciation plus précise de l’efficacité à long terme.
Dans monarchE, après un suivi médian de 76,2 mois, l’association abémaciclib plus TE a montré une réduction significative du risque de décès par rapport à la TE seule (HR: 0,84; 95%; IC: 0,72–0,98; p=0,027).5 Le taux d’OS à 7 ans était de 86,8% sous abémaciclib plus TE contre 85,0% sous TE seule, soit une différence absolue de 1,8%.
La mise à jour de l’étude NATALEE a montré que les patient·es sans atteinte ganglionnaire pouvaient également bénéficier d’un traitement adjuvant par ribociclib, avec une amélioration absolue de 5,7 points de pourcentage du taux de survie sans maladie invasive (iDFS) à cinq ans.6
Thérapie endocrinienne et qualité devie
Le Dr K. Zaman a ensuite présenté l’étude POSITIVE.7
Cette étude a évalué si une interruption de la TE pouvant aller jusqu’à deux ans – afin de permettre une grossesse – avait un impact négatif sur le pronostic. Les premiers résultats étaient rassurants et ont été confirmés par une mise à jour récente.8 Après cinq ans, aucune différence pertinente n’a été observée par rapport à la cohorte contrôle SOFT/TEXT, ni pour les événements spécifiques au cancer du sein ni pour les récidives à distance. L’incidence cumulée à 5 ans était de 12,3% versus 13,2% pour les événements spécifiques au cancer du sein, et de 6,2% versus 8,3% pour les récidives à distance.
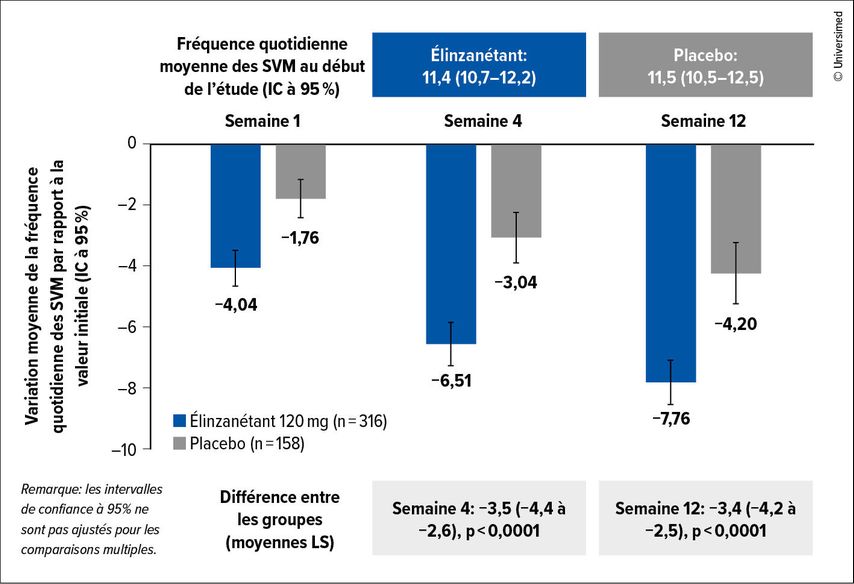
Par ailleurs, les résultats de l’étude OASIS-4 ont été présentés pour la première fois à l’ASCO.9 Ils ont montré que l’élinzanétant, nouvel inhibiteur dual de la neurokinine 1/3, réduisait significativement, par rapport au placebo, la fréquence des symptômes vasomoteurs modérés à sévères sous thérapie endocrinienne à 4 et 12 semaines (Fig.1). En outre, une amélioration numérique de la sévérité des symptômes a été observée à 4 et 12 semaines, ainsi qu’une augmentation significative de la qualité du sommeil et de la qualité de vie spécifique à la ménopause à 12 semaines.
Fig.1: Par rapport au placebo, l’élinzanétant a significativement réduit la fréquence des symptômes vasomoteurs modérés à sévères sous traitement endocrinien (modifiée selon Cardoso F et al.)9
SCLC: amélioration du pronostic grâce au traitement d’entretien
Les avancées thérapeutiques dans le carcinome pulmonaire à petites cellules (SCLC), particulièrement difficile à traiter, comptaient sans conteste parmi les temps forts dans le domaine des tumeurs pulmonaires. La Dre méd. Laetitia Mauti, Hôpital cantonal de Winterthur, a présenté dans ce contexte l’étude de phaseIII IMforte. Cette étude incluait des patient·es atteint·es d’un SCLC au stade étendu (ES-SCLC) et a montré qu’un traitement d’entretien par lurbinectédine et atézolizumab, comparé à l’atézolizumab seul après une induction standard par chimiothérapie à base de platine et atézolizumab, entraînait une prolongation significative de la PFS et de l’OS (gain médian d’OS de 2,6 mois).10
La Dre L. Mauti a toutefois souligné que le traitement d’entretien par lurbinectédine plus atézolizumab était associé à un taux nettement plus élevé d’effets indésirables, y compris d’événements sévères (effets indésirables liés au traitement de grade 3/4: 25,6% vs 5,8%). À ce jour, aucune donnée relative à la qualité de vie de ces patient·es n’est disponible, ce qu’elle considère comme un désavantage majeur. Il convient également de noter qu’après la fin du traitement d’induction, seuls environ deux tiers des patient·es initialement sélectionné·es ont pu être inclus·es dans le traitement d’entretien. Une sélection rigoureuse des patient·es éligibles à ce schéma thérapeutique est donc déterminante, selon Mauti.
DLL3 comme nouvelle cible thérapeutique dans le SCLC
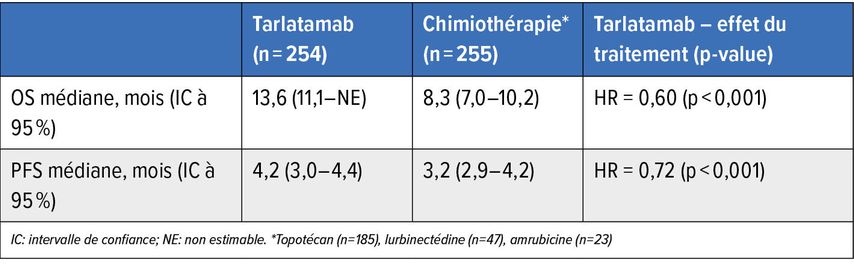
La Dre L. Mauti a qualifié l’utilisation d’engageurs bispécifiques des lymphocytes T contre DLL3 de «plus grand temps fort dans le SCLC». Avec le tarlatamab, un engageur bispécifique des lymphocytes T (BiTE) a pour la première fois obtenu des résultats cliniques convaincants dans une tumeur solide. Le tarlatamab relie DLL3 exprimé sur les cellules tumorales à CD3 sur les lymphocytes T cytotoxiques, déclenchant ainsi une réponse immunitaire ciblée. Dans l’étude randomisée de phaseIII DeLLphi-304, l’anticorps a démontré un net bénéfice en survie par rapport à la chimiothérapie standard chez des patient·es présentant majoritairement un ES-SCLC et une progression pendant ou après une chimiothérapie à base de platine (OS médiane: 13,6 vs 8,3 mois, HR 0,60; p<0,001) (Tab.1).11 Le bénéfice en survie a été observé de manière cohérente dans tous les sous-groupes analysés, y compris chez les patient·es présentant une maladie résistante au platine (près de 50% des participant·es). Le traitement a en outre entraîné une amélioration significative des symptômes associés à la tumeur, tels que la dyspnée, la toux ou les douleurs thoraciques.
Tab.1: Survie globale médiane (OS) et survie sans progression (PFS) sous traitement par tarlatamab, un engageur bispécifique des lymphocytes T, chez des patient·es atteint·es d’un carcinome pulmonaire à petites cellules au stade extensif avec progression pendant ou après une chimiothérapie à base de platine (étude DeLLphi-303) (modifié selon Wermke M et al.)12
Le profil d’effets indésirables spécifique aux BiTE comprend le syndrome de libération de cytokines (CRS), majoritairement de faible intensité sous tarlatamab et rarement responsable d’un arrêt du traitement. Une dysgueusie a également été fréquemment rapportée et peut, malgré une sévérité généralement modérée, être très invalidante pour les patient·es.
Les premiers résultats de l’étude de phaseIb DeLLphi-303 évaluant le tarlatamab en première ligne à une immunochimiothérapie dans l’ES-SCLC ont montré un taux d’OS à 12 mois jusqu’ici inégalé de 81,1%.12 La Dre L. Mauti s’est ainsi dite convaincue que les BiTE dirigés contre DLL3 intégreront rapidement des lignes de traitement plus précoces.
Lymphomes: des signaux forts avec une pertinence pratique encore limitée
Alors que plusieurs avancées immédiatement pertinentes pour la pratique ont été présentées dans le domaine du carcinome pulmonaire, ce sont surtout des développements prometteurs qui se sont dessinés dans le champ des lymphomes, dont l’interprétation définitive reste toutefois en partie en suspens. Comme l’a rapporté la Dre méd. Fatime Krasniqi, Hôpital universitaire de Bâle, les résultats de l’étude de phaseIII Skyglo sont particulièrement attendus, car ils pourraient s’avérer déterminants pour le traitement de première ligne des patient·es à haut risque atteint·es d’un lymphome diffus à grandes cellules B.
Des données déjà convaincantes sur le plan clinique ont été présentées dans la situation de récidive ou de maladie réfractaire: l’association d’un BiTE et d’un conjugué anticorps-médicament (mosunetuzumab et polatuzumab vedotin) s’est révélée nettement supérieure au rituximab, à la gemcitabine et à l’oxaliplatine (PFS médiane de 11,5 vs 3,8 mois; HR: 0,41; p<0,0001), ce qui souligne le potentiel thérapeutique pertinent de cette stratégie.13
Dans le lymphome à cellules du manteau à faible risque, les résultats de l’étude ENRICH ont également suscité l’attention: pour la première fois, un schéma sans chimiothérapie associant rituximab et ibrutinib a pu s’imposer face à l’immunochimiothérapie standard R-CHOP.14 Dans le lymphome folliculaire, le traitement de deuxième ligne par tafasitamab en association avec le rituximab et le lénalidomide (étude inMIND) a montré des améliorations cliniquement pertinentes susceptibles d’influencer la séquence thérapeutique future.15
Source:
Session «Highlights of the Year». Swiss Oncology & Hematology Congress, 21 novembre 2025, Bâle
Littérature:
1 Bidard FC et al.: J Clin Oncol 2022; 40(28): 3246-56 2 Mayer E et al.: ESMO 2025, Abstr. #LBA16 3 Genentech Press Release du 17 novembre 2025. Disponible sur: www.gene.com/media/press-releases/15090/2025-11-17/genentechs-giredestrant-becomes-the-firs , dernier accès le 19 janvier 2026 4 Jhaveri KL et al.: N Engl J Med 2025; 393(2): 151-61 5 Johnston S et al.: ESMO 2025, Abstr. #LBA13 6 Crown J et al.: ESMO Open 2025; 10: 105858 7 Partridge AH et al.: NEngl J Med 2023; 388(18): 1645-56 8 Pagani O et al.: ESMO 2025, Abstr. #LBA12 9 Cardoso F et al.: JClin Oncol 2025; 43: 508 10 Paz-Ares L et al.: Lancet 2025; 405(10495): 2129-43 11 Mountzios G et al.: NEngl J Med 2025; 393(4): 349-61 12 Wermke M et al.: Ann Oncol 2025; 36 (suppl_2): S1479-501 13 Westin J et al.: ICML 2025, Abstr. #LBA3 14 Lewis DJ et al.: Lancet 2025; 406(10514): 1953-68 15 Sehn LH et al.: ICML 2025, Abstr. #28
Das könnte Sie auch interessieren:
Nouvelles options thérapeutiques pour quatre organes
Les tumeurs urologiques font partie des tumeurs solides les plus fréquentes dans le monde. Leur traitement dépend du stade, de la classification du risque correspondante, des marqueurs ...
Normes thérapeutiques: développements actuels
Les standards thérapeutiques du lymphome à cellules du manteau (MCL) sont actuellement en pleine évolution: récemment, des inhibiteurs de la tyrosine kinase de Bruton (BTKi) ont été ...
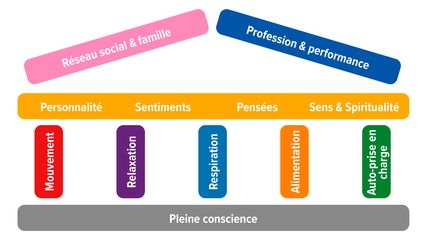
«Mind Body Medicine»: un programme en oncologie ambulatoire
La «Mind Body Medicine» (MBM), composante de l’oncologie intégrative, est un concept qui relie le corps et l’esprit et transmet des compétences d’auto-prise en charge. Dans le cadre du « ...