Normes thérapeutiques: développements actuels
Auteur·es:
Dr méd. Alexander Mang
Dre méd. Annegret Meyer-Hari
Dr méd. Martin Fehr
Klinik für Medizinische Onkologie und Hämatologie, Kantonsspital St. Gallen
Les auteur·es ont contribué à parts égales à cetravail.
Correspondance:
E-mail: martin.fehr@h-och.ch
Les standards thérapeutiques du lymphome à cellules du manteau (MCL) sont actuellement en pleine évolution: récemment, des inhibiteurs de la tyrosine kinase de Bruton (BTKi) ont été autorisés en association avec une immunochimiothérapie en première ligne.Dans ce contexte, l’utilisation de l’ibrutinib en combinaison avec une induction intensive et un traitement d’entretien adapté n’apporte pas de bénéfice supplémentaire par rapport à une chimiothérapie à haute dose suivie d’une autogreffe de cellules souches (ASCT), de sorte que celle-ci ne fait désormais plus partie du standard thérapeutique. L’aperçu ci-dessous met également en lumière d’autres évolutions prometteuses et potentiellement pertinentes pour la pratique dans le traitement des récidives. Pour un aperçu complet et une présentation détaillée, il convient également de se référer aux recommandations récemment publiées par le réseau EHA-EU-MCL.1
Traitement de première intention
L’algorithme thérapeutique établi jusqu’à présent pour les stades avancés prévoyait une stratification des patient·es selon leur éligibilité à la transplantation, largement fondée sur l’âge. Le traitement standard chez les patient·es plus jeunes, jusqu’à l’âge de 65 ans, comprenait une immunochimiothérapie d’induction à base de rituximab et de cytarabine, suivie d’une chimiothérapie à haute dose avec autogreffe de cellules souches (ASCT). Ce schéma était suivi d’un traitement d’entretien par rituximab pendant trois ans.2,3
TRIANGLE: combinaison avec l’ibrutinib
Ce concept est remis en question par les résultats de l’étude TRIANGLE.4
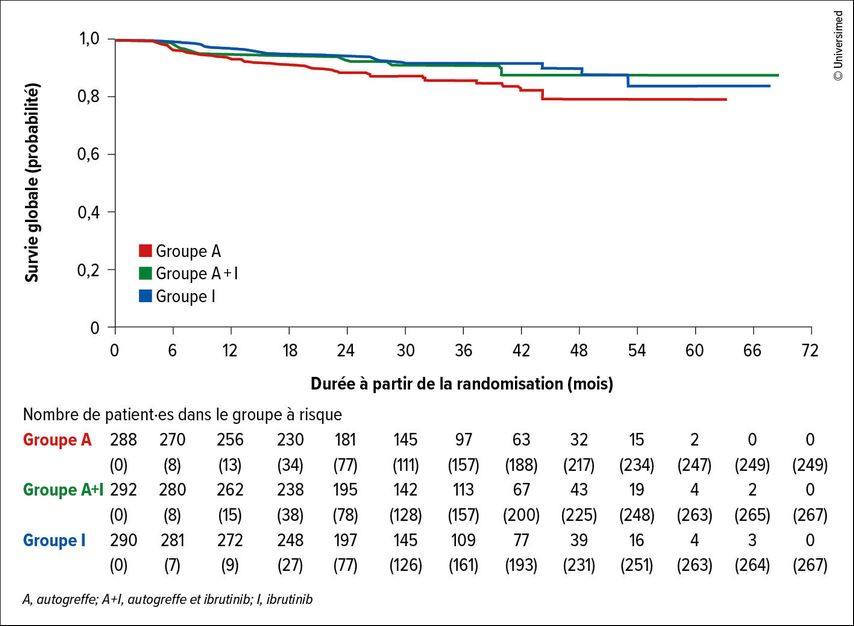
L’étude a randomisé les patient·es éligibles à la transplantation dans trois bras thérapeutiques: immunochimiothérapie d’induction suivie d’une autogreffe de cellules souches; immunochimiothérapie+ibrutinib suivie d’une ASCT et de deux ans de traitement d’entretien par ibrutinib; ou immunochimiothérapie+ibrutinib sans ASCT, suivie de deux ans d’entretien par ibrutinib. Au moment de la conception de l’étude TRIANGLE, le traitement d’entretien par rituximab ne constituait pas encore un standard; il ne faisait donc pas partie du protocole et a été administré, selon les pratiques nationales, à la majorité des patient·es dans les trois bras, avec une fréquence comparable. Dans les deux bras de traitement contenant de l’ibrutinib, une amélioration statistiquement significative et cliniquement pertinente de la survie sans échec (FFS) et de la survie globale (OS) a été observée par rapport à l’immunochimiothérapie standard suivie d’une ASCT: le taux de FFS à 3 ans était de 88% et 86%, respectivement, contre 72%, et le taux de survie globale à 3 ans de 91% et 92%, respectivement, contre 86% (Fig.1).4
Aucune supériorité n’a pu être démontrée pour l’ancien standard comprenant l’ASCT (sans ibrutinib) par rapport au bras ibrutinib sans ASCT.4
Ces résultats ont conduit à considérer l’ajout de l’ibrutinib à l’immunochimiothérapie d’induction, suivi d’un entretien par ibrutinib et rituximab, comme le nouveau standard chez les patient·es plus jeunes atteint·es de MCL (avec autorisation correspondante de l’ibrutinib en première ligne dans l’UE). Une chimiothérapie à haute dose avec ASCT ne fait donc plus partie du traitement standard chez les patient·es recevant l’ibrutinib en induction et en entretien.
Les études ECHO et SHINE
Chez les patient·es plus âgé·es ne pouvant pas bénéficier d’une chimiothérapie d’induction intensive (anciennement «non transplantables»), deux études prospectives de phaseIII, randomisées et contrôlées par placebo – ECHO et SHINE – ont évalué l’association d’inhibiteurs de BTK avec le schéma de première ligne établi rituximab/bendamustine (R/B) ainsi qu’un entretien par rituximab.5,6
ECHO: R/B+acalabrutinib
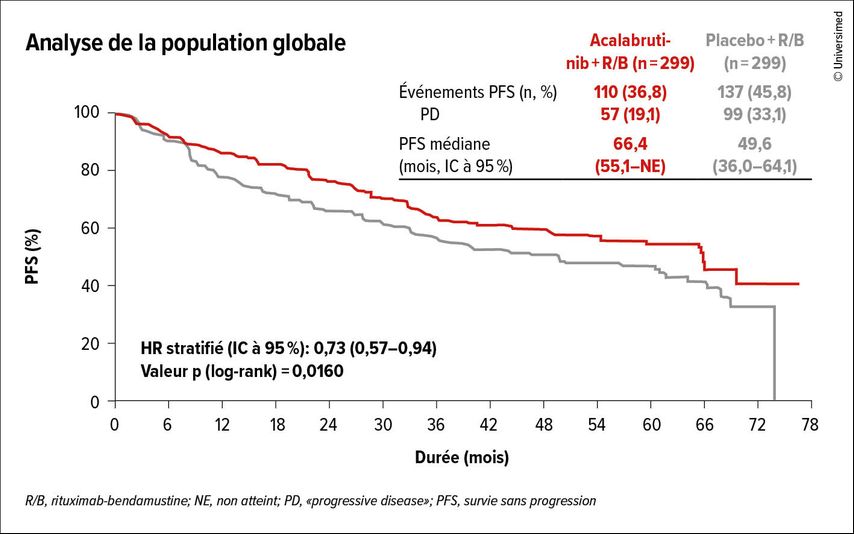
Dans l’étude ECHO, l’ajout d’acalabrutinib a entraîné une amélioration significative de la survie sans progression (PFS) par rapport au bras contrôle (R/B+placebo), avec un HR de 0,73 (IC à 95%: 0,57–0,94) (Fig.2). Ce bénéfice était également observé dans des sous-groupes à haut risque (p.ex. masse tumorale volumineuse, Ki-67 ≥30%, morphologie blastoïde). Sur la base des résultats de l’étude ECHO, l’acalabrutinib a été autorisé par l’EMA et Swissmedic en association avec l’induction R/B et l’entretien par rituximab.
Fig.2: Dans l’étude ECHO, l’ajout de l’acalabrutinib a entraîné une prolongation significative de la survie sans progression par rapport au bras contrôle (modifiée selon Wang M et al.)5
SHINE: R/B+ibrutinib
L’étude SHINE, de conception similaire, a évalué l’ajout de l’ibrutinib au schéma R/B et a également atteint son critère d’évaluation primaire, avec une prolongation significative de la PFS.6
Il convient toutefois de noter que l’ibrutinib en association avec R/B ne dispose pas d’autorisation; de manière générale, chez les patient·es âgé·es atteint·es de MCL, l’utilisation d’une trithérapie incluant un inhibiteur de BTK doit être envisagée en tenant compte de la situation clinique globale, du bénéfice potentiel, des objectifs thérapeutiques individuels et des risques de toxicité.
ENRICH: première ligne sans chimiothérapie
Plusieurs études sont actuellement en cours afin d’établir des options de première ligne sans chimiothérapie, en particulier chez les patient·es âgé·es. Des résultats de l’étude ENRICH sont déjà disponibles. Dans cette étude, des patient·es ≥60 ans présentant un MCL non traité (stadeII–IV) ont été randomisé·es dans deux bras: ibrutinib+rituximab suivi d’ibrutinib jusqu’à progression ou toxicité inacceptable, vs rituximab+chimiothérapie (R/B ou R-CHOP). Dans les deux bras, les patient·es ont reçu un entretien par rituximab (12 cycles, intervalle de 8 semaines).
L’association ibrutinib+rituximab a montré une PFS globalement significativement plus longue que l’association rituximab+chimiothérapie, avec une hématotoxicité moindre.7
Toutefois, selon l’analyse de sous-groupe, la PFS ne différait pas significativement entre les patient·es traité·es par rituximab/ibrutinib et celles et ceux traité·es par rituximab/bendamustine. Par ailleurs, les données de l’étude ENRICH ne sont que partiellement extrapolables aux patient·es présentant des caractéristiques à haut risque (score MIPI élevé, morphologie blastoïde, mutation TP53 ou surexpression de p53).
Thérapie en cas de récidive
De manière générale, dans toutes les situations de récidive, il convient d’évaluer les facteurs liés au·à la patient·e, à la maladie et aux traitements antérieurs (p.ex. comorbidités, état général; indice de prolifération, aberration TP53, histologie blastoïde; réponse et toxicité des traitements antérieurs) et, sur cette base, de discuter du choix thérapeutique et des objectifs individuels.1
Dans le traitement de la première récidive de MCL, il est en outre essentiel de distinguer les patient·es naïf·ves de BTKi de celles et ceux déjà exposé·es à un inhibiteur de BTK.1
Récidive après immunochimiothérapie
Chez les patient·es naïf·ves de BTKi, l’ibrutinib et l’acalabrutinib sont autorisés en monothérapie; le traitement est généralement poursuivi jusqu’à progression de la maladie ou survenue d’une toxicité inacceptable. Dans une comparaison rétrospective avec des immunochimiothérapies, des avantages en termes de tolérance ont été démontrés, ainsi qu’une PFS plus longue sous ibrutinib chez les patient·es présentant une récidive précoce après immunochimiothérapie (<2 ans).8
Il n’existe pas de données comparatives directes entre l’ibrutinib et l’acalabrutinib chez les patient·es atteint·es de MCL récidivant/réfractaire; en revanche, chez les patient·es atteint·es de leucémie lymphoïde chronique (LLC), une comparaison prospective randomisée a montré un profil d’effets indésirables plus favorable pour l’acalabrutinib.9,10
La réponse aux BTKi covalents (cBTKi) est hétérogène: alors que chez les patient·es obtenant une rémission complète (RC), celle-ci peut souvent se maintenir sur une longue durée, environ un tiers des patient·es ne répondent pas au traitement.1
Le risque de progression précoce sous cBTKi peut être estimé à l’aide du score «2nd line BTKi-MIPI», qui intègre, en plus des facteurs MIPI connus, l’indice de prolifération Ki-67 et la durée sans récidive.11
Chez les patient·es présentant un risque élevé de progression précoce et éligibles à un traitement ultérieur par cellules CAR-T, une surveillance étroite est recommandée ainsi que, le cas échéant, une prise de contact précoce avec un centre spécialisé en thérapie CAR-T.12
SYMPATICO: ibrutinib+vénétoclax
Plusieurs approches visent actuellement à améliorer l’efficacité du traitement des récidives à base de BTKi par des stratégies de combinaison. L’étude de phaseIII randomisée en double aveugle SYMPATICO a comparé l’association ibrutinib+vénétoclax à ibrutinib+placebo.13
Les patient·es du bras expérimental ont reçu de l’ibrutinib jusqu’à progression et du vénétoclax pendant les 24 premiers mois.
La thérapie combinée s’est révélée supérieure à la monothérapie par ibrutinib en termes de survie sans progression et de taux de réponse, au prix toutefois d’une toxicité accrue. Fait notable, les patient·es présentant une mutation TP53, caractéristique de haut risque, ont également bénéficié de cette combinaison.13
SAKK 36/13: ibrutinib+bortézomib
L’étude de phaseI/II SAKK 36/13, menée dans plusieurs centres en Suisse ainsi que dans certains centres allemands et italiens, a évalué l’association de l’ibrutinib avec le bortézomib, un inhibiteur du protéasome.14
Un taux de réponse global de 87% a été obtenu, 75% des patient·es présentant une ou plusieurs caractéristiques à haut risque (taux de prolifération élevé, aberration TP53, histologie blastoïde/pléomorphe).14
Récidive après exposition aux cBTKi ou progression sous cBTKi
En cas de progression sous traitement cBTKi, les possibilités étaient jusqu’à récemment limitées et la survie sous traitements conventionnels souvent courte (médiane de huit mois). De nouvelles options thérapeutiques laissent entrevoir des améliorations dans cette situation particulièrement difficile.
Brexucabtagen autoleucel
Dans une étude de phaseII, la thérapie par cellules T CAR anti-CD19 brexucabtagen autoleucel a permis d’obtenir un taux de réponse de 91% et une survie globale médiane d’environ 47 mois.15
BRUIN: pirtobrutinib
Le pirtobrutinib, un inhibiteur non covalent de BTK (ncBTKi), constitue une autre option thérapeutique.16
Dans la cohorte MCL de l’étude de phaseII BRUIN, 49% des patient·es en progression après un traitement préalable par cBTKi ont présenté une réponse, avec une bonne tolérance globale. Le pirtobrutinib peut ainsi être utilisé chez les patient·es pour lesquel·les une thérapie par cellules CAR-T n’est pas indiquée ou n’est pas immédiatement réalisable.
Des données en vie réelle issues du registre EMCL montrent que le pirtobrutinib est utilisé dans environ 50% des cas comme traitement relais jusqu’à la thérapie par cellules CAR-T.17
Le brexucabtagen autoleucel et le pirtobrutinib disposent tous deux d’autorisations dans l’UE et en Suisse, bien que celles-ci diffèrent dans leurs modalités précises.
Anticorps CD3xCD20
Comme dans d’autres entités lymphomateuses, le développement des anticorps bispécifiques CD3xCD20 se poursuit également dans le MCL, avec des résultats prometteurs en termes d’activité clinique; toutefois, selon les connaissances actuelles, une attention particulière doit être portée à la prévention et à la prise en charge du syndrome de libération des cytokines (CRS), relativement fréquent et parfois sévère, lors de leur utilisation dans le MCL.18
Littérature:
1 Jerkeman M et al.: EHA–EU MCL network guidelines for diagnosis and treatment of mantle cell lymphoma. Hemasphere 2025; 9(10): e70233 2 Wilson MR et al.: How I manage mantle cell lymphoma: indolent vs. aggressive disease. Br J Haematol 2023; 201(2): 185-98 3 Hermine O et al.: High-dose cytarabine and autologous stem-cell transplantation in mantle cell lymphoma: long-term follow-up of the randomized Mantle Cell Lymphoma Younger Trial of the European Mantle Cell Lymphoma Network. JClin Oncol 2023; 41(3): 479-84 4 Dreyling M et al.: Ibrutinib combined with immunochemotherapy with or without autologous stem-cell transplantation vs. immunochemotherapy and autologous stem-cell transplantation in previously untreated patients with mantle cell lymphoma (TRIANGLE): a three-arm, randomised, open-label, phase 3 superiority trial of the European Mantle Cell Lymphoma Network. Lancet 2024; 403(10441): 2293-306 5 Wang M et al.: Acalabrutinib plus bendamustine and rituximab in untreated mantle cell lymphoma: results from the phase 3, double-blind,placebo-controlled ECHO trial. EHA24 2024; Abstr. #LB3439 6 Wang ML et al.: Ibrutinib plus bendamustine and rituximab in untreated mantle-cell lymphoma. N Engl J Med 2022; 386(25): 2482-94 7 Lewis N et al.: ENRICH: ibrutinib plus rituximab vs chemoimmunotherapy in elderly patients with mantle cell lymphoma. ICML 2025 8 Viso C et al.: Outcomes in first relapsed-refractory younger patients with mantle cell lymphoma: results from the MANTLE-FIRST study. Leukemia 2021; 35(3): 787-95 9 Byrd JC et al.: Acalabrutinib vs. ibrutinib in previously treated chronic lymphocytic leukemia: results of the first randomized phase iii trial. J Clin Oncol 2021; 39(31): 3441-52 10 Seymour JF et al.: Detailed safety profile of acalabrutinib vs ibrutinib in previously treated chronic lymphocytic leukemia in the ELEVATE-RR trial. Blood 2023; 142(8): 687-99 11 Villa D et al.: Time to progression of disease and outcomes with second-line BTK inhibitors in relapsed/refractory mantle cell lymphoma. Blood Adv 2023; 7(16): 4576-85 12 Eyre TA et al.: Diagnosis and management of mantle cell lymphoma: A British Society for Haematology Guideline. Br J Haematol 2024 13 Wang M et al.: Ibrutinib plus venetoclax in relapsed or refractory mantle cell lymphoma (SYMPATICO): a multicentre, randomised, double-blind, placebo-controlled, phase 3 study. Lancet Oncol 2025; 26(2): 200-13 14 Novak U et al.: Combined therapy with ibrutinib and bortezomib followed by ibrutinib maintenance in relapsed or refractory mantle cell lymphoma and high-risk features: a phase 1/2 trial of the European MCL network (SAKK 36/13). EClinicalMedicine 2023; 64: 102221 15 Wang M et al.: Three-year follow-up of KTE-X19 in patients with relapsed/refractory mantle cell lymphoma, including high-risk subgroups, in the ZUMA-2 study. J Clin Oncol 2023; 41(3): 555-67 16 Wang ML et al.: Pirtobrutinib in covalent bruton tyrosine kinase inhibitor pretreated mantle-cell lymphoma. JClin Oncol 2023; 41(24): 3988-97 17 Aydilek E et al.: ICML 2025; Poster #273 18 Phillips TJ et al.: Glofitamab in relapsed/refractory mantle cell lymphoma: results from a phase I/II study. J Clin Oncol 2025; 43(3): 318-28
Das könnte Sie auch interessieren:
Nouvelles options thérapeutiques pour quatre organes
Les tumeurs urologiques font partie des tumeurs solides les plus fréquentes dans le monde. Leur traitement dépend du stade, de la classification du risque correspondante, des marqueurs ...
Des avancées modifiant la pratique et des signaux déterminants pour l’avenir
Le congrès SOHC 2025 a illustré de manière impressionnante la diversité des dynamiques actuelles du progrès thérapeutique en oncologie. Le programme de la session «Highlights of the Year ...
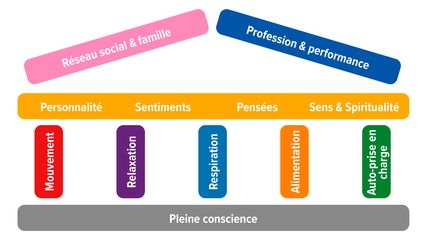
«Mind Body Medicine»: un programme en oncologie ambulatoire
La «Mind Body Medicine» (MBM), composante de l’oncologie intégrative, est un concept qui relie le corps et l’esprit et transmet des compétences d’auto-prise en charge. Dans le cadre du « ...