Nebenniereninsuffizienz: Management in der Praxis
Autorinnen:
Dr. Elisabeth Nowak
Dr. Hanna Nowotny
Prof. Dr. Nicole Reisch
Medizinische Klinik und Poliklinik IV
LMU Klinikum, München
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Aufgrund der Gefahr lebensbedrohlicher Nebennierenkrisen erfordern die Diagnostik und Therapie von Patient:innen mit Nebenniereninsuffizienz ein schnelles und zielgerichtetes Vorgehen. Fachspezifische Maßnahmen erfordern das Erkennen von Symptomen, die notwendige Diagnostik und ein effektives Management der Notfallsituation.
Keypoints
-
Eine Nebenniereninsuffizienz tritt häufig auf – das rechtzeitige Erkennen und die rechtzeitige Behandlung können Leben retten.
-
Bei v.a. eine Nebennierenkrise sollte immer eine umgehende Substitution mit Hydrocortison erfolgen. Es gilt: erst handeln, dann denken!
-
Betroffene sollten regelmäßige Schulungen erhalten und stets einen Notfallausweis und -medikamente mit sich führen.
Abhängig von ihrer Ätiologie lässt sich die Nebenniereninsuffizienz in eine primäre, sekundäre und tertiäre Form unterteilen. Bei einer primären Nebenniereninsuffizienz handelt es sich um eine Störung auf Ebene der Nebenniere selbst. Mit einer Inzidenz von 10–22 Fällen pro 100000 Personen1–5 umfasst sie eine Reihe seltener Erkrankungen verschiedener Genese. Die häufigste genetische Ursache ist das adrenogenitale Syndrom (AGS). Es bezeichnet eine Gruppe autosomal-rezessiv vererbter Stoffwechselerkrankungen, bei denen eine gestörte Steroidbiosynthese vorliegt. In ca. 95% beruht das AGS auf einer Mutation im CYP21A2-Gen, das das Enzym 21-Hydroxylase codiert, das an der Cortisol- und Aldosteronsynthese beteiligt ist.6 Die häufigste Ursache der erworbenen primären Nebennierenrindeninsuffizienz ist mit 80–90% in Europa und Nordamerika eine Autoimmunadrenalitis (Morbus Addison).7 Weltweit gehören Infektionen und hierbei insbesondere die Tuberkulose zu den Hauptursachen.8,9 Darüber hinaus kann eine primäre Nebenniereninsuffizienz auch medikamentös (z.B. durch CYP3A4-Inhibitoren, Steroidsyntheseinhibitoren, Immuncheckpoint-Inhibitoren) sowie durch Blutungen oder Metastasen hervorgerufen werden.10 Eine sekundäre Nebenniereninsuffizienz entsteht durch Störungen auf Ebene der Hypophyse. Dies umfasst Schädigungen des Hypophysenvorderlappens, die entweder zu einer unzureichenden Produktion von adrenokortikotropem Hormon (ACTH) allein oder auch zu einem Mangel an anderen Hypophysenhormonen führen können. Mit 14–28 Fällen pro 100000 Personen (Daten aus dem Vereinigten Königreich und Spanien) zählt sie ebenfalls zu den seltenen Erkrankungen.11,12 Ursachen für erworbene sekundäre Nebenniereninsuffizienzen umfassen beispielsweise Tumoren (z.B. Kraniopharyngeome, Meningeome, Metastasen), Traumata (z.B. nach einem Verkehrsunfall bzw. ein Schütteltrauma bei Kindern), die Einnahme von Opioiden und Schlaganfälle (z.B. Sheehan-Syndrom).10 Den angeborenen Formen liegt eine Reihe von seltenen genetischen Defekten zugrunde, die an der ACTH-Synthese beteiligt sind.
Die tertiäre Nebenniereninsuffizienz resultiert größtenteils aus der Behandlung mit exogenen Glukokortikoiden und/oder der unsachgemäßen Einnahme von Opiaten. Da die Verwendung von Glukokortikoiden weltweit weitverbreitet ist, wie zum Beispiel zur Behandlung chronisch-entzündlicher sowie rheumatischer und autoimmuner Erkrankungen, ist dies die häufigste Ursache einer Nebenniereninsuffizienz. Bereits ab einer Einnahme von 5mg Prednisolonäquivalent über einen Zeitraum von über vier Wochen kann – wenngleich selten – eine tertiäre Nebenniereninsuffizienz entstehen.13 Daher ist es besonders wichtig, vor allem bei einem plötzlichen Absetzen der Therapie eine entsprechende Diagnostik durchzuführen. Auch im Rahmen eines Glukokortikoidentzugssyndroms nach erfolgreicher Therapie eines endogenen Cushingsyndroms kommt es regelrecht zu einer tertiären Nebenniereninsuffizienz, die postoperativ eine entsprechende Substitution erfordert.
Klinische Zeichen einer Nebenniereninsuffizienz
Während die genetischen Ursachen einer Nebenniereninsuffizienz in der Regel bereits zu einem Symptombeginn im Neugeborenen und (Klein-)Kindesalter führen, treten die erworbenen Ursachen je nach Ätiologie eher im jungen (z.B. bei Autoimmunerkrankungen) oder im höheren Erwachsenenalter (z.B. bei Tumoren, Metastasen) auf. Die Intensität der klinischen Anzeichen richtet sich dabei meist nach der Ätiologie und Dauer der zugrunde liegenden Erkrankung, wobei die Symptome bei einer primären Nebenniereninsuffizienz in der Regel am stärksten ausgeprägt sind. Das markanteste Merkmal einer autoimmunen primären Nebenniereninsuffizienz ist die Hyperpigmentierung der Haut und Schleimhäute. Diese entsteht durch Stimulation der kutanen Melanokortinrezeptoren durch die erhöhten ACTH-Konzentrationen.10 Hingegen sind Patient:innen mit einer sekundären und tertiären Nebenniereninsuffizienz aufgrund des ACTH-Mangels und damit auch des Melanozyten-stimulierenden Hormonsmangels typischerweise auffallend blass. Insgesamt sind die Anzeichen einer Nebenniereninsuffizienz jedoch unspezifisch. Am häufigsten zeigt sich eine Erschöpfungssymptomatik.14 Weitere Symptome sind Hypotonie, Hypovolämie, Kopf- und Bauchschmerzen sowie Übelkeit und Erbrechen. Bei einer Nebennierenkrise sind diese Symptome stark ausgeprägt und können mit einer Schocksymptomatik einhergehen. Eine Nebennierenkrise ist lebensbedrohlich und das frühzeitige Erkennen und die Behandlung sind essenziell.
Nebenniereninsuffizienz erkennen und richtig behandeln
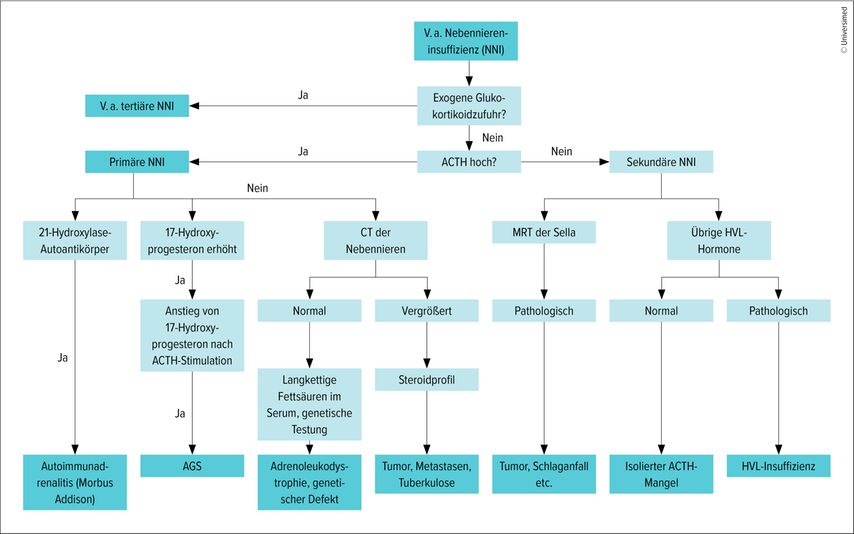
Im Rahmen der Anamnese sollten bei Verdacht auf Nebenniereninsuffizienz exogene Glukokortikoide sowie Opiate sorgfältig erfasst werden. Hierzu gehört auch die Anwendung topischer Applikationsformen wie beispielsweise Cortison-haltiger Nasen- und Asthmasprays sowie intraartikulärer Injektionen. Die laborchemische Basisdiagnostik umfasst die Bestimmung von Elektrolyten, Nierenfunktion, Blutbild und Entzündungswerten. Laborchemisch geht eine Nebenniereninsuffizienz in >80% der Fälle mit einer Hyponatriämie einher.15 Bei unklarer Hyponatriämie sollte daher differenzialdiagnostisch auch immer an eine Nebenniereninsuffizienz gedacht werden. Zusätzlich sollte eine basale (nüchtern morgens) Bestimmung von Cortisol und ACTH im Serum erfolgen und ein ACTH-Stimulationstest durchgeführt werden. Nach der basalen Blutentnahme wird hierbei 250µg ACTH (Synacthen®) i.v. verabreicht und Cortisol nach 30 und 60 Minuten bestimmt. Die genauen Referenzwerte des Tests hängen dabei von dem verwendeten Assay sowie der Einheit ab. Generell wird eine Cortisolkonzentration von mindestens 500nmol/l (entspricht 18µg/dl) für Immunoassays und mindestens 412nmol/l (entspricht15µg/dl nach 30 Minuten) bzw. 485nmol/l (entspricht 17,6µg/dl, nach 60 Minuten) für massenspektrometrisch Messungen („liquid chromatography-mass spectrometry“; LCMS)empfohlen.16 Sobald eine Nebenniereninsuffizienz nachgewiesen wurde, muss eine Ursachensuche ergänzt und differenzialdiagnostisch abgewogen werden (Abb.1). Zudem müssen Betroffene im Umgang mit der täglichen Substitution geschult sowie auch insbesondere im Vorgehen bei Notfallsituationen angeleitet werden.
Abb. 1: Differenzialdiagnostisches Vorgehen bei Verdacht auf Nebenniereninsuffizienz im Erwachsenenalter (modifiziert nach Husebye et al. 2021)10
Substitutionstherapie bei Nebenniereninsuffizienz im Alltag
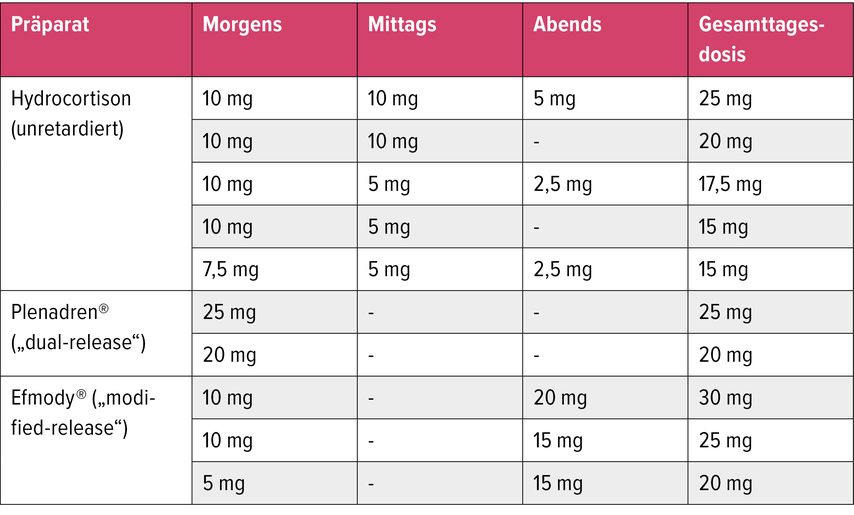
Gesunde Nebennieren sezernieren ca. 5–10mg Cortisol/m2 Körperoberfläche pro Tag.17 Die Freisetzung unterliegt hierbei einer ultradianen und zirkadianen Rhythmik, wobei das Maximum in den frühen Morgenstunden und das Minimum gegen Mitternacht erreicht wird. Für Erwachsene entspricht dies einer typischen Substitutionsdosis von 15–25mg Hydrocortison/Tag. Hierbei sollte auf eine zeitversetzte Einnahme von 2–3 Einzeldosen geachtet werden, wobei die größte Dosis morgens und die kleinste ca. 4–6 Stunden vor dem Schlafengehen eingenommen werden sollte, um Schlafstörungen zu vermeiden (Tab.1).10 Kinder und Jugendliche unter 18Jahren sollten täglich 8–10mg Hydrocortison/m2 aufgeteilt in 3–4 Gaben erhalten, wovon 50–66% als morgendliche Dosis eingenommen werden sollten.10 Als Alternative zum konventionellen Hydrocortison oder auch zu den seltener eingesetzten synthetischen länger wirksamen Glukokortikoiden, wie Prednisolon und Dexamethason, können sogenannte duale oder „Modifie release“-Präparate angewendet werden.18 Ein typisches Beispiel ist das Medikament Plenadren® mit einer zweiphasigen Wirkstofffreisetzung von Hydrocortison. Die äußere Schicht führt zu einer sofortigen Wirkstofffreisetzung, während der innere Kern verzögert freigesetzt wird. Gegenüber dem Standardsubstitutionsschema mit Hydrocortison birgt Plenadren® den Vorteil der einmaligen täglichen Einnahme und der physiologischeren Nachahmung des zirkadianen Rhythmus im Tagesverlauf.19,20 Plenadren® ist nur für die Behandlung Erwachsener zugelassen. Efmody® ist ein weiteres neuartiges Hydrocortisonpräparat mit modifizierter Wirkstofffreisetzung, das 2021 für Patient:innen mit AGS ab 12 Jahren zugelassen wurde. Es besteht aus einem Kern, der mit Mikrokristallen gefüllt ist, und einer Polymerummantelung, was zu einer verzögerten und kontinuierlichen Freisetzung des Wirkstoffs führt. Durch die Einnahme von Efmody® gemäß einem spezifischen Dosierungsschema nach einem Zahnputzregime (ein Drittel der Tagesdosis um 7:00 Uhr und zwei Drittel um 23:00 Uhr) können deutlich physiologischere Cortisolkonzentrationen erzielt werden.21 Der frühmorgendliche Anstieg der Cortisolspiegel ermöglicht dabei eine suffiziente ACTH- und Androgensuppression, die in dieser Patientenkohorte von großem Nutzen ist und eine Dosiseinsparung von Glukokortikoiden ermöglicht.
Tab. 1: Typische Hydrocortison-Substitutionsschemata für Erwachsene mit Nebenniereninsuffizienz. Die Tagesdosis kann je nach Art und Ausprägung der Nebenniereninsuffizienz variieren. Kurz vor dem Schlafengehen sollte kein Hydrocortison in unretardierter Form eingenommen werden (modifiziert nach Husebye et al. 2021)10
Beim Vorliegen einer primären Nebenniereninsuffizienz ist in der Regel auch die Substitution von Mineralokortikoiden erforderlich. Hierfür wird Fludrocortison (meistens 0,1mg/Tag) morgens verabreicht. Auch Dehydroepiandrosteron (DHEA und DHEA-Sulfat, DHEA-S) kann bei einer erniedrigten Plasmakonzentration prinzipiell substituiert werden. Insgesamt ist die Datenlage zu Dosierung und Dauer der DHEA-Substitution jedoch begrenzt und ein potenzieller Nutzen bislang nicht bewiesen.22,23 Bei Patient:innen mit primärer Nebenniereninsuffizienz und persistierender gedrückter Stimmung und/oder verminderter Libido kann ein Substitutionsversuch mit 25–50mg DHEA/d unternommen werden. Patient:innen sollten darüber informiert werden, dass DHEA nicht zum Standardsubstitutionsschema einer Nebenniereninsuffizienz gehört und dass es oft erst verzögert nach mehreren Monaten zu einem Wirkeintritt kommt.23
Notfall in der Praxis: Nebennierenkrisen erkennen und richtig handeln
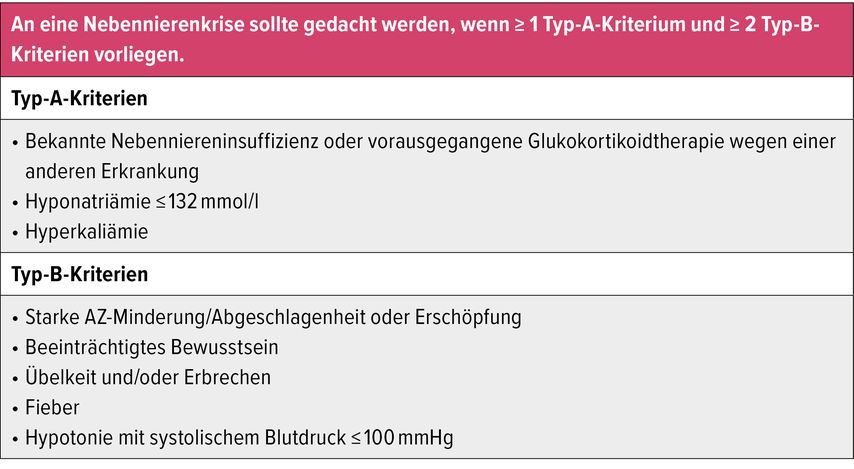
Eine Nebennierenkrise wird häufig als akute Beeinträchtigung des Gesundheitszustands in Verbindung mit spezifischen Kriterien, die sich innerhalb von ein bis zwei Stunden nach Substitution von Glukokortikoiden deutlich bessern, definiert. Es sollten mindestens ein Typ-A-Kriterium und mindestens zwei Typ-B-Kriterien vorliegen (Tab.2). Bei klinischem Verdacht auf eine Nebennierenkrise gilt es, keine Zeit zu verlieren, sondern sofort zu handeln (Tab.3).24 Im ambulanten und stationären Setting sollte bei Erwachsenen hierfür umgehend die Gabe von 100mg Hydrocortison i.v. als Bolus erfolgen, gefolgt von 200mg Hydrocortison/Tag kontinuierlich mittels Perfusor oder wiederholter Bolusgabe von 50mg alle sechs Stunden. In Notfallsituationen zu Hause sollte die umgehende Gabe von 100mg Hydrocortison intramuskulär in den Oberschenkel erfolgen oder „off-label“ eine subkutane Injektion in die Bauchhaut durch die Betroffenen selbst bzw. Angehörige. Im Anschluss muss ein Arzt aufgesucht/informiert werden.24 Bei Nebenniereninsuffizienz und (fieberhaften) Infekten, jedoch ohne Anzeichen einer Nebennierenkrise, empfehlen wir, die doppelte bis dreifache Menge der üblichen oralen Hydrocortisondosis einzunehmen. Bei schwerem Erbrechen kann ein 100-mg-Prednisonzäpfchen (Rectodelt®) angewendet werden. Anschließend sollten sich Betroffene umgehend ärztlich vorstellen. Betroffene müssen Hydrocortisontabletten, ein Hydrocortisoninjektionsset und Prednisonzäpfchen stets in ausreichender Menge vorrätig haben und gemeinsam mit ihrem Notfallausweis in einem leicht zugänglichen Notfallset mitführen. Zur Prävention einer Nebennierenkrise ist die mindestens einmalige Schulung von Patient:innen unerlässlich. Hierbei empfiehlt es sich bei vorliegendem Einverständnis der Betroffenen, mindestens eine weitere Person aus dem Familien-/Bekanntenkreis (z.B. Partner:in, Kollege, Kollegin) ebenfalls einzuweisen. Betroffene können nützliche Informationen zum Umgang mit Nebennierenkrisen sowie zu Nebennierenschulungen auf den Websites der Österreichischen Gesellschaft für Endokrinologie und Stoffwechsel (ÖGES), der Deutschen Gesellschaft für Endokrinologie (DGE) und der Selbsthilfenetzwerke für Menschen mit Hypophysen- und Nebennierenerkrankungen e.V. (Glandula) erhalten.
Literatur:
1 Lovas K, Husebye ES: High prevalence and increasing incidence of Addison’s disease in western Norway. Clin Endocrinol (Oxf) 2002; 56(6): 787-91 2 Eaton WW et al.: Epidemiology of autoimmune diseases in Denmark. J Autoimmun 2007; 29(1): 1-9 3 Olafsson AS, Sigurjonsdottir HA: Increasing prevalence of Addison disease: results from a nationwide study. Endocr Pract 2016; 22(1): 30-5 4 Laureti S et al.: Is the prevalence of Addison’s disease underestimated? J Clin Endocrinol Metab 1999; 84(5): 1762 5 Meyer G et al.: Increasing prevalence of Addison‘s disease in german females: health insurance data 2008-2012. Eur J Endocrinol 2014; 170(3): 367-73 6 Auer MK et al.: Congenital adrenal hyperplasia. Lancet 2023; 401(10372): 227-44 7 Charmandari E et al.: Adrenal insufficiency. Lancet 2014; 383(9935): 2152-67 8 Hong AR et al.: Characteristics of korean patients with primary adrenal insufficiency: a registry-based nationwide survey in Korea. Endocrinol Metab (Seoul) 2017; 32(4): 466-74 9 Lam KY, Lo CY: A critical examination of adrenal tuberculosis and a 28-year autopsy experience of active tuberculosis. Clin Endocrinol (Oxf) 2001; 54(5): 633-9 10 Husebye ES et al.: Adrenal insufficiency. Lancet 2021 397(10274): 613-29 11 Regal M et al.: Prevalence and incidence of hypopituitarism in an adult Caucasian population in northwestern Spain. Clin Endocrinol (Oxf) 2001; 55(6): 735-40 12 Tomlinson JW et al.: Association between premature mortality and hypopituitarism. West midlands prospective hypopituitary study group. Lancet 2001; 357(9254): 425-31 13 Martin-Grace J et al.: Iatrogenic adrenal insufficiency in adults. Nat Rev Endocrinol 2024; 20(4): 209-27 14 Bancos I et al.: Diagnosis and management of adrenal insufficiency. Lancet Diabetes Endocrinol 2015; 3(3): 216-26 15 Saevik AB et al.: Clues for early detection of autoimmune Addison’s disease - myths and realities. J Intern Med 2018; 283(2): 190-9 16 Ueland GA et al.: The short Cosyntropin test revisited: new normal reference range using LC-MS/MS. J Clin Endocrinol Metab 2018; 103(4): 1696-703 17 Esteban NV et al.: Daily Cortisol production rate in man determined by stable isotope dilution/mass spectrometry. J Clin Endocrinol Metab 1991; 72(1): 39-45 18 Nowotny H et al.: Therapy options for adrenal insufficiency and recommendations for the management of adrenal crisis. Endocrine 2021; 71(3): 586-94 19 Johannsson G et al.: Improved cortisol exposure-time profile and outcome in patients with adrenal insufficiency: a prospective randomized trial of a novel hydrocortisone dual-release formulation. J Clin Endocrinol Metab 2012; 97(2): 473-81 20 Nowotny H, Reisch N: Modified-release hydrocortisone for glucocorticoid deficiency. Internist 2020; 61(6): 565-72 21 Whitaker M et al.: An oral multiparticulate, modified-release, hydrocortisone replacement therapy that provides physiological cortisol exposure. Clin Endocrinol 2014; 80(4): 554-61 22 Alkatib AA et al.: A systematic review and meta-analysis of randomized placebo-controlled trials of DHEA treatment effects on quality of life in women with adrenal insufficiency. J Clin Endocrinol Metab 2009; 94(10): 3676-81 23 Lang K et al.: Is DHEA replacement beneficial in chronic adrenal failure? Best Pract Res Clin Endocrinol Metab 2015; 29(1): 25-32 24 Kienitz T et al.: Adrenal crisis - definition, prevention and treatment: results from a delphi survey. Horm Metab Res 2024; 56(1): 10-5
Das könnte Sie auch interessieren:
Wie oft wird Diabetes nicht oder spät erkannt?
Im Allgemeinen wird von einer hohen Dunkelziffer an Personen mit undiagnostiziertem Typ-2-Diabetes ausgegangen. Ein Teil davon sind von Ärzten „übersehene“ Fälle. Eine von der University ...
Neue Studiendaten zu Typ-2-Diabetes und Lebensstil
Dass gesunde Ernährung und Bewegung das Diabetesrisiko sowie verschiedene Risiken von Patienten mit Diabetes senken, ist seit Langem bekannt. Und das Detailwissen zur Bedeutung von ...
Diabetes erhöht das Sturzrisiko deutlich
Eine dänische Studie kommt zu dem Ergebnis, dass sowohl Patienten mit Typ-1- als auch Patienten mit Typ-2-Diabetes öfter stürzen und häufiger Frakturen erleiden als Menschen aus einer ...