Früher Gewichtsverlust macht Typ-2-Diabetes rückgängig
Bericht:
Dr. med. Anna Maria Roll
Medizinjournalistin
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Neue pathophysiologische Konzepte stellen das bisherige Verständnis des Typ-2-Diabetes (T2D) infrage. Im Mittelpunkt steht nicht mehr der erhöhte Blutzucker, sondern die Rolle von Fettablagerungen in Muskeln, Leber und Pankreas. Beim FOMF Diabetes Update Refresher rollte Prof. Dr. med. Roger Lehmann vom Universitätsspital Zürich die Entstehung des T2D neu auf und stellte aktuelle Präventionsempfehlungen vor. Denn früh behandelt, ist ein T2D reversibel.
Normalerweise speichert der Skelettmuskel überschüssige Kalorien in Form von Glykogen. Muskelglykogen erreicht etwa vier Stunden nach einer Mahlzeit sein Maximum und wird über die folgenden sieben Stunden wieder abgebaut.1 Beim T2D ist diese Glykogenspeicherung eingeschränkt, weshalb die überschüssige Glukose in Fett umgewandelt wird.2 Die Konversion von Glukose zu Fett findet ausschliesslich in der Leber statt. Insulin stimuliert die De-novo-Lipogenese, wodurch vermehrt Fettsäuren (v.a. Palmitinsäure) und in der Folge Triglyzeride gebildet werden. «Mit jedem Essen wird der Körper also mit gesättigten Fettsäuren belastet. Das ist ein erheblicher Risikofaktor für kardiovaskuläre Erkrankungen», erläuterte der Referent.
Die Zwillingszyklus-Hypothese
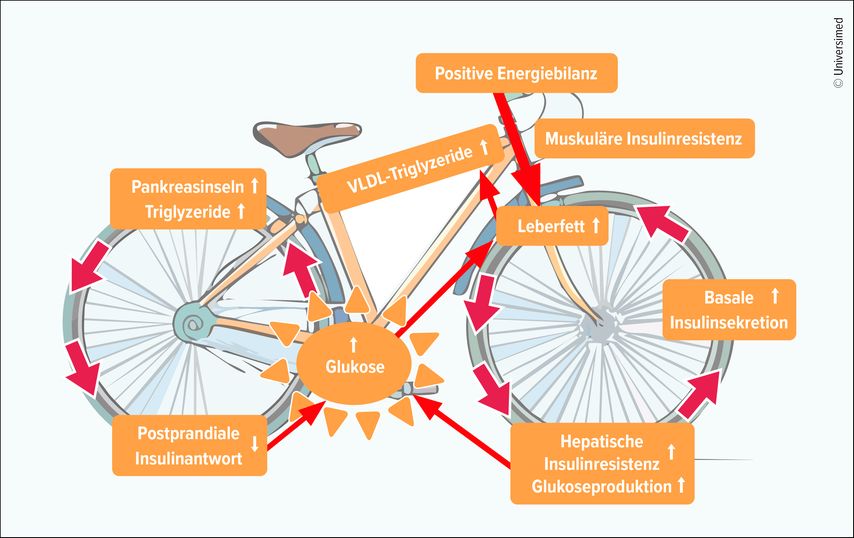
Die Zwillingszyklus-Hypothese postuliert, dass wechselwirkende Teufelskreisläufe ausgelöst durch eine chronische positive Energiebilanz zu Insulinresistenz und einer Funktionsstörung der Betazellen des Pankreas führen (Abb. 1).3 Die Insulinresistenz der Muskeln führt zu einer erhöhten De-novo-Lipogenese und zu einer erhöhten Bildung von Leberfett. Aufgrund des erhöhten Leberfettgehalts nimmt die Resistenz gegenüber der normalen Insulinwirkung, die die Glukoseproduktion in der Leber hemmt, stetig zu. Das Resultat ist ein Anstieg des Nüchtern-Plasmaglukosespiegels und kompensatorisch eine Zunahme des Nüchtern-Plasmainsulinspiegels. Insulin wiederum stimuliert direkt die De-novo-Lipogenese: Ein Teufelksreislauf entsteht. Mit dem steigenden Leberfettgehalt nimmt die Produktion von VLDL-Triglyzeriden zu. Sind die subkutanen Fettspeicher voll, werden ektopische Stellen, darunter die Bauchspeicheldrüse, mit Triglyzeriden überversorgt. Die Folgen sind eine Verfettung der Pankreasinseln und eine Beeinträchtigung der Insulinsekretion. Betroffen ist insbesondere die Erstphasenantwort, also die schnelle Insulinausschüttung nach einer Mahlzeit. Der daraus resultierende Anstieg des postprandialen Plasmaglukosespiegels führt zur einer anhaltenden Hyperinsulinämie, während der Überschuss an Glukose und Insulin die De-novo-Lipogenese verstärkt.
Abb. 1: Laut Zwillingszyklus-Hypothese sind für den Glukoseanstieg drei Mechanismen verantwortlich: die muskuläre Insulinresistenz, die hepatische Insulinresistenz und die Verfettung der Pankreasinseln (adaptiert nach Taylor R 2025)3
Typ-2-Diabetes und Fettleber
Auf die Frage, welcher Fettgehalt der Leber noch als normal gelte, nannte der Referent den in Leitlinien häufig angegebenen Grenzwert von 5%, der auf populationsbasierte MR-spektroskopische Untersuchungen zurückgeht.4 Gleichzeitig wies er darauf hin, dass sich dieser Wert v.a. zur Klassifikation der Steatose und ihres Fortschreitens zur Leberfibrose eignet. Metabolische Studien zeigen, dass hepatisches Fett bereits in niedrigen Konzentrationen mit Insulinresistenz und metabolischer Dysfunktion korreliert. Für die mit einer metabolischen Dysfunktion assoziierte Fettleber liege der relevante Schwellenwert demnach deutlich niedriger, nämlich bei weniger als 2% Leberfett.5 «Und das bedeutet, dass nicht nur diejenigen Patienten, die die 5%-Schwelle überschreiten, eine Leberverfettung aufweisen, sondern alle mit Typ-2-Diabetes», betonte der Diabetologe.
Die Genetik entscheidet, wer erkrankt
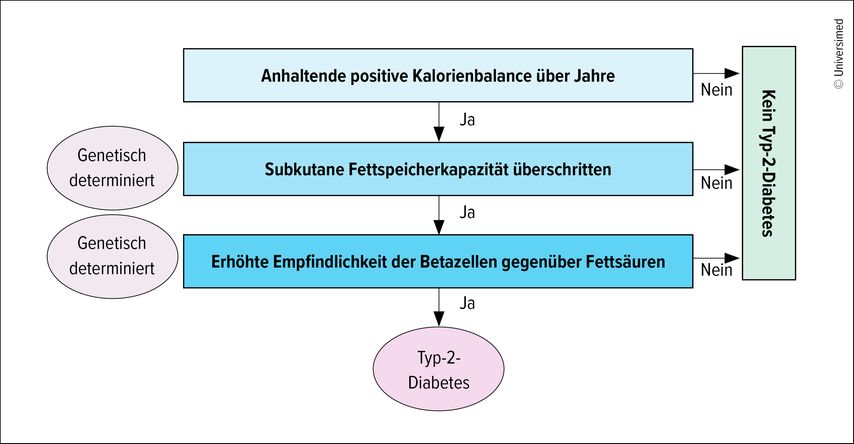
Die Fähigkeit zur subkutanen Fettspeicherung ist individuell und wird durch 53 verschiedene genetische Loci bestimmt.6 «Wird die Aufnahmekapazität überschritten, kommt es aber noch nicht zwingend zum T2D», so der Experte. Damit ein T2D entstehe, müsste neben der individuellen Fettspeicherkapazität noch ein weiterer genetischer Faktor vorhanden sein – die Empfindlichkeit der Betazellen gegenüber Fettsäuren (Abb. 2).3,7 «Die meisten Menschen haben diese Prädisposition zum Glück nicht», erklärte der Referent. «Deshalb haben auch mehr als 70% der stark adipösen Personen keinen Diabetes.»
Abb. 2: Ein Typ-2-Diabetes entsteht nur, wenn zwei genetische Faktoren vorhanden sind: eine zu geringe subkutane Fettkapazität und eine erhöhte Empfindlichkeit der pankreatischen Betazellen für Fettsäuren (adaptiert nach Taylor R 2025)3
Je kürzer die Diabetesdauer, desto eher eine Remission
Klinische Beobachtungen zeigen: Verlieren Patienten mit T2D frühzeitig stark an Gewicht, reduzieren sich das Leberfett und die Triglyzeridspiegel. Darüber hinaus normalisiert sich die schnelle Ausschüttung von Insulin nach einer Mahlzeit.8 «Das heisst, die Betazellfunktion kann sich wieder erholen, wenn die Patienten abnehmen», unterstrich der Diabetologe.
Die COUNTERPOINT-Studie zeigte 2011 erstmals eindrücklich, dass eine massive Kalorienreduktion bei Patienten mit kurzer Diabetesdauer (<4 Jahre) zu einer raschen Normalisierung der Glukosehomöostase führt: Bereits nach sieben Tagen normalisierte sich der Nüchternblutzucker, nach acht Wochen sank das HbA1c von 7,4 auf 6,0%.9 Parallel sanken die hepatischen und plasmatischen Triglyzeride, während die Insulinsensitivität langsam auf Normalwerte anstieg und sich die Erstphasen-Insulinsekretion wieder einstellte. «Die Normalisation der Betazellfunktion hängt von der Diabetesdauer ab», betonte der Experte. Eine Erkenntnis, die auch die COUNTERBALANCE-Studie bestätigte: Während die hepatischen und plasmatischen Triglyzeride bei allen Patienten sanken, verbesserte sich die Insulinsekretion ausschliesslich bei Patienten mit einer Diabetesdauer von weniger als vier Jahren. 10
Gewichtsabnahme und -stabilisierung im Vordergrund – auch bei Normalgewichtigen
Entscheidend für den Erfolg einer Diabetesremission ist jedoch die konsequente Gewichtsstabilisierung, wie die DIRECT-Studie mit knapp 300 Patienten bewies.11 Nach einem Jahr waren 46% der Patienten, die ≥10kg verloren hatten, in Remission, verglichen mit 4% in der Kontrollgruppe. Nach zwei Jahren lag die Remissionsrate bei 36%. Bei den Patienten, die das Körpergewicht nicht halten konnten, stiegen jedoch nach initialer Abnahme sowohl die Nüchternglukose und Triglyzeride als auch das Pankreas- und Leberfett wieder an.12 Nach fünf Jahren verblieben nur 26% der initialen Responder in Remission. «Aber verschwindet das exzessive ektope Fett, dann gehen die Betazellen nicht weiter verloren», unterstrich der Experte. Ausserdem nahmen die kritischen Komplikationen mit Spitalaufenthalt in der Interventionsgruppe um die Hälfte ab.13
Interessant ist: Selbst Normalgewichtige können einen Typ-2-Diabetes entwickeln, wenn ihre subkutanen Fettspeicher erschöpft sind. Dies gelte insbesondere für die asiatische Bevölkerung, merkte der Referent an. Studien belegen, dass nicht nur Adipöse, sondern auch Patienten mit einem deutlich niedrigeren BMI (21–27kg/m2) ebenso von einer Gewichtsabnahme profitieren.14 Remissionen seien in dieser Gruppe zudem leichter zu erhalten.
Diabetesremission reduziert kardiovaskuläres Risiko
Nach internationalem Konsens liegt eine Diabetesremission vor, wenn das HbA1c unter 6,5% liegt. Auch wenn sich die Glukosewerte bei diesen Patienten häufig noch im prädiabetischen Bereich bewegen würden, seien die Hauptursachen makrovaskulärer Erkrankungen, Leberfett und Hypertriglyzeridämie, weitgehend eliminiert, so der Experte. Langzeitdaten aus der Look-AHEAD-Studie zeigen, dass eine über mehrere Jahre anhaltende Remission das Risiko für eine chronische Nierenerkrankung (CKD) um bis zu 55% und für kardiovaskuläre Ereignisse um etwa 50% senkt.15 Hatte zumindest einmal eine vorübergehende Remission bestanden, sank das Risiko für eine CKD immerhin noch um ein Drittel, das für kardiovaskuläre Ereignisse um 40%.
Therapie: möglichst früh, möglichst schnell
Im Vordergrund steht der frühzeitige Gewichtsverlust, idealerweise noch im Prädiabetesstadium. Denn 90% der Patienten mit T2D erreichen mit einem Gewichtsverlust eine Diabetesremission, wenn die Erkrankung erst kurz besteht.13 Wie dieser zustande komme, spiele keine Rolle. Neben einer gesunden Ernährung und einer geringeren Nahrungsaufnahme ist vor allem die körperliche Aktivität wesentlich. Bewegung senkt den Blutzucker ohne Insulin, da sie die Glukoseaufnahme und Glykogenspeicherung in der Muskulatur erhöht. Darüber hinaus reduziert sie Leber- und Muskelfett sowie Entzündungsprozesse.
Moderne Antidiabetika unterstützen diese Prozesse: SGLT2-Hemmer senken insulinunabhängig die Glukose, führen zu moderatem Gewichtsverlust und mindern die Leberverfettung. GLP-1-Rezeptor-Agonisten sowie GIP/GLP-1- und Tripel-Agonisten bewirken eine ausgeprägte Gewichtsreduktion, normalisieren einen Prädiabetes und reduzieren Leberfett und Fibrose substanziell. Die Frage, ob es sinnvoll sei, die Medikamente nach Verschwinden des Diabetes wieder abzusetzen, verneinte der Referent. Seine Begründung: Zum einen würde der Grossteil der Patienten wieder an Gewicht zunehmen, zum anderen rechtfertige der kardiorenale Schutz eine langfristige Therapie. Er wies darauf hin, dass GLP-1- bzw. GIP/GLP-1-Rezeptor-Agonisten für diese Patientengruppe am besten geeignet sind, gefolgt von SGLT2-Hemmern und Metformin, welches die Glukoneogenese hemmt. «Insbesondere die Patienten mit schwerer Insulinresistenz profitieren enorm von der Tripletherapie in den Schweizer Empfehlungen», so der Experte.
Abschliessend hob der Diabetologe hervor, möglichst frühzeitig nahezu normale Blutzuckerwerte anzustreben, da sich dadurch die Gesamtmortalität deutlich reduzieren würde.16 Ausserdem wies er darauf hin, dass sich sämtlichen diabetesbedingten Komorbiditäten vorbeugen lässt. «Je früher Sie beginnen, umso besser.»
Quelle:
FOMF Diabetes Update Refresher, 6. bis 8. November 2025, Zürich
Literatur:
1 Taylor R et al.: Direct measurement of change in muscle glycogen concentration after a mixed meal in normal subjects. Am J Physiol 1993; 265: E224-9 2 Carey PE et al.: Direct assessment of muscle glycogen storage after mixed meals in normal and type 2 diabetic subjects. Am J Physiol Endocrinol Metab 2003; 284: E688-94 3 Taylor R: Aetiology of type 2 diabetes: an experimental medicine odyssey. Diabetologia 2025; 68: 1375-89 4 Szczepaniak LS et al.: Magnetic resonance spectroscopy to measure hepatic triglyceride content: prevalence of hepatic steatosis in the general population. Am J Physiol Endocrinol Metab 2005; 288: E462-8 5 Petersen KF et al.: Ethnic and sex differences in hepatic lipid content and related cardiometabolic parameters in lean individuals. JCI Insight 2022; 7: e157906 6 Lotta LA et al.: Integrative genomic analysis implicates limited peripheral adipose storage capacity in the pathogenesis of human insulin resistance. Nat Genet 2017; 49: 17-26 7 Kashyap S et al.: A sustained increase in plasma free fatty acids impairs insulin secretion in nondiabetic subjects genetically predisposed to develop type 2 diabetes. Diabetes 2003; 52: 2461-74 8 Lee Y et al.: Beta-cell lipotoxicity in the pathogenesis of non-insulin-dependent diabetes mellitus of obese rats: impairment in adipocyte-beta-cell relationships. Proc Natl Acad Sci USA 1994; 91: 10878-82 9 Lim EL et al.: Reversal of type 2 diabetes: normalisation of beta cell function in association with decreased pancreas and liver triacylglycerol. Diabetologia 2011; 54: 2506-14 10 Steven S et al.: Very low-calorie diet and 6 months of weight stability in type 2 diabetes: pathophysiological changes in responders and nonresponders. Diabetes Care 2016; 39: 808-15 11 Lean MEJ et al.: Durability of a primary care-led weight-management intervention for remission of type 2 diabetes: 2-year results of the DiRECT open-label, cluster-randomised trial. Lancet Diabetes Endocrinol 2019; 7: 344-55 12 Zhyzhneuskaya SV et al.: Time course of normalization of functional β-cell capacity in the diabetes remission clinical trial after weight loss in type 2 diabetes. Diabetes Care 2020; 43: 813-20 13 Lean ME et al.: 5-year follow-up of the randomised diabetes remission clinical trial (DiRECT) of continued support for weight loss maintenance in the UK: an extension study. Lancet Diabetes Endocrinol 2024; 12: 233-46 14 Taylor R et al.: Aetiology of type 2 diabetes in people with a «normal» body mass index: testing the personal fat threshold hypothesis. Clin Sci (Lond) 2023; 137: 1333-46 15 Gregg EW et al.: Impact of remission from type 2 diabetes on long-term health outcomes: findings from the Look AHEAD study. Diabetologia 2024; 67: 459-69 16 Adler AI et al.: Post-trial monitoring of a randomised controlled trial of intensive glycaemic control in type 2 diabetes extended from 10 years to 24 years (UKPDS 91). Lancet 2024; 404: 145-55
Das könnte Sie auch interessieren:
Wie oft wird Diabetes nicht oder spät erkannt?
Im Allgemeinen wird von einer hohen Dunkelziffer an Personen mit undiagnostiziertem Typ-2-Diabetes ausgegangen. Ein Teil davon sind von Ärzten „übersehene“ Fälle. Eine von der University ...
Neue Studiendaten zu Typ-2-Diabetes und Lebensstil
Dass gesunde Ernährung und Bewegung das Diabetesrisiko sowie verschiedene Risiken von Patienten mit Diabetes senken, ist seit Langem bekannt. Und das Detailwissen zur Bedeutung von ...
Diabetes erhöht das Sturzrisiko deutlich
Eine dänische Studie kommt zu dem Ergebnis, dass sowohl Patienten mit Typ-1- als auch Patienten mit Typ-2-Diabetes öfter stürzen und häufiger Frakturen erleiden als Menschen aus einer ...