Gewichtsabnahme unter GLP-1-Rezeptor-Agonisten immer erwünscht?
Autorin:
OÄ Dr. Andrea Malzner
Abteilung für Innere Medizin I
Klinikum Wels-Grieskirchen
E-Mail: Andrea.Malzner@klinikum-wegr.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
GLP-1-Rezeptor-Agonisten (GLP-1-RA) und duale GLP-1/GIP-Agonisten haben in den letzten Jahren einen festen Stellenwert in der Therapie des Typ-2-Diabetes (T2D) und der Adipositas erlangt. Trotz ihres günstigen Wirkprofils insbesondere im Hinblick auf das kardiovaskuläre Outcome stehen – überwiegend gastrointestinale – Nebenwirkungen sowie ein potenzieller Zusammenhang mit Pankreaserkrankungen immer wieder im Fokus klinischer Diskussionen.
Keypoints
-
Der vorliegende Fall verdeutlicht, dass gastrointestinale Symptome unter Inkretintherapie nicht vorschnell als medikamentöse Nebenwirkung interpretiert werden sollten.
-
Red Flags sind dabei eine zunehmende Verschlechterung der glykämischen Kontrolle unter Therapie, persistierende oder bei längerer Therapiedauer neuaufgetretene Symptome sowie fehlende Besserung nach Absetzen der Medikation.
-
Insbesondere bei progredientem Gewichtsverlust (v.a. bei Menschen mit Diabetes) ist eine weiterführende Diagnostik zwingend erforderlich.
Inkretinbasierte Therapien, insbesondere GLP-1-RA und zuletzt auch vermehrt duale GLP1-/GIP-RA, werden aufgrund ihrer effektiven Blutzuckersenkung, ihres kardiovaskulären Zusatznutzens, der Verbesserung metabolischer Parameter und ausgeprägter Gewichtsreduktion zunehmend breit eingesetzt. Ein Teil ihrer therapeutischen Wirkung wird durch eine Verlangsamung der Magen-Darm-Motilität und die zentrale Wirkung auf Appetit und Sättigung vermittelt. Dem gegenüber stehen überwiegend gastrointestinale Beschwerden wie Übelkeit, Völlegefühl und Erbrechen, aber auch Obstipation und Diarrhö, in zumeist milder bis moderater Ausprägung. Die Beschwerden treten vor allem in der Titrationsphase auf und bessern sich zumeist im weiteren Therapieverlauf. Klinischen Studien ist eine Abbruchrate von 6–10% zu entnehmen – vermutlich hauptsächlich durch die genannten gastrointestinalen Nebenwirkungen begründet. Bei einem kleineren Anteil an Patient:innen kann es zu anhaltenden dyspeptischen oder gastropareseähnlichen Symptomen kommen. Die Prävalenz und Schwere dieser gastrointestinalen Nebenwirkungen nehmen tendenziell mit steigender Dosis zu, wobei v.a. in der Indikation Adipositas höhere Dosierungen verwendet werden.1–3
Aufgrund des Wirkmechanismus der GLP1-RA und GLP1/GIP-RA im enterohumoralen System wird ein Zusammenhang mit Pankreaserkrankungen wie Pankreatiden und Pankreaskarzinomen immer wieder diskutiert. Gleichzeitig besteht bei Patient:innen mit Adipositas und/oder Typ-2-Diabetes per se ein erhöhtes Risiko für bestimmte maligne Erkrankungen, wie beispielsweise gastrointestinale Tumoren. Die Abgrenzung zwischen medikamentenassoziierten Nebenwirkungen und strukturellen Ursachen stellt im klinischen Alltag oftmals eine relevante Herausforderung dar.4–6
Fallbeschreibung
Anamnese und Vorerkrankungen
Ein 63-jähriger männlicher Patient stellte sich im April 2025 erstmalig in unserer Notaufnahme vor. Der Patient berichtete über seit wenigen Wochen bestehende, vorwiegend postprandiale Übelkeit und Erbrechen und konsekutiv reduzierte Nahrungsaufnahme. Fallweise bestand auch eine moderate Abdominalgie. In den letzten drei Wochen hatte der Patient nach eigenen Angaben etwa 6kg Körpergewicht verloren. An relevanten Vorerkrankungen bestanden ein Typ-2-Diabetes, Adipositas, arterielle Hypertonie, Hypercholesterinämie sowie ein Z.n. tiefer Venenthrombose vor einigen Jahren unter laufender oraler Antikoagulation.
Die antidiabetische Therapie umfasste Metformin, Empagliflozin (SGLT2-Inhibitor) sowie Semaglutid (GLP1-RA). Aufgrund der geschilderten Beschwerden und verminderter Nahrungsaufnahme hatte der Patient, wie stets in Patient:innenschulungen zur Diabetestherapie empfohlen, Empagliflozin und Semaglutid bereits vor der Konsultation in unserer Akutversorgungseinrichtung pausiert. Der letzte dem Patienten erinnerliche HbA1c lag bei 9%. Die weitere Medikation bestand aus Rivaroxaban, Rosuvastatin, Amlodipin und Valsartan/Hydrochlorothiazid (HCT).
Der Patient war Nichtraucher. Die Anamnese für kardiovaskuläre Ereignisse oder Malignome sowohl bei ihm als auch in der Familie war leer. Eine Vorsorgekoloskopie wurde bereits vor ca. 10 Jahren durchgeführt, mit anamnestisch unauffälligem Ergebnis. Aufgrund der Beschwerdesymptomatik wurde bereits durch den Hausarzt eine Abklärung mittels Videokinematografie des Ösophagus/Schluckaktröntgen veranlasst. Hierbei zeigte sich eine moderate Hypomotilität des Ösophagus, die sich im Liegen etwas verstärkte, mit verstärkten Kontrastmittelretentionen im distalen Ösophagus. Es ergab sich kein Hinweis auf einen gastroösophagealen Reflux oder eine fixierte Stenose.
Klinischer Befund und Labor
Bei Aufnahme präsentierte sich der Patient in leicht reduziertem Allgemeinzustand, afebril. Es zeigten sich eine grenzwertig hypertensive Blutdrucklage (139/99mmHg), eine Herzfrequenz von 98/min sowie als auffälligster Laborbefund ein deutlich erhöhter Blutzucker von 339mg/dl. Der pH-Wert lag bei 7,53, es ergab sich somit kein Hinweis auf das Vorliegen einer diabetischen Ketoazidose. Die übrigen Laborbefunde lagen im Normbereich. Klinisch war das Abdomen weich und druckschmerzfrei, die Darmgeräusche zeigten sich spärlich, aber ansonsten in unauffälliger Qualität in allen vier Quadranten. Aufgrund der Hyperglykämie und der protrahierten, letztlich unklaren gastrointestinalen Beschwerdesymptomatik erfolgte eine stationäre Aufnahme zur weiteren Abklärung und Blutzuckereinstellung. Ein nachträglich eingelangter HbA1c-Wert betrug 10,3%.
Diagnostik und Verlauf
Bildgebung und Endoskopie
In einer initialen Sonografie zeigte sich die Gallenblase trotz Nüchternheit nicht distendiert, soweit ersichtlich aber nicht wandverdickt ohne schallschattengebende Konkremente. Die Gallenwege waren schlank. Der Magen imponierte auffällig prall gefüllt, der Pylorus und die Pars descendens des Duodenums waren erweitert. Das Pankreas war nur unzureichend einsehbar. Ansonsten ergaben sich keine Auffälligkeiten an den Oberbauchorganen, Nieren und im kleinen Becken. Kein Hinweis auf freie Flüssigkeit.
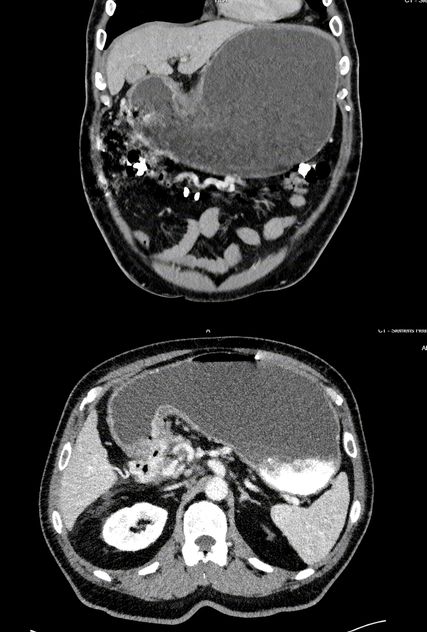
Abb. 1 und 2: Computertomografie Abdomen: massiv dilatierter Magen mit Kalibersprung am Pylorus und tumoröser Infiltration ausgehend vom Pankreaskopf
Gastroskopisch zeigte sich das Bild einer Refluxösophagitis Grad D, wobei als auffallendster Befund größere Speisereste im Magen imponierten. Das Antrum zeigte sich, soweit beurteilbar, verquollen, womit sich insgesamt der Verdacht auf eine Magenausgangsstenose ergab. In routinemäßig entnommenen Gewebeproben aus Antrum und Corpus des Magens zeigte sich histologisch eine geringgradige Gastritis (Typ C) ohne Nachweis von Helicobacter pylori. In einer weiterführend veranlassten kontrastmittelgestützten CT-Untersuchung zeigte sich ein massiv dilatierter Magen mit Spiegelbildung und Kalibersprung im Bereich des Pylorus. Die Magenwand war bis zu 2cm verdickt und nicht eindeutig vom Pankreaskopf abgrenzbar (Abb.1 und 2). Es zeigte sich eine wohl vom Pankreaskopf ausgehende, schwer vermessbare, den Pylorus infiltrierende weichteildichte Raumforderung mit Umscheidung der Arteria hepatica propria und ihrer Aufgabelung im Bereich der Leberpforte. Der Pankreasschwanz war hochgradig atrophiert, der Ductus pancreaticus mit 6mm erweitert. Womit sich insgesamt ein hochgradig suspekter Befund für ein Pankreaskarzinom ergab.
Weiterer Verlauf
Bemerkenswerterweise war der Patient zum Aufnahmezeitpunkt nur leicht übergewichtig (BMI 28kg/m2, Größe 170cm, Gewicht 81kg). Es konnte retrospektiv ein Beginn der GLP1-RA-Therapie vor circa 2,5 Jahren exploriert werden. Damals wog der Patient 110kg, was einem BMI von 38,1kg/m2 entsprach.
Die Verträglichkeit der Therapie wurde zunächst als gut angegeben. Insbesondere die Blutzuckereinstellung habe sich anfangs deutlich verbessert. Im weiteren Verlauf traten dann häufiger Abdominalgien und Inappetenz auf. Aufgrund des deutlichen, anhaltenden und subjektiv sehr erwünschten Gewichtsverlusts hielt der Patient an der Therapie fest. In konsekutiven hausärztlichen Kontrollen fiel schließlich eine zunehmende Verschlechterung der glykämischen Kontrolle auf. Die vom Patienten geschilderten Beschwerden wurden mit dem bekannten gastrointestinalen Nebenwirkungsprofil von GLP-1-RA in Übereinstimmung gebracht.
Eine Magnetresonanztomografie des Pankreas erhärtete den Verdacht einer suspekten Raumforderung im Pankreaskopf. Bildgebend ergab sich kein Hinweis auf Fernmetastasen. Aufgrund des ausgedehnten Lokalbefundes sowie der Gefäßumscheidung bzw. Infiltration durch den Tumor bestand jedoch primär eine Inoperabilität. Mittels ultraschallgezielter Feinnadelpunktion konnte die Diagnose eines duktalen Pankreas-Adenokarzinoms gesichert werden (positiver Panzytokeratinmarker AE1/3, kräftig nukleär positiv mit Antikörpern gegen p53, Proliferationsmarker Ki67, deutlich erhöhte proliferative Aktivität, positive Reaktion der atypischen Proliferate mit Antikörpern gegen CK7, keine Reaktion mit der Dopplerfärbung CK20/CDx2, keine nukleäre Reaktion mit Antikörpern gegen TTF-1, Reaktion mit Antikörpern gegen MUC 1 und MUC 5AC schwach zytoplasmatisch positiv).
Weil eine adäquate orale Flüssigkeits- und Nahrungszufuhr mittlerweile völlig unmöglich war, wurde eine palliative Gastroenterostomie durchgeführt. Eine tumorspezifische Therapie im Sinne einer systemischen Chemotherapie nach dem FOLFIRINOX-Schema wurde etabliert. Zur Blutzuckertherapie erfolgte der Beginn einer Basis-Bolus-Insulintherapie mit Semglee und Novorapid. Die orale andidiabetische Medikation wurde gänzlich beendet. Ein Tumorstaging im Juli 2025, also 3 Monate nach Diagnosestellung bzw. Therapiebeginn, zeigte einen stabilen Erkrankungsverlauf („stable disease“).
Diskussion
GLP-1-Rezeptor-Agonisten und Magenentleerung
GLP-1 hemmt physiologisch die Magenentleerung nach dem Essen und reduziert die Magensäuresekretion. Weiters kommt es zu einer vagal vermittelten Suppression der Peristaltik von Magen und Duodenum sowie zu einer Erhöhung des Pylorusdrucks. Enterohumorale Feedbackmechanismen reduzieren die Magen-Darm-Motilität und die Sekretion von Verdauungssekreten. Dadurch kommt es zu einem vermehrten Sättigungsgefühl, weniger Appetit und einer letztlich verminderten Nahrungsaufnahme.7,8
Praxistipp
Die verzögerte Magen-entleerung unter GLP1-RA- bzw. GLP1/GIP-RA-Therapie muss in Situationen wie z. B. vor Operationen oder Endoskopien bedacht werden. Es besteht kein klarer Zusammenhang zwischen subjektiven gastro-intestinalen Beschwerden und in Studien objektiv gemessener verlängerter Magenentleerungszeit.Randomisierte Studien zeigen eine dosisabhängige Verzögerung der Magenentleerung, insbesondere bei kurz wirksamen GLP-1-RA wie Liraglutid, während für lang wirksame Substanzen wie Semaglutid nach längerer Therapiedauer kein konsistenter Effekt nachweisbar war. Zudem besteht kein klarer Zusammenhang zwischen subjektiven gastrointestinalen Beschwerden und objektiv gemessener Magenentleerungszeit. Immer häufiger problematisch ist die verzögerte Magenentleerung unter GLP-RA bzw. GLP1/GIP-RA im klinischen Alltag aufgrund der zunehmend breiten Verwendung vor allem bei Eingriffen, die formal eine Nüchternheit des Patienten/der Patient:in voraussetzen, wie etwa bei Endoskopien oder Operationen, was sich in verschiedenen Konsensuspapieren und Leitlinien der jeweiligen Fachgesellschaften widerspiegelt. Eine sehr praktische Handlungsempfehlung kann dem Konsensuspapier der Österreichischen Adipositas Gesellschaft zum Thema Übergewicht und Adipositas bei Erwachsenen entnommen werden (flüssige Nahrung 24 Stunden vor dem Eingriff, im Zweifelsfall präoperativ, interventionelle Sonografie des Magens, um ggf. Vorhandensein von Mageninhalt zu beurteilen, vor elektiven Eingriffen kann eine einwöchige Pausierung der Inkretintherapie erwogen werden).9–14
GLP-1-RA und Pankreaskarzinom
Trotz früher Sicherheitsbedenken im Hinblick auf Pankreaserkrankungen aufgrund der direkten Wirkung von GLP-1-RA und GLP-1/GIP-RA auf die Azinuszellen des Pankreas bzw. einer Steigerung der pankreatischen Enzymsekretion zeigen aktuelle große Beobachtungsstudien und Metaanalysen keine Evidenz für ein erhöhtes Risiko für Pankreatitis oder Pankreaskarzinomen unter Inkretintherapie. Bezüglich des Pankreaskarzinoms sind wir in den letzten Jahren mit steigenden Prävalenzraten konfrontiert, wobei zu den komplexen und gegenwärtig nicht gänzlich geklärten zugrunde liegenden Mechanismen neben genetisch prädisponierenden Faktoren weitere Risikofaktoren wie Adipositas, Typ-2-Diabetes und Nikotinkonsum hinzukommen. Adipositas stellt dabei einen der stärksten Risikofaktoren für das Pankreaskarzinom dar, mit einer signifikanten Zunahme der Mortalität mit steigendem BMI. Retrospektive Analysen nach metabolischer Chirurgie deuten sogar auf eine Reduktion der Malignominzidenz hin, auch für Pankreaskarzinome.5,6,15–17
Klinische Implikationen
GLP-1-RA sind wirksame und insgesamt sichere Medikamente in der Therapie von Typ-2-Diabetes und Adipositas, was bereits in zahlreichen kardiovaskulären Outcome-Studien gezeigt werden konnte. Aufgrund der positiven Datenlage in verschiedenen anderen medizinischen Bereichen sind künftige Zulassungserweiterung und eine damit breitere Anwendung anzunehmen (z.B. bei metabolisch assoziierter steatotischer Lebererkrankung, obstruktivem Schlafapnoesyndrom u.v.m.)
Eine verzögerte Magenentleerung unter GLP1-RA-Therapie tritt häufig auf und ist in o.g. speziellen medizinischen Situationen gesondert zu beachten. Die häufigsten Nebenwirkungen sind gastrointestinale Beschwerden, wobei diese zumeist in der Titrationsphase transient in milder bis moderater Ausprägung auftreten können. Bei atypischem oder progredientem klinischem Beschwerdebild ist eine strukturelle Ursache konsequent auszuschließen. Aktuell besteht keine wissenschaftliche Evidenz für ein erhöhtes Pankreaskarzinomrisiko unter GLP-1-RA. Diesbezüglich deutet die wissenschaftliche Datenlage vielmehr darauf hin, dass Adipositas einen entscheidenden Risikofaktor darstellt.
Literatur:
1 Aronne LJ et al.: Tirzepatide as compared with Semaglutide for the treatment of obesity. N Engl J Med 2025; 393(1): 26-36 2 Masulli M et al.: GLP-1 and GIP agonists in diabetes and obesity and the rise of dyspepsia. Intern Emerg Med 2025; 20(8): 2291-4 3 Kushner RF et al.: Managing adverse effects of incretin-based medications for obesity. JAMA 2025; 334(9): 822-3 4 Nreau B et al.: Pancreatitis and pancreatic cancer in patients with type 2 diabetes treated with glucagon-like peptide-1 receptor agonists: an updated meta-analysis of randomized controlled trials. Minerva Endocrinol 2023; 48(2): 206-13 5 Pati S et al.: Obesity and cancer: a current overview of epidemiology, pathogenesis, outcomes, and management. Cancers (Basel) 2023; 15(2): 485 6 Poman DS et al.: Pancreatic cancer and the obesity epidemic: a narrative review. Cureus 2022; 14(7): e26654 7 Umapathysivam MM et al.: Comparative effects of prolonged and intermittent stimulation of the Glucagon-like peptide 1 receptor on gastric emptying and glycemia. Diabetes 2014; 63(2): 785-90 8 Wang JY et al.: GLP−1 receptor agonists for the treatment of obesity: Role as a promising approach. Front Endocrinol (Lausanne) 2023; 14: 1085799 9 Brix JM: Konsensuspapier der Österreichischen Adipositasgesellschaft (ÖAG). Wien Klin Wochenschr 2025; 137(5): 167-217 10 Kindel TL et al.: Multisociety clinical practice guidance for the safe use of Glucagon-like peptide-1 receptor agonists in the perioperative period. Surg Obes Relat Dis 2024; 20(12): 1183-6 11 Hashash JG et al.: AGA Rapid Clinical Practice Update on the management of patients taking GLP-1 receptor agonists prior to endoscopy: communication. Clin Gastronterol Hepatol 2024; 22(4): 705-7 12 Ushakumari DS, Sladen RN: ASA consensus-based guidance on preoperative management of patients on glucagon-like peptide-1 receptor agonists. Anesthesiology 2024; 140(2): 346-8 13 Aldawsari M et al.: The efficacy of GLP-1 analogues on appetite parameters, gastric emptying, food preference and taste among adults with obesity: systematic review of randomized controlled trials. Diabetes Metab Syndr Obes 2023; 16: 575-95 14 Jalleh RJ et al.: Clinical consequences of delayed gastric emptying with GLP-1 receptor agonists and Tirzepatide. J Clin Endocrinol Metab 2024; 110(1): 1-15 15 Shinoda S et al.: Obesity and pancreatic cancer: recent progress in epidemiology, mechanisms and bariatric surgery. Biomedicines 2022; 10(6): 1284 16 Wang L et al.: Glucagon-like peptide-1 receptor agonists and pancreatic cancer risk: target trial emulation using real-world data. J Natl Cancer Inst 2025; 117(3): 476-85 17 Drucker DJ: Efficacy and safety of GLP-1 medicines for type 2 diabetes and obesity. Diabetes Care 2024; 47(11): 1873-88
Das könnte Sie auch interessieren:
Wie oft wird Diabetes nicht oder spät erkannt?
Im Allgemeinen wird von einer hohen Dunkelziffer an Personen mit undiagnostiziertem Typ-2-Diabetes ausgegangen. Ein Teil davon sind von Ärzten „übersehene“ Fälle. Eine von der University ...
Neue Studiendaten zu Typ-2-Diabetes und Lebensstil
Dass gesunde Ernährung und Bewegung das Diabetesrisiko sowie verschiedene Risiken von Patienten mit Diabetes senken, ist seit Langem bekannt. Und das Detailwissen zur Bedeutung von ...
Diabetes erhöht das Sturzrisiko deutlich
Eine dänische Studie kommt zu dem Ergebnis, dass sowohl Patienten mit Typ-1- als auch Patienten mit Typ-2-Diabetes öfter stürzen und häufiger Frakturen erleiden als Menschen aus einer ...