Traitement par des anticorps dans la BPCO: premières autorisations et nombreuses questions en suspens
Compte-rendu:
Reno Barth
Journaliste médical
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Les premiers médicaments biologiques ont désormais été autorisés dans l’indication de la BPCO pour réduire le risque d’exacerbation. Plusieurs autres médicaments biologiques font l’objet d’études cliniques dans cette indication. Parfois contradictoires, les résultats constatés ne sont toutefois que partiellement compris. Les anticorps pourraient à l’avenir également permettre d’agir sur de nouvelles cibles thérapeutiques et de nouvelles comorbidités.
Jusqu’à récemment, les médicaments biologiques ne jouaient aucun rôle dans la prise en charge de la BPCO. Cela a changé avec l’autorisation de l’anticorps anti-IL-4/IL-13 dupilumab (autorisation Swissmedic en février 2025) et de l’anticorps anti-IL-5 mépolizumab (actuellement autorisé uniquement par la FDA) dans cette indication. Cependant, les médicaments biologiques constituent pour l’heure surtout une option pour les patients présentant un phénotype éosinophile et des exacerbations fréquentes malgré un traitement inhalé maximal. L’intérêt de la recherche s’est au départ essentiellement porté sur le groupe des anticorps ciblant l’IL-5 ou son récepteur, comme le mépolizumab ou le benralizumab, a expliqué le Pr Gerard J. Criner de la Lewis Katz School of Medicine, Temple University, Philadelphie, États-Unis, qui a également souligné que les premières études sur les médicaments biologiques dans l’indication de la BPCO ont donné des résultats peu clairs. Cela a changé avec les études de phase III BOREAS portant sur le dupilumab1 et MATINEE portant sur le mépolizumab2, qui ont toutes deux mis en évidence des réductions significatives du risque d’exacerbation dans les populations traitées.
La sélection des patients fournit des informations pour la pratique clinique quotidienne
Selon G.J. Criner, les résultats des deux études sont assez similaires en ce qui concerne ce critère d’évaluation primaire, mais des différences intéressantes sont constatées en ce qui concerne les critères d’évaluation secondaires. Alors que la fonction pulmonaire et la qualité de vie des patients se sont améliorées de manière significative dans l’étude BOREAS (dupilumab), ce n’était pas le cas dans l’étude MATINEE (mépolizumab) après un an. Un examen de la sélection des patients fournit des explications possibles pouvant également être pertinentes pour des recommandations dans la pratique clinique quotidienne, selon G. J. Criner. Par exemple, l’ensemble des patients des études portant sur le dupilumab souffraient de bronchite chronique, alors que ce n’était pas une condition préalable à l’inclusion dans les études portant sur le mépolizumab.
La population de l’étude MATINEE comprenait des patients atteints de BPCO de grade GOLD 2 à 4, tandis que l’étude BOREAS n’incluait que des patients atteints de BPCO de grade GOLD 2 et 3. Les patients pouvaient être inclus quel que soit leur stade de dyspnée dans l’étude MATINEE, tandis que seuls les patients présentant une dyspnée de stade 2 à 4 pouvaient l’être dans l’étude BOREAS. La qualité de vie à l’inclusion était légèrement meilleure dans l’étude BOREAS par rapport à l’étude MATINEE. Des analyses de sous-groupes indiquent également des réponses différentes dans différentes populations. La réduction du taux d’exacerbation sous mépolizumab a été plus marquée en cas de grade GOLD 3 ou 4 par rapport au grade GOLD 2. En revanche, la qualité de vie s’est améliorée sous mépolizumab, surtout en cas de grade GOLD 2. La durée des études est également pertinente, car la deuxième année de traitement dans l’étude MATINEE a également vu une amélioration de la fonction pulmonaire par rapport au placebo. Selon l’intervenant, cela montre que les biothérapies peuvent avoir besoin de plus de temps pour déployer pleinement leurs effets.
Pour illustrer la complexité de la situation, il a cité l’étude de phase III RESOLUTE portant sur le benralizumab, qui n’a pas atteint le critère d’évaluation primaire selon les informations fournies par le fabricant, bien que la population de l’étude ait été sélectionnée sur la base de deux études antérieures.3Les conditions préalables à l’inclusion étaient des exacerbations fréquentes et un nombre d’éosinophiles dans le sang d’au moins 300cellules/μl sous traitement inhalé maximal.
Alarmines comme cible thérapeutique
L’inflammation de type 2 n’est toutefois pas la seule cible potentielle de la biothérapie dans la BPCO. Des stratégies visant à agir sur les alarmines, des cytokines épithéliales, sont également étudiées. Les anticorps ciblant la «thymic stromal lymphopoietin» (TSLP) offrent l’option d’inhiber à la fois les voies de signalisation T2 et T1/T17. De même, l’IL-33 constitue une cible potentielle. Une corrélation avec un risque accru d’exacerbation a été mise en évidence tant pour l’IL-33 que pour la TSLP.4 Les conséquences sur le plan clinique ne sont pas encore claires.
L’anticorps anti-IL-33 itépékimab n’a pas réduit le risque d’exacerbation dans l’étude de phase II menée dans une population atteinte de BPCO. Cependant, des analyses de sous-groupes ont montré qu’il était bien efficace chez les anciens fumeurs, mais pas chez les fumeurs actifs ou les non-fumeurs.5 Deux études de phase III ont été menées sur la base de ces données, rendant la situation encore plus confuse. Le critère d’évaluation primaire a été atteint après 52 semaines dans l’étude AERIFY-1, mais pas dans l’étude AERIFY-2, alors que tout laissait présager un succès dans les premières phases de l’étude. Les raisons de cet échec ne sont pas claires, mais une explication possible réside dans le taux d’événements globalement très faible, l’étude ayant été menée pendant la pandémie de Covid-19.
L’anticorps monoclonal ciblant le récepteur ST2 de l’IL-33 astégolimab est également étudié dans l’indication de la BPCO. Les données de phase II de l’étude ALIENTO, qui documentent une réduction de 15,4% des exacerbations modérées ou sévères, ont été présentées dans le cadre du congrès de l’ERS.6 Dans une deuxième étude de phase II (ARNASA), une réduction numérique des exacerbations dans des proportions similaires a été observée, mais celle-ci n’était pas significative. «L’évaluation plus précise des données dans les semaines à venir apportera, nous l’espérons, plus de clarté dans ces résultats», a déclaré G.J. Criner.
Les données de phase II concernant l’anticorps anti-IL-33 tozorakimab sont également contradictoires. Celles-ci étaient toutefois suffisamment positives pour justifier l’initiation de plusieurs études de phase III. De même, le critère d’évaluation primaire de réduction du risque d’exacerbation n’a pas été atteint avec le tézépélumab, qui cible la TSLP, dans une étude de phase II. Les analyses de sous-groupes chez les patients présentant un nombre plus élevé d’éosinophiles dans le sang montrent toutefois un effet très net du traitement.7
Nouvelles cibles thérapeutiques: «mucus plugs» et comorbidités
De nouvelles cibles thérapeutiques cliniques dans la BPCO sont également envisagées. G. J. Criner a souligné que les effets défavorables du «mucus plugging» (bouchon muqueux) dans la BPCO sont un problème fréquent qui a des conséquences négatives sur la fonction pulmonaire, la qualité de vie, le risque d’exacerbation et la mortalité. Chez les patients asthmatiques, une réduction du «mucus plugging» a été démontrée pour plusieurs médicaments biologiques. Pour la BPCO, les données correspondantes font jusqu’à présent défaut.
Une autre cible pertinente est l’inflammation neutrophile, sur laquelle les traitements disponibles n’ont jusqu’à présent guère d’effet. G. J. Criner a fait référence à une étude montrant une réduction du risque d’exacerbation chez les patients souffrant de bronchectasie grâce à l’inhibiteur oral de la dipeptidyl peptidase-1 brensocatib.8 Des patients atteints de BPCO ont également été inclus dans l’étude. Dans ce sous-groupe, le brensocatib a été aussi efficace que dans l’ensemble de la population. Cependant, aucune étude n’a été menée jusqu’à présent pour déterminer si le brensocatib présente également des avantages chez les patients atteints de BPCO sans bronchectasie.
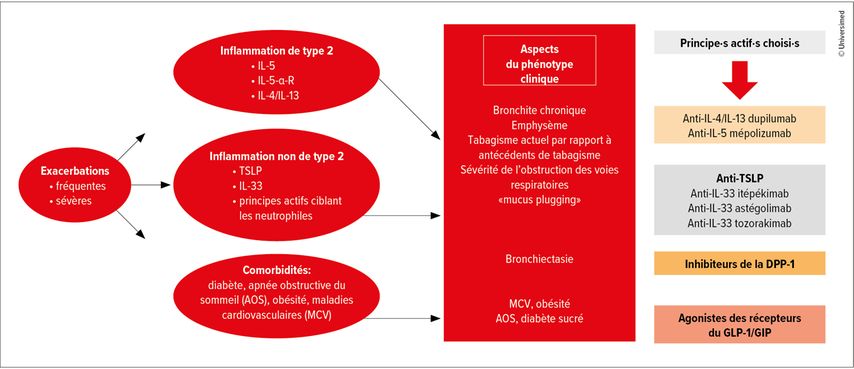
Enfin, il est possible d’agir sur différentes comorbidités fréquentes dans la BPCO (Fig.1). Cela concerne par exemple le groupe des agonistes des récepteurs du GLP-1 (GLP-1-RA), utilisés pour traiter le diabète de type 2 et l’obésité. Les données d’études rétrospectives portant sur une population atteinte de BPCO et de diabète de type 2 montrent que le risque d’exacerbation de la BPCO était corrélé aux antidiabétiques utilisés, les GLP-1-RA, suivis des inhibiteurs du SGLT2, étant associés au risque le plus faible.9 Cependant, il n’est pas clair si les GLP-1-RA réduisent également le risque d’exacerbation chez les patients atteints de BPCO qui ne souffrent pas de diabète.
Fig.1: Intégration du phénotype clinique avec des facteurs endotypiques (modifiée selon Criner GJ 2025)
Source:
Congrès 2025 de l’ERS, du 27 septembre au 1er octobre 2025, à Amsterdam
Littérature:
1 Bhatt SP et al.: N Engl J Med 2023; 389: 205-14 2 Sciurba FC et al.: N Engl J Med 2025; 392: 1710-20 3 https://www.astrazeneca.com/media-centre/press-releases/2025/update-on-resolute-phase-iii-trial.html 4 Joo H et al.: BMC Pulm Med 2021; 21: 86 5 Rabe KF et al.: Lancet Respir Med 2021; 9: 1288-98 6 Greening N et al.: Randomised, placebo-controlled trial of astegolimab for COPD with frequent exacerbations: ALIENTO. ERS 2025, Presentation #1116 7 Singh D et al.: Lancet Respir Med 2025; 13: 47-58 8 Chalmers JD et al.: N Engl J Med 2025; 392: 1569-81 9 Foer D et al.: Am J Respir Crit Care Med 2023; 208: 1088-100
Das könnte Sie auch interessieren:
Infection par le VIH chez les personnes âgées: quels sont les défis?
Grâce aux progrès de la médecine, le VIH est aujourd’hui une maladie chronique qui peut être traitée et les patient·es peuvent avoir une espérance de vie presque normale. De plus en plus ...
Médicaments biologiques dans l’asthme sévère: l’embarras du choix
Pour le traitement de l’asthme bronchique sévère, six anticorps monoclonaux aux cibles différentes sont actuellement autorisés dans l’UE et en Suisse. Les biomarqueurs aident à choisir ...
Directives de l’ERS sur la bronchiectasie
L’European Respiratory Society (ERS) a élaboré de nouvelles recommandations pour la prise en charge de la bronchiectasie. Une nouveauté importante concerne le seuil clinique à partir ...