Médicaments biologiques dans l’asthme sévère: l’embarras du choix
Compte-rendu:
Reno Barth
Journaliste médical
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Pour le traitement de l’asthme bronchique sévère, six anticorps monoclonaux aux cibles différentes sont actuellement autorisés dans l’UE et en Suisse. Les biomarqueurs aident à choisir le médicament biologique approprié pour chaque patient·e. Il faut également prendre en compte le tableau clinique ou les comorbidités, qui peuvent indiquer un traitement optimal.
L’asthme sévère est associé à des exacerbations fréquentes, à une mauvaise qualité de vie, à des effets secondaires qui bouleversent la vie des patient·es en raison d’une exposition prolongée aux corticoïdes, à une mortalité accrue et à des frais de santé élevés. Entre 5 et 10% des personnes asthmatiques sont concernées, selon le PrGuy Brusselle de l’Hôpital universitaire de Gand, en Belgique.
Une manière d’aborder le phénotypage consiste à s’interroger sur le début de la maladie. Typiquement, les phénotypes qui apparaissent à l’âge adulte sont moins souvent associés à une allergie, a expliqué G.Brusselle. Les différents phénotypes de l’asthme peuvent également être identifiés à l’aide de divers biomarqueurs. G. Brusselle a qualifié de particulièrement pertinents le taux d’éosinophiles dans le sang et la fraction expirée du monoxyde d’azote (FeNO), qui sont respectivement corrélés à l’interleukine (IL-)5 et à l’IL-13 dans les voies respiratoires. Si un seul des deux biomarqueurs est élevé, il s’agit d’un asthme de type 2 (T2-high). Dans l’asthme non T2 (T2-low), les deux marqueurs sont faibles.1 Le taux d’éosinophiles dans le sang («blood eosinophile count», BEC) est un marqueur pronostique des exacerbations et la FeNO fournit des informations supplémentaires. Si les deux marqueurs sont élevés, le risque d’exacerbation est maximal. Dans de tels cas, les directives GINA recommandent l’utilisation d’un médicament biologique (niveau 5 de la GINA) en plus du traitement de référence inhalé par des LAMA/LABA/CSI.
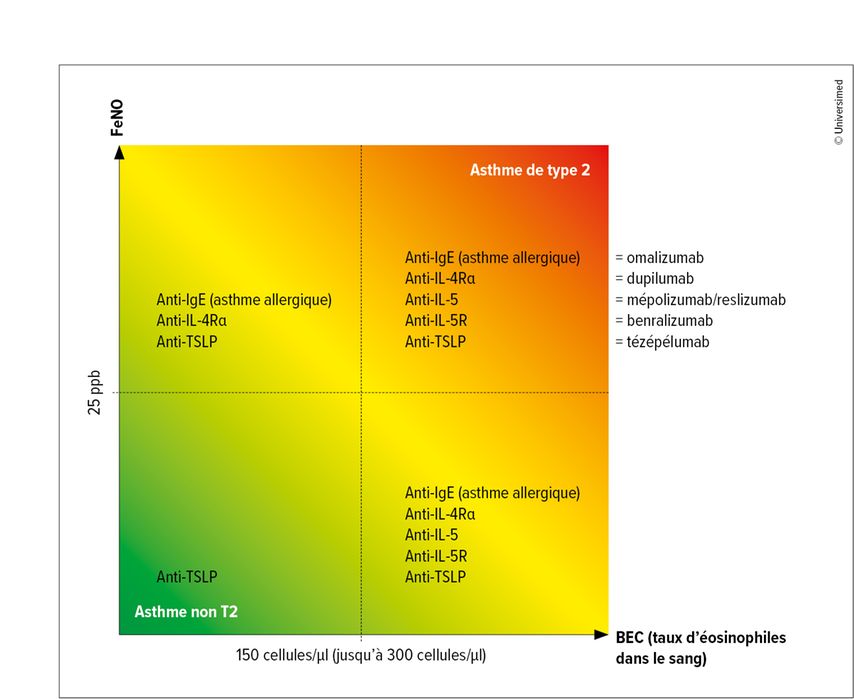
Six médicaments biologiques sont actuellement autorisés dans le traitement de l’asthme: le tézépélumab est un anticorps ciblant l’alarmine TSLP, le dupilumab cible les récepteurs de l’IL-4/IL-13 et l’omalizumab les IgE. Le mépolizumab, le reslizumab et le benralizumab sont des anticorps monoclonaux ciblant l’IL-5 ou son récepteur (Fig.1).
Fig.1: FeNO et BEC: facteurs prédictifs de la réponse thérapeutique des médicaments biologiques dans l’asthme sévère non contrôlé (modifiée selon Brusselle GG et Koppelman GH 2022)1
Réductions significatives du risque d’exacerbation sous médicaments biologiques
L’étude MENSA portant sur le mépolizumab et menée dans une population présentant des exacerbations fréquentes ainsi que des taux élevés d’éosinophiles dans le sang a par exemple démontré ce dont ces anticorps étaient capables. Le médicament biologique a réduit le taux d’exacerbation de 47% et amélioré la qualité de vie.2 Cependant, G. Brusselle a ajouté qu’il ne fallait pas s’attendre à un résultat comparable dans toutes les populations. Le mépolizumab n’a réduit les exacerbations que de 23% chez les enfants et les adolescents. Inversement, l’effet a été encore plus marqué chez les patient·es dont la maladie a débuté très tardivement et qui présentaient une rhinosinusite comorbide avec polypes nasaux, avec une réduction de 80% du taux d’exacerbation.3 De même, le benralizumab a uniquement montré un effet dans l’asthme éosinophile sévère chez les patient·es dont l’asthme avait débuté à 18 ans ou plus. «Ce ne sont pas seulement les biomarqueurs qui comptent, mais aussi le tableau clinique», a déclaré G. Brusselle.
Le dupilumab a montré une efficacité particulièrement bonne chez les patient·es présentant une FeNO élevée.4 Selon G.Brusselle, cela n’est pas surprenant du fait que le dupilumab inhibe l’IL-13 et que l’IL-13 est corrélée à la FeNO. Le tézépélumab est également le plus efficace en cas de taux d’éosinophiles et de FeNO élevés.5 Cependant, l’intervenant a souligné que le tézépélumab était le premier médicament biologique à réduire significativement les exacerbations, même en cas de taux d’éosinophiles et de FeNO faibles. Cela s’explique par le fait qu’il intervient tôt dans la cascade inflammatoire.
Facteurs dans le choix des médicaments biologiques
Dans la pratique clinique quotidienne, il faut faire un choix. Les exacerbations survenues au cours de l’année précédant le début de la biothérapie sont un facteur qui plaide en principe en faveur de cette dernière. Si le taux d’éosinophiles est élevé, cela plaide en faveur d’un anticorps anti-IL-5 ou anti-IL-5R. Les patient·es présentant un taux d’éosinophiles élevé, une FeNO élevée et/ou prenant des corticoïdes oraux sont de bonnes candidat·es pour le dupilumab. L’asthme allergique constitue un facteur en faveur de l’omalizumab; il n’existe aucun biomarqueur prédictif fiable. Le tézépélumab peut en revanche être utilisé en cas d’exacerbations fréquentes, même si ni le taux d’éosinophiles ni la FeNO ne sont élevés. En pratique, le médicament biologique choisi doit être administré pendant au moins quatre mois avant de pouvoir évaluer son efficacité.
G. Brusselle a toutefois recommandé de ne pas se baser uniquement sur les biomarqueurs, mais de prendre aussi en compte le tableau clinique. Le schéma ABCDE («age and age at onset», «biomarkers», «comorbidities», «dosing», «exacerbations») est indiqué. Pour illustrer l’importance des comorbidités, G. Brusselle a cité la dermatite atopique qui, si elle est présente en tant que comorbidité, doit orienter le choix vers le dupilumab. Il a également souligné que de bons résultats thérapeutiques peuvent uniquement être attendus chez les patient·es présentant des exacerbations fréquentes pour l’ensemble de ces médicaments biologiques.
Nouvelles options thérapeutiques
À l’avenir, G. Brusselle s’attend à une utilisation plus précoce de ces médicaments biologiques chez les patient·es à haut risque. Il sera également possible d’allonger les intervalles entre les doses grâce à des anticorps monoclonaux à longue durée d’action. Enfin, les anticorps ainsi que les nanocorps bi- et trispécifiques permettront de s’attaquer à plusieurs cibles à la fois. G.Brusselle a cité comme exemple le nanocorps expérimental Lunsekimig ciblant l’IL-13 et la TSLP.
Source:
Congrès 2025 de l’ERS, du 27 septembre au 1er octobre 2025, à Amsterdam
Littérature:
1 Brusselle GG, Koppelman GH: N Engl J Med 2022; 386: 157-71 2 Ortega HG et al.: N Engl J Med 2014; 371: 1198-207 3 Brusselle G et al.: Respirology 2023; 28: 696-8 4 Castro M et al.: N Engl J Med 2018; 378: 2486-96 5 Menzies-Gow A et al.: N Engl J Med 2021; 384: 1800-9
Das könnte Sie auch interessieren:
Infection par le VIH chez les personnes âgées: quels sont les défis?
Grâce aux progrès de la médecine, le VIH est aujourd’hui une maladie chronique qui peut être traitée et les patient·es peuvent avoir une espérance de vie presque normale. De plus en plus ...
Traitement par des anticorps dans la BPCO: premières autorisations et nombreuses questions en suspens
Les premiers médicaments biologiques ont désormais été autorisés dans l’indication de la BPCO pour réduire le risque d’exacerbation. Plusieurs autres médicaments biologiques font l’objet ...
Directives de l’ERS sur la bronchiectasie
L’European Respiratory Society (ERS) a élaboré de nouvelles recommandations pour la prise en charge de la bronchiectasie. Une nouveauté importante concerne le seuil clinique à partir ...