Hochfluss-Sauerstofftherapie: wann und wie lange?
Bericht:
Dr. Corina Ringsell
Redaktorin
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Hochfluss-Sauerstofftherapie (HFOT) kann die inspiratorische Sauerstofffraktion (FiO2) verbessern. Sie hat einen dynamischen Effekt auf den positiven endexspiratorischen Atemwegsdruck (PEEP), verringert die Atemarbeit sowie den Totraum und verbessert die mukoziliäre Clearance, was für die Heimtherapie der wichtigste Effekt ist.1–3 Doch für welche Patienten ist diese Therapie geeignet?
Die HFOT für die Anwendung zu Hause ist für alle Patienten mit einer durch entsprechende Studien belegten Indikation geeignet. Die meiste Evidenz gibt es für die chronisch obstruktive Lungenkrankheit (COPD), es liegen aber auch Studien zu Bronchiektasien und zur interstitiellen Lungenkrankheit (ILD) vor.
Langzeit-Sauerstofftherapie bei COPD
Eine dänische Studie von 2018 untersuchte 200 Personen mit stabiler COPD, die zu Hause eine Langzeit-Sauerstofftherapie (LTOT) erhielten. Sie hatten einen medianen PaCO2 von 6,5kPa und median drei Exazerbationen pro Jahr. Sie wurden randomisiert zwischen Standardsauerstofftherapie und Behandlung mit Sauerstoff plus HFOT mittels High-Flow-Nasenkanüle (HFNC) aufgeteilt. Studiendauer war ein Jahr. Die HFOT wurde etwa sechs Stunden pro Tag, meist nachts, verabreicht. Der Durchfluss war mit 20l/min bei HFOT geringer als die Durchflussraten im Spital, aber mit anderen Studien zur HFOT im häuslichen Bereich vergleichbar. Das Gleiche gilt für den Sauerstofffluss mit 1,8l/min.
Es zeigte sich, dass die COPD-Exazerbationen in der HFNC-Gruppe im Vergleich zur Kontrollgruppe deutlich zurückgingen (3/J vs. 5/J; p<0,001). Der Dyspnoe-Score verbesserte sich ebenso wie der PaCO2 (–0,4kPa; p=0,005) und der 6-Minuten-Gehtest (+30m; p=0,005), was insgesamt auch die gesundheitsbezogene Lebensqualität steigerte. Die Zahl der Hospitalisationen war dagegen in beiden Gruppen gleich.4
Eine Metaanalyse bisheriger Vergleichsstudien mit insgesamt 440 COPD-Patienten mit/ohne HFOT zeigt, dass die HFOT die Zahl akuter Exazerbationen im Vergleich zur Standard-LTOT reduziert (RR: 0,77; 95% CI: 0,66–0,89) und die Häufigkeit von Krankenhausaufenthalten senken kann (RR: 0,87; 95% CI: 0,69–1,09).5 Der zugrunde liegende Mechanismus ist vermutlich die Verbesserung der mukoziliären Clearance. Aufgrund der Daten werden häufige COPD-Exazerbationen inzwischen zunehmend als eine Indikation für HFOT zu Hause anerkannt. Derzeit laufen vier randomisierte kontrollierte Studien zur HFOT zu Hause, sodass wir weitere Daten dazu erhalten werden.
HFNC versus NIV: die Studienlage
Zahlreiche Studien haben den Einsatz der HFNC bei akuter Exazerbation der COPD (AECOPD) untersucht und ob sowie nach welchen Kriterien sie alternativ zur nichtinvasiven Beatmung (NIV) eingesetzt werden kann.
Eine italienische Studie umfasste 79 Patienten mit leichten bis moderaten AECOPD (Blut-pH 7,25–7,35; PaCO2 ≥55mmHg vor Atemunterstützung). Primärer Endpunkt dieser Nichtunterlegenheitsstudie war die Senkung des PaCO2 innerhalb von zwei Stunden, Hauptsekundärendpunkte waren die Senkung des PaCO2 innerhalb von sechs Stunden und die Rate an Therapiewechseln. Das Luftvolumen wurde auf 60l/min, die Lufttemperatur auf 37 Grad eingestellt. Bei Ausgangs-PaCO2-Werten von durchschnittlich >70mmHg in beiden Gruppen senkte die HFNC den PaCO2 nach zwei Stunden um 6,8mmHg (+/–8,7), die NIV um 9,5mmHg (+/–8,5). Der Unterschied war statistisch nicht signifikant (p=0,404). Allerdings waren nach sechs Stunden 32% der Patienten aus der HFNC-Gruppe zur NIV gewechselt und eine Person wurde invasiv beatmet.6
Mehrere Metaanalysen fanden keine signifikanten Unterschiede zwischen NIV und HFNC hinsichtlich Mortalität, Notwendigkeit einer Intubation oder Dauer des Aufenthalts auf der Intensivstation.7–9
Eine der wenigen Studien mit einem negativen Ergebnis schloss 225 Patienten mit schwerer Hyperkapnie (PaCO2 63bzw. 61mmHg) ein. Der primäre Endpunkt war die Rate an Therapieversagen, definiert als endotracheale Intubation oder Wechsel zu einer anderen Studienbehandlungsmethode. Sekundäre Endpunkte waren die Intubations- oder Behandlungswechselraten, Blutgaswerte, Vitalparameter nach 1, 12 und 48 Stunden, die 28-Tage-Mortalität sowie die Dauer des Aufenthalts auf der Intensivstation und im Krankenhaus. Zu einem Therapieversagen kam es bei 25,7% in der HFNC-Gruppe und 14,3% in der NIV-Gruppe. Auch die Intubationsrate war in der HFNC-Gruppe höher (14,2% vs. 5,4%, p=0,026). Hinsichtlich der anderen Endpunkte gab es keine statistisch signifikanten Unterschiede.10
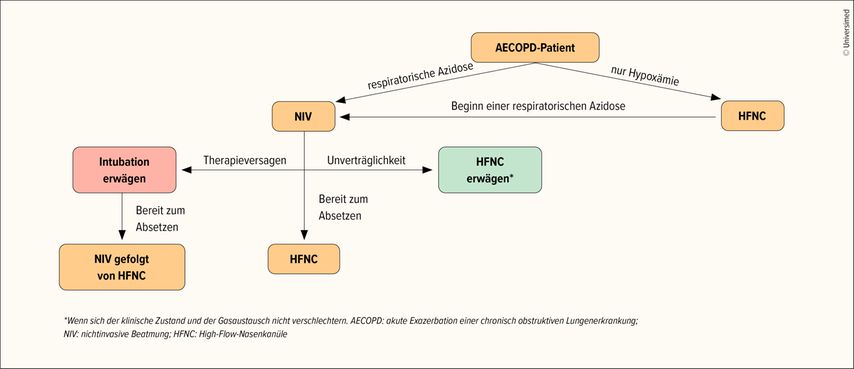
Eine Empfehlung von 2022 besagt, dass bei einer respiratorischen Azidose die NIV nach wie vor Goldstandard ist. HFNC ist Therapie der Wahl, wenn keine respiratorische Azidose vorliegt. Sie kann ausserdem erwogen werden, wenn die NIV nicht vertragen wird. Bei NIV-Versagen sollte eine Intubation in Betracht gezogen werden. Sobald Intubation und NIV nicht mehr nötig sind, kann ebenfalls auf HFNC umgestellt werden (Abb.1).11
Abb. 1: Algorithmus zur möglichen Anwendung von HFNC bei AECOPD-Patienten (modifiziert nach Bruni A et al. 2022)11
HFOT bei Bronchiektasien
Hier ist die Evidenz gering, denn es gibt nur eine randomisierte kontrollierte Studie. Sie schloss 108 stabile Patienten ein, von denen zwei Drittel eine COPD und ein Drittel Bronchiektasien hatten. Sie mussten mehr als zwei Exazerbationen pro Jahr aufweisen und wurden randomisiert entweder der üblichen Behandlung oder der High-Flow-Therapie mittels HFNC zugewiesen. Die HFNC-Therapie wurde nur tagsüber und lediglich für etwa zwei Stunden angewendet. Das Ergebnis bezog sich auf die gesamte Population mit COPD und Bronchiektasien. Dabei liessen sich für die HFNC-Gruppe eine signifikante Verlängerung der Dauer bis zur ersten Exazerbation (52 vs. 27 Tage; p=0,05), eine Senkung der Exazerbationsrate (2,97 vs. 3,63; p=0,067) und eine Abnahme der Zahl der Exazerbationstage pro Jahr (18,2 vs. 33,5; p=0,045) feststellen. Betrachtet man nur die Population mit Bronchiektasien (n=45), so wurden ebenfalls eine Verringerung der Exazerbationsrate und eine signifikante Verbesserung der damit verbundenen Lebensqualität beschrieben.12
Eine retrospektive Fall-Kontroll-Studie zu Bronchiektasie aus Italien mit 40 Bronchiektasiepatienten konnte eine signifikante Abnahme der Anzahl der Exazerbationen innerhalb eines Jahres und einen signifikanten Rückgang der Anzahl der Krankenhausaufenthalte zeigen. Zudem kam es zu einer leichten Verbesserung der Lungenfunktion.13
HFOT bei ILD
Noch weniger Daten gibt es für die ILD. Derzeit liegt nur eine sehr kleine randomisierte kontrollierte Cross-over-Studie mit neun ILD-Patienten vor. Das Ergebnis: Mit der HFOT kam es zu einer statistisch und klinisch signifikanten Verlängerung der Distanz im 6-Minuten-Gehtest und einer Verkürzung der Zeit bis zur Sättigungserholung nach dem Gehtest. Allerdings konnte keine Verbesserung der gesundheitsbezogenen Lebensqualität in Bezug auf Dyspnoe oder Schlafqualität festgestellt werden.14
Dauer der Sauerstofftherapie
Die Ziele der Sauerstofftherapie sind die Korrektur der Hypoxämie und die Verbesserung der physiologischen Parameter, um die körperliche Leistungsfähigkeit zu steigern, die kognitiven Funktionen zu verbessern, kardiovaskuläre Komorbiditäten zu verringern und die Hospitalisierungsrate zu senken. Hauptziel sind jedoch die Verbesserung der gesundheitsbezogenen Lebensqualität und die Senkung der Mortalität.
Die LTOT ist nur angezeigt bei schwerer Hypoxämie, definiert als PaO2 <56mmHg oder PaO2 <60mmHg in Verbindung mit Polyzythämie (Ht >54%) oder Cor pulmonale. Bei moderater Hypoxämie senkt sie weder die Hospitalisierungsrate noch die Mortalitätsrate. Die gesundheitsbezogene Lebensqualität wird nicht verbessert und das Fortschreiten zu einer schweren Hypoxämie nicht verhindert.15
Die derzeit gültigen europäischen und US-amerikanischen Leitlinien empfehlen eine Anwendung von mindestens 15 Stunden pro Tag.16–18
Herausforderungen
Eines der grössten Hindernisse ist die Überwachung der Therapie. Daten aus dem dänischen Sauerstoffregister zeigen, dass nur rund 40% der Patienten nach Beginn der Sauerstofftherapie nachbehandelt wurden. Diese Nachsorge erfolgte hauptsächlich dann, wenn die Therapie von einem Lungenfacharzt eingeleitet wurde und eine sehr klare Verschreibung der erforderlichen Sauerstoffdauer vorlag. Diese Studie zeigte ausserdem, dass die Hälfte der Patienten keine Verschreibunghinsichtlich der Dauer der Sauerstofftherapie erhielt.19 Eine weitere Herausforderung ist die Compliance: In einer kanadischen Studie gaben nur 60% der Patienten an, die Sauerstofftherapie mehr als 15 Stunden pro Tag zu nutzen. Die Compliance hängt dabei unter anderem mit der Mobilität zusammen. Ältere Patienten halten sich eher daran, weil sie ihr Zuhause nicht verlassen. Auch ambulante Sauerstoffgeräte erhöhen die Therapietreue.20 Zudem geht die Sauerstofftherapie mit Belastungen für die Patienten einher, zum Beispiel lokalen Beschwerden wie Trockenheit der Schleimhäute, Nasenbluten und Hautentzündungen. Ausserdem haben sie soziale Unannehmlichkeiten mit Geräten, die oft sehr laut sind. Eine koreanische Studie untersuchte solche sozialen Barrieren und kam zu dem Ergebnis, dass 50% der Betroffenen Angst hatten, die Geräte dauerhaft verwenden zu müssen, jeweils 40% der Patienten scheuten die ungewollte Aufmerksamkeit, die sie erregten, oder glaubten, dass sie keinen Sauerstoff benötigten. 20% der Patienten glaubten, dass Sauerstoff für sie schädlich sei.
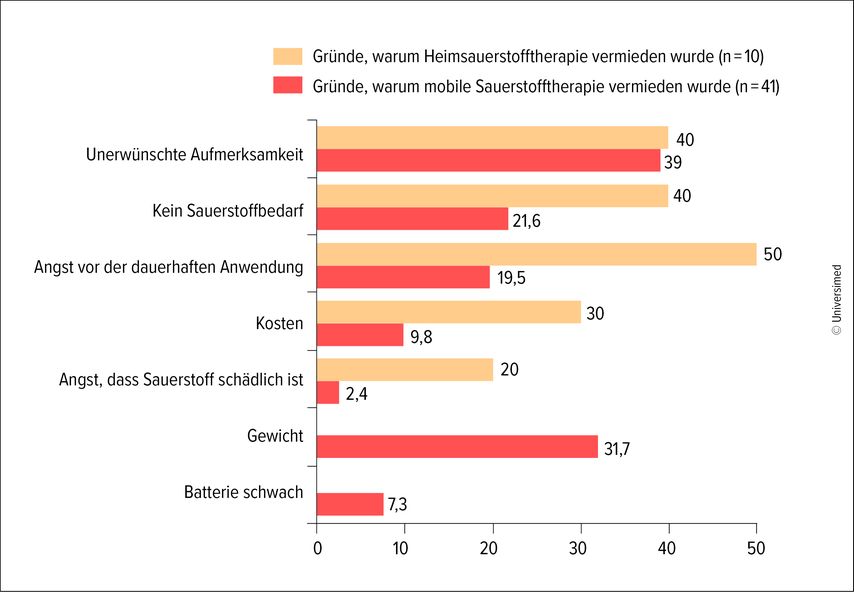
Von den Patienten, die mobile Geräte nutzten, beklagten viele, das Gerät sei zu schwer, die Autonomie zu gering und der Durchfluss lasse sich nicht an ihre Bedürfnisse anpassen (Abb.2). Wichtig ist daher eine Aufklärung der Patienten, warum eine Sauerstofftherapie nötig ist und wozu sie dient.21
Abb. 2: Gründe, warum Patienten die Sauerstofftherapie nicht wie verordnet anwendeten in % (modifiziert nach Kim HJ et al. 2024)21
Ein wichtiger Aspekt sind die Kosten. Rund 30% der Patienten sind besorgt über die Kosten ihrer Therapie. Eine Analyse der französischen nationalen Gesundheitsdatenbank zeigt, dass die Kosten für die Versorgung von sauerstoffabhängigen Patienten vor allem auf Krankenhausaufenthalte zurückzuführen sind und nicht so sehr auf die Kosten für den Sauerstoff selbst. Die Überlebensrate von Patienten, die ein tragbares Gerät haben, ist höher als jene von Patienten, die nur einen stationären Konzentrator erhalten.22
Letztlich muss die Technologie hinsichtlich Mobilität und Sauerstofffluss an die Bedürfnisse der Patienten angepasst werden. Die tatsächliche Therapietreue muss immer wieder erfragt werden, und auch ob die Behandlung die Lebensqualität der Betroffenen tatsächlich steigert.
Quelle:
«Optimal duration of oxygen therapy», Referat von Dr. med. Maura Prella, Lausanne; «HFOT in AE-COPD, according to which criteria should it be used alternately with NIV?», Referat von Prof. Dr. med. Jean-Paul Janssens, Genève; «HF(O)T at home - for which patients and how can we implement it in Switzerland?», Referat von Dr. med. Grégoire Gex, Sion. Jahreskongress der Schweizerischen Gesellschaft für Pneumologie, 15.–16. Mai 2025, Genève
Literatur:
1 Mündel T et al.: J Appl Physiol 2013; 114(8): 1058-65 2 Möller W et al.: J Appl Physiol 2017; 122(1): 191-7 3 Hasani A et al.: Chron Respir Dis 2008; 5(2): 81-6 4 Storgaard LH et al.: Int J Chron Obstruct Pulmon Dis 2018; 13: 1195-205 5 Pitre T et al.: Respir Med 2023; 219: 107420 6 Cortegiani A et al.: Crit Care 2020; 24(1): 692 7 Yang PL et al.: Heart Lung 2021; 50(2): 252-61 8 Feng Z et al.: Int J Chron Obstruct Pulmon Dis 2022: 17: 1987-99 9 Du Y et al.: Can Respir J 2023; doi: 10.1155/2023/7707010 10 Tan D et al.: Crit Care 2024; 28(1): 250 11 Bruni A et al.: Healthcare (Basel) 2022; 10(3): 536 12 Rea H et al.: Respir Med 2010; 104(4): 525-33 13 Crimi C et al.: J Clin Med 2022; 11(24): 7323 14 Weinreich UM et al.: Chron Respir Dis 2022; 19: 14799731221137085 15 Lacasse Y et al.: Lancet Respir Med 2022; 10(11): 1029-37 16 Haidl P et al.: S2k-Leitlinie Langzeit-Sauerstofftherapie. AWMF-Registernummer 020-002 17 Jacobs SS et al.: Am J Respir Crit Care Med 2020; 202(10): e121-41 18 Hardinge M et al.: Thorax 2015; 70(6): 589-91 19 Ringbaek TJ et al.: J Intern Med 2001; 250(2): 131-6 20 Gauthier A et al.: Chron Respir Dis 2019; 16: 1479972318767724 21 Kim HJ et al.: Tuberc Respir Dis (Seoul) 2024; 87(1): 100-14 22 Glezer S et al.: Pulm Ther 2024; 10(2): 237-62; Correction: 263-5
Das könnte Sie auch interessieren:
Asthma – State of the Art: AIR, MART und Biologika
Die lange Zeit in der Behandlung von Asthma bronchiale eingesetzten kurz wirksamen Beta-2-Sympathomimetika sind heute weitgehend obsolet und haben sich im Vergleich zu einer kombinierten ...
Kontroversen in der Diagnostik
Interstitielle Lungenkrankheiten (ILD) sind eine heterogene Gruppe verschiedener Erkrankungen. Daher ist die Diagnostik komplex und umfasst klinische, radiologische und ...