Spannende Daten zu neuen Therapieoptionen bei verschiedenen Entitäten
Bericht:
Reno Barth
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Der jährliche Kongress der American Association for Cancer Research (AACR) fand 2021 wieder virtuell statt. Die in der ersten Kongresswoche im April präsentierten Arbeiten zeigen jedoch, dass es auch in Pandemiezeiten keinen Stillstand in der Krebsforschung gab. Einige präsentierte Studien haben das Potenzial, die klinische Praxis zu verändern.
Neoadjuvanter Einsatz von Nivolumab bei NSCLC
Checkpoint-Inhibitoren finden zunehmend ihren Weg aus der palliativen in die advuvante und neoadjuvante Therapie unterschiedlicher Malignome. So zum Beispiel des nicht kleinzelligen Lungenkarzinoms (NSCLC). „Die Standardtherapie beim resektablen Lungenkarzinom ist die Resektion. Leider sind die Rezidivraten hoch und der rezidivierende Tumor hat eine sehr schlechte Prognose. Platinbasierte Chemotherapie verlängert sowohl bei adjuvantem als auch neoadjuvantem Einsatz das Überleben um lediglich fünf Prozent“, sagt Prof. Dr. Patrick Forde von der Johns Hopkins University. Strategien, die Effektivität dieser Therapie zu verbessern, werden daher dringend gesucht.
Im Rahmen der Phase-III-Studie CheckMate816 wurde unter anderem untersucht, ob der adjuvante Einsatz von Nivolumab die Chancen auf komplettes Ansprechen vor der chirurgischen Therapie verbessert. In CheckMate816 erhielten jeweils 179 Patienten mit resektablem NSCLC und keinen bekannten Alterationen der EGFR oder ALK-Gene randomisiert entweder Nivolumab plus ein Platin-Dublett Chemotherapie oder Chemotherapie alleine. Die Patienten wurden im Anschluss operiert. Komplettes Ansprechen (pCR) war definiert durch das Fehlen von Tumor in den resezierten Lungenabschnitten und Lymphknoten.
Die Studie erreichte ihren ersten primären Endpunkt. Die pCR-Rate lag im Kombinationsarm bei 24% im Vergleich zu 2,2% im Chemotherapie-Arm. Dieses Ergebnis war durch alle Subgruppen konsistent – also unabhängig unter anderem vom Tumorstadium, NSCLC-Subtyp, PD-L1-Status und Geschlecht. Auch die Rate des pathologischen Ansprechens (definiert durch eine Reduktion des Tumors auf maximal 10%) war nach der Kombinationstherapie mit 36,9% signifikant höher als im Chemotherapie-Arm (8,9%). Die Bildgebung zeigte vor der Operation bei 54% der mit Nivolumab-Chemotherapie behandelten Patienten ein objektives Ansprechen – im Vergleich zu 37% nach Chemotherapie. Bei Patienten aus dem Kombinationsarm wurde nach drei Zyklen adjuvanter Therapie auch weniger zirkulierende Tumor-DNA gefunden als bei Patienten aus dem Chemotherapie-Arm und reduzierte Tumor-DNA war assoziiert mit höheren Chancen auf komplettes Ansprechen.
„Zum ersten Mal sehen wir in einer kontrollierten Phase-III-Studie, dass der neoadjuvante Einsatz einer Anti-PD-1-Immuntherapie das Outcome bei frühem Lungenkrebs verbessern kann“, so Forde. Aus retrospektiven Daten lasse sich nun ableiten, dass Patienten mit komplettem Ansprechen vor der Tumorresektion nach neoadjuvanter Chemotherapie länger leben. Dieses Ergebnis sei insofern besonders erfreulich, als die Kombination aus Immuntherapie und Chemotherapie gut vertragen wurde. Unter der Kombinationstherapie traten nicht mehr Toxizitäten auf als unter Chemotherapie alleine und die zusätzliche Gabe von Nivolumab führte in keinem einzigen Fall dazu, dass die Operation abgesagt oder verschoben werden musste. Forde: „Wir haben also die Bestätigung erhalten, dass die neoadjuvante Kombinationstherapie kein Problem für die folgende kurative chirurgische Therapie darstellt. Damit kann CheckMate816 die Praxis im Umgang mit resektablem NSCLC mit hohem Rezidivrisiko verändern. Wir haben bislang ja vor allem adjuvante und nur selten neoadjuvante Strategien eingesetzt.“ Zuvor gelte es aber, die Auswertungen in Bezug auf den zweiten primären Endpunkt, ereignisfreies Überleben, abzuwarten.1
Neues Regime für indolentes Non-Hodgkin-Lymphom
Rituximab-Monotherapie ist eine Standardtherapie für Patienten mit indolentem Non-Hodgkin-Lymphom, die nach einer Rituximab-basierten Therapie eine längere Phase der Remission erreichten und keine Chemotherapie erhalten können oder wollen. Leider sind die Erfolge meist zeitlich begrenzt, wie Dr. Matthew Matasar vom Memorial Sloan Kettering Cancer Center ausführt. Daher werden wirksamere Alternativen dringend gesucht. Im Rahmen der CHRONOS-3-Studie wurde die Kombination von Rituximab mit Copanlisib in einer Population von Patienten mit rezidiviertem indolentem Non-Hodgkin-Lymphom, die mindestens eine oder mehrere Behandlungslinien erhalten hatten, untersucht. Copanlisib ist ein intravenöser Phosphatidylinositol-3-Kinase(PI3K)-Inhibitor der Pan-Klasse I mit Aktivität gegen alle vier Isoformen, einschließlich der in malignen B-Zellen exprimierten PI3K-alpha- und PI3K-delta-Isoformen. Copanlisib wurde in den USA im Rahmen eines beschleunigten Zulassungsverfahrens für die Behandlung von erwachsenen Patienten mit rezidiviertem follikulärem Lymphom (FL) zugelassen, die zuvor mindestens zwei systemische Therapien erhalten hatten. „Präklinische Studien haben gezeigt, dass Lymphomzellen den PI3K-Pathway benötigen und dass die Aktivierung von PI3K Resistenz gegenüber Rituximab begünstigt“, erläutert Matasar die Rationale hinter CHRONOS-3.
CHRONOS-3 ist eine randomisierte, doppelblinde, placebokontrollierte Phase-III-Studie, in die 458 Patienten eingeschlossen und im Verhältnis 2 : 1 randomisiert wurden. Copanlisib wurde an Tag 1, 8 und 15 jedes 28-Tage-Zyklus verabreicht, zusätzlich zu Rituximab, das wöchentlich während Zyklus 1 an den Tagen 1, 8, 15 und 22 und dann am Tag 1 der Zyklen 3, 5, 7 und 9 gegeben wurde. Die Vergleichsgruppe erhielt Rituximab und Placebo nach dem gleichen Schema. In die Studie eingeschlossene histologische Subtypen waren follikuläres Lymphom (FL), kleinzelliges lymphozytisches Lymphom (SLL), lymphoplasmacytoidales Lymphom/Waldenström-Makroglobulinämie (LPL/WM) und Marginalzonen-Lymphom (MZL).
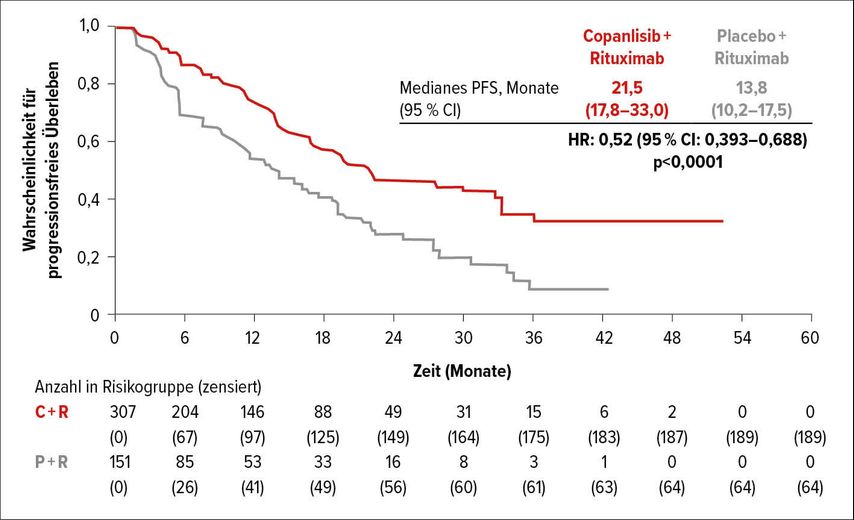
Die Studie erreichte nach einem medianen Follow-up von 19,2 Monaten ihren primären Endpunkt aus progressionsfreiem Überleben und Tod mit einer signifikanten Risikoreduktion um 48% (Abb. 1). Die Ansprechrate betrug im Copanlisib-Rituximab-Arm 80% im Vergleich zu 47,7% im Placebo-Rituximab-Arm. Vollständiges Ansprechen erreichten 33,9% der Patienten im Kombinations- und 14,6% im Placebo-Rituximab-Arm. Die primäre Analyse der Studie wurde durchgeführt, sobald eine bestimmte Anzahl von Events (Tod oder Progression) erreicht war. Damit standen zum Zeitpunkt der Analyse noch zahlreiche Patienten unter Therapie und das mediane Gesamtüberleben konnte zum Zeitpunkt der Auswertung noch nicht abgeschätzt werden. Die Vorteile für die Kombinationstherapie waren in allen histologischen Subtypen gegeben.
Die häufigsten unerwünschten Wirkungen waren Blutzucker- und Blutdruckanstieg, was den bisherigen Erfahrungen mit Copanlisib entspricht. Diese Effekte waren jedoch zeitlich begrenzt und erforderten keine therapeutischen Maßnahmen. Therapieabbrüche waren im Kombinationsarm nur bei 3% der Studienpatienten erforderlich. Pneumonitis als befürchtete schwere Nebenwirkung trat ebenfalls bei 3% der Patienten in der Copanlisib-Rituximab-Gruppe auf. Die gute Verträglichkeit ist von besonderer Bedeutung, da in der Vergangenheit Kombinationen von Rituximab mit oralen PI3K-Inhibitoren zu schweren Toxizitäten, Todesfällen und Studienabbrüchen geführt hatten. Die unerwünschten Effekte treten offenbar mit dem intravenös in einem intermittierenden Schema verabreichten Copanlisib nicht auf. Daher sei diese Studie, so Matasar, auch als „proof of concept“ dafür zu werten, dass Rituximab mit einem PI3K-Inhibitor sicher kombiniert werden kann.
Die Daten wurden simultan zur Präsentation im Rahmen des AACR-Kongresses in Lancet Oncology publiziert.2
Erstmals reduzierte Mortalität beimAderhautmelanom
Im Rahmen des AACR 2021 wurden auch erstmals Phase-III-Daten präsentiert, die die Wirksamkeit einer Therapie beim Aderhautmelanom (malignes uveales Melanom) zeigen. Das Aderhautmelanom ist ein seltener Tumor mit schlechter Prognose. Rund die Hälfte der Betroffenen entwickelt Metastasen und nur vereinzelt wird ein Ansprechen auf Checkpoint-Inhibitoren beobachtet, so Dr. Jessica Hassel von der Universität Heidelberg. Für die metastasierte Erkrankung gibt es keinen Standard of Care und die 1-Jahres-Überlebens-Rate liegt bei 50%.
Nun konnte erstmals eine Verlängerung des Gesamtüberlebens bei Patienten mit metastasiertem Aderhautmelanom durch eine Therapie demonstriert werden.3 Dabei machte man sich die Tatsache zunutze, dass dieser Tumor ein gp100 genanntes melanozytisches Protein in hoher Konzentration exprimiert. Tebentafusp ist ein bispezifisches Fusionsprotein, das einerseits an gp100 und andererseits gleichzeitig als Anti-CD3-Antikörper an T-Zellen bindet und diese damit zu den gp100 exprimierenden Zellen dirigiert. Voraussetzung für die Einsetzbarkeit von Tebentafusp ist ein bestimmter HLA-Typ (A*02:01), den rund 50% der weißen Bevölkerung (die die große Mehrheit der Patientenpopulation mit Aderhautmelanom ausmacht) aufweisen. Hassel: „Tebantafusp wird zu einer Brücke zwischen dem Tumor und den Immunzellen, denen es so ermöglicht wird, den Tumor anzugreifen.“
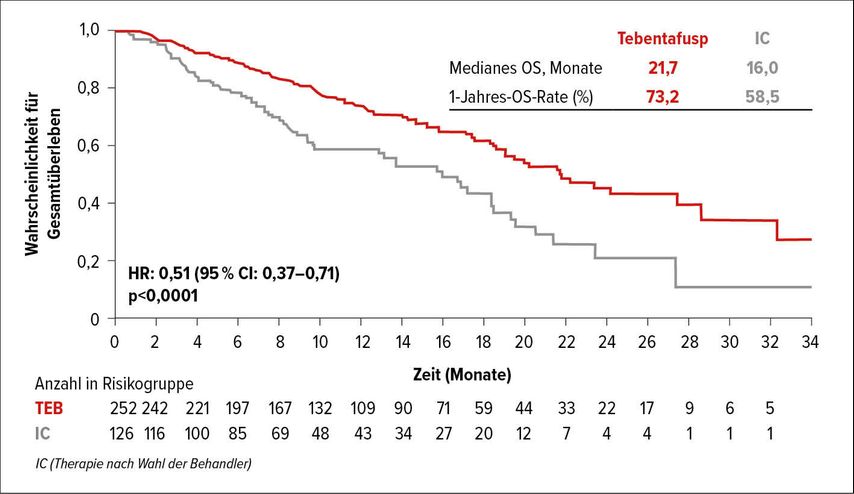
Tebentafusp wurde nun in einer randomisierten, Open-label-Phase-III-Studie mit 378 HLA-A*02:01-positiven Patienten mit Therapie nach Wahl der Behandler (in den meisten Fällen Pembrolizumab) verglichen. Primärer Endpunkt war das Gesamtüberleben. Sekundäre Endpunkte inkludierten Sicherheit sowie das Ansprechen nach RECIST(„Response Evaluation Criteria in Solid Tumors“)-Kriterien, das progressionsfreie Überleben (PFS) und die Krankheitskontrolle. Die nun präsentierten Daten stammen aus der ersten Interimsanalyse, die Ende 2020 durchgeführt wurde. Die Auswertung zeigt eine signifikante Verlängerung des Gesamtüberlebens unter Therapie mit Tebentafusp in der „Intent to treat“- (ITT)-Population um rund die Hälfte (HR: 0,51; 95% CI: 0,36–0,71; p<0,0001) mit einer geschätzten 1-Jahres-Überlebens-Rate von 73,2% (95% CI: 66,3–78,9) gegenüber 58,5% (95% CI: 47,0–66,6) in der Vergleichsgruppe (Abb. 2). Das mediane Gesamtüberleben lag im Tebentafusp-Arm bei 22 Monaten und im Vergleichsarm bei 16 Monaten.
Zum Erstaunen der Autoren war der Effekt auf das progressionsfreie Überleben weniger deutlich, wobei auch hier Signifikanz erreicht wurde. Die Hintergründe sind unklar und in Diskussion. „Das längere Gesamtüberleben wurde auch bei Patienten beobachtet, die kein objektives Ansprechen nach den RECIST-Kriterien zeigten“, sagt Studienautorin Hassel. Der Überlebensvorteil blieb in verschiedenen Subgruppenanalysen, beispielsweise bei einem Vergleich Tebentafusp versus Pembrolizumab, stabil. Auch Alter, Geschlecht oder geografische Region hatten keinen Einfluss auf die Ergebnisse. Generell schnitten Patienten mit niedriger Tumorlast besser ab als Patienten mit hoher Tumorlast.
Die häufigsten Nebenwirkungen betrafen die Haut oder waren Zytokin-mediiert. Gesehen wurden unter anderem Pyrexie, Pruritus und Ausschlag. Diese Nebenwirkungen waren beherrschbar und nahmen nach den ersten drei oder vier Dosen an Häufigkeit und Schwere ab. Weniger als 4% der Patienten brachen die Therapie wegen Nebenwirkungen ab. Es kam zu keinen Todesfällen durch die Therapie.
Prostatakarzinom: der begrenzte Einfluss des Lebensstils
Mit einer großen retrospektiven Beobachtungsstudie4 näherte sich ein Team der Harvard University der Frage, ob und wie weit der Lebensstil das Risiko, an Prostatakrebs zu erkranken bzw. zu sterben, beeinflussen kann. „Genetische Faktoren machen ungefähr 58% der Variabilität des individuellen Prostatakarzinom-Risikos aus“, sagt Studienautorin Dr. Anna Plym. Zahlreiche mit dem Risiko assoziierte Einzelnukleotid-Polymorphismen (SNPs) konnten bereits identifiziert werden. Kürzlich wurde ein Score zur Quantifizierung des Prostatakarzinom-Risikos anhand von 269 SNPs mit hohem Prädiktionswert publiziert.5 Die nun vorgestellte Studie untersuchte nun, wie weit Lebensstilfaktoren zusätzlichen Einfluss auf das genetische Risiko haben.
Dazu wurde zunächst das genetische Risiko von 10443 Männern aus der Health Professionals Follow-up Study, von denen genetische Daten verfügbar waren, quantifiziert. Im Anschluss wurde ein validierter Score zur Ermittlung des Risikos, an einem Prostatakarzinom zu sterben, auf diese Population angewandt. Der Score beinhaltet Körpergewicht, Training, Rauchen und Konsum von Tomaten, Fisch sowie Konsum von verarbeitetem Fleisch.
Über eine mediane Beobachtungszeit von 18 Jahren für die Prostatakarzinom-Inzidenz und 22 Jahren für die Prostatakarzinom-Mortalität wurden 2111 Prostatakarzinom-Erkrankungen und 238 Prostatakarzinom-Todesfälle identifiziert. Die Studie zeigte, dass Männer in der höchsten genetischen Risiko-Quartile im Vergleich zu Männern mit dem niedrigsten Risiko 5,4-mal häufiger an einem Prostatakarzinom erkrankten und 3,5-mal häufiger daran starben. Die zusätzliche Anwendung des Lifestyle-Scores machte die Sache komplexer. In der Quartile mit dem höchsten genetischen Risiko führte ein optimaler Lebensstil (höchste Werte im Score) zu einer Reduktion des Risikos, an einem Prostatakarzinom zu sterben, um rund die Hälfte. Ein gesunder Lebensstil war in der Gruppe der Männer mit dem höchsten genetischen Risiko mit einem Lebenszeitrisiko eines tödlichen Prostatakarzinoms von 3% assoziiert – im Vergleich zu 6% bei Männern mit hohem genetischem Risiko und ungünstigem Lebensstil sowie 3% für die gesamte Studienpopulation. Dies zeige, so Plym, dass sich ein genetisch erhöhtes Risiko, an Prostatakrebs zu sterben, durch einen gesunden Lebensstil normalisieren lässt.
Damit waren allerdings in diesem Kollektiv die Möglichkeiten der Lebensstilintervention ausgeschöpft. Ein günstigerer Lifestyle-Score war weder mit einer geringeren Gesamtinzidenz von Prostatakarzinomen assoziiert noch beeinflusste er die Prostatakarzinom-Mortalität bei Männern mit niedrigerem genetischem Risiko. Die Hintergründe sind unklar. Möglicherweise interagieren, so Plym, gerade jene genetischen Faktoren, die besonders zu einem erhöhten Risiko beitragen, auch am stärksten mit Lebensstilfaktoren. Die Autorin betont auch die Wichtigkeit von Screening-Maßnahmen. Diese könnten sich in Zukunft auch am individuellen genetischen Risiko orientieren.
Quelle:
AACR Annual Meeting 2021, Week 1: 10.–15. April 2021, virtuell
Literatur:
1 Forde PM et al.: Nivolumab + platinum-doublet chemotherapy vs. chemotherapy as neoadjuvant treatment for resectable (IB-IIIA) non-small cell lung cancer in the phase 3 CheckMate-816 trial, AACR 2021, presented during session “CTPL01. Phase III Clinical Trials: Dedicated to the Memory of José Baselga” 2 Matasar MJ et al.: Copanlisib plus rituximab versus placebo plus rituximab in patients with relapsed indolent non-Hodgkin lymphoma (CHRONOS-3): a double-blind, randomised, placebo-controlled, phase 3 trial. Lancet Oncol 2021; S1470-2045(21)00145-5 3 Piperno-Neumann S et al.: Phase 3 randomized trial comparing tebentafusp with investigator‘s choice in first line metastatic uveal melanoma. AACR 2021; CT002 4 Plym A et al.: Can the genetic risk of prostate cancer be attenuated by a healthy lifestyle? Poster 822, presented at AACR 2021, Session PO.EP01.08. Gene-Gene and Gene-Environment Interactions 5 Conti DV et al.: Nat Genet 2021; 53(1): 65-75
Das könnte Sie auch interessieren:
Adjuvantes Osimertinib reduziert ZNS-Rezidive bei EGFR-mutierter Erkrankung
Etwa 30% der Patienten mit nicht kleinzelligem Lungenkarzinom (NSCLC) präsentieren sich mit resezierbarer Erkrankung und werden einer kurativen Operation unterzogen. Viele Patienten ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...