Neues aus dem Bereich der Gynäkoonkologie
Bericht:
Mag. Dr. Anita Schreiberhuber
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Im Rahmen der diesjährigen AGO-Jahrestagung wurden relevante Studienergebnisse präsentiert, wobei v.a. beim Mammakarzinom einige neue Substanzen das Therapiearmamentarium erweitern bzw. sich in klinischen Studien als vielversprechend erweisen. Spannend war auch ein Vortrag über die Subklassifizierung des frühen Ovarialkarzinoms und die damit assoziierten Outcomes.
In der Session zum Ovarialkarzinom (OC) berichtete Univ.-Prof. Dr. Nicole Concin, Medizinische Universität (MU) Innsbruck und Kliniken Essen-Mitte, über das Management von präinvasiven Läsionen und Frühstadien (EOC) sowie über Neuerungen im Konsensusstatement der internationalen gynäkologischen Gesellschaften.1
Erstmals wurde darin das Thema gynäkologische Malignome in der Schwangerschaft aufgegriffen: Die erste Untersuchung, die man bei Verdacht auf einen Tumor machen sollte, ist ein Ultraschall (US), der ausschließlich von Expert*innen durchgeführt werden sollte, denn „Tumoren während der Schwangerschaft können durch Hormoneinwirkung anders aussehen und auch eine Residualisierung von Endometriomen kann Malignome nachahmen“, erläuterte Concin die Herausforderungen einer akkuraten Diagnosefindung.
Nur wenn kein klarer Befund aus der US-Untersuchung resultiert, sollte ein MRT durchgeführt werden. Die Entscheidung für die Durchführung einer Laparoskopie sollte gemäß der Einstufung ovarialer Raumforderungen im US nach den IOTA(International Ovarian Tumor Analysis)-Kriterien erfolgen: Wenn ein Hochrisiko (HR) festgestellt wird, sollte zügig eine operative Abklärung erfolgen.1
Histologie & Staging bei EOC entscheidend
An sich weisen die EOC unabhängig vom histologischen Subtyp eine exzellente Prognose auf, jedoch wurde festgestellt, dass das infiltrative muzinöse, das hochgradige seröse und das hochgradige endometroide OC mit einem 5-Jahres-Rezidivrisiko von 20% einhergehen, beim niedriggradigen serösen und niedriggradigen endometroiden OC beträgt das Risiko 10% und beim niedriggradigen muzinösen OC 5%.2
Ebenso relevant ist das Staging zur Beurteilung, ob es sich tatsächlich um ein frühes Stadium handelt, denn immerhin werden bei einem akkuraten Screening in 20–30% der Fälle okkulte Metastasen detektiert, was entsprechende Konsequenzen für die Therapie mit sich bringt.3 In einer retrospektiven Studie mit 163 Patient*innen war in 15,3% der Fälle – davon bei einem Viertel mit serösen OC – ein Upstaging erforderlich, was die Relevanz eines akkuraten Stagings beim EOC unterstreicht.4
Muzinöses EOC: neue Klassifizierung
„Insbesondere beim muzinösen EOC hat sich sehr viel getan, was die Interpretation der alten Daten schwierig macht. Wir sollten nicht mehr von ‚Low-Grade‘ und ‚High-Grade‘ sprechen, sondern vom expansiven und infiltrativen Typ“, erläuterte Concin und begründete dies damit, dass die beiden Subentitäten eine komplett unterschiedliche Biologie und Prognose aufweisen: Patient*innen mit einem muzinösen EOC vom expansiven Typ werden hauptsächlich im Stadium I diagnostiziert und weisen eine exzellente Prognose auf. Hingegen werden beim EOC vom infiltrativen Typ ca. nur 50% der Patient*innen im Stadium I diagnostiziert und leben mit einem deutlich höheren Rezidivrisiko als jene mit Tumoren vom expansiven Typ.5
Mehrwert durch Chemotherapie?
Aus einer Analyse der SEER(Surveillance, Epidemiology, and End Results)-Datenbank geht hervor, dass eine adjuvante Chemotherapie (CTx) bei keinem histologischen Subtyp des Grades I mit einem signifikanten Benefit einhergeht. Lediglich in der Subgruppe von Patient*innen mit endometroidem EOC im FIGO(Fédération Internationale de Gynécologie et d’Obstétrique)-Substadium IC wurde mit einer CTx eine signifikante Verlängerung des 5-Jahres-Gesamtüberlebens (OS) erzielt. Dieses lag bei unbehandelten Patient*innen bei 83% vs. 62% (p=0,030), die CTx führte zu einer Reduktion des Risikos zu sterben um 42% (HR: 0,58).6
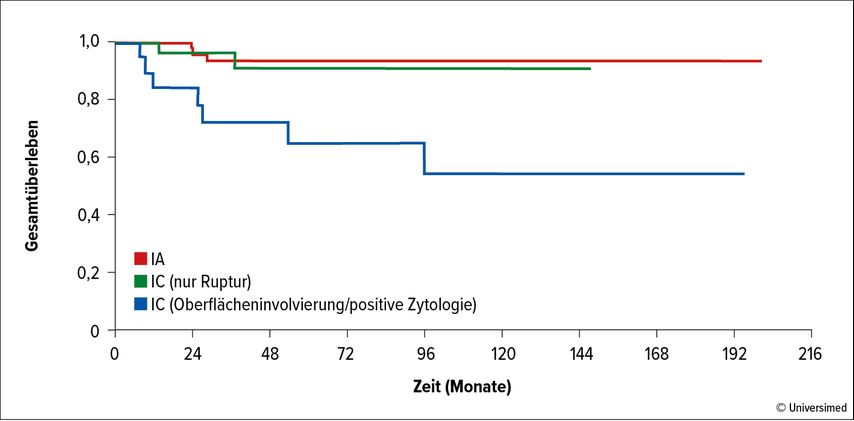
In einer weiteren Untersuchung wurde der Frage nachgegangen, ob bei Stadium IC eine Differenzierung bzgl. der Outcomes möglich ist. Dabei wurde eine Unterscheidung zwischen Einstufung in IC basierend auf einer Zystenruptur vs. aus positiver Zytologie und/oder Oberflächeninfiltration getroffen. Es stellte sich heraus, dass EOC im Stadium IC aufgrund von Zystenruptur ein ähnlich langes OS aufweisen wie Stadium-IA-Malignome. Hingegen wies die andere Subgruppe sehr schlechte Outcomes auf (Abb. 1).7
HR-Positivität beim Mammakarzinom
PIK3CA-Inhibition
„Die CDK4/6-Inhibitoren (CDK4/6-I) haben sich beim lokal fortgeschrittenen/metastasierten HR-positiven, HER2-negativen Mammakarzinom (ABC; MBC) in den vergangenen Jahren zu einem Goldstandard in der Erstlinie entwickelt und rücken zunehmend ins adjuvante Setting“, so die einleitenden Worte von Dr. Tanja Brack, MU Graz, die über diese Substanzklasse und über PIK3CA-I referierte. Mit den Ergebnissen der Phase-III-Studie MonarchE8 hat es Abemaciclib als erster CDK4/6-I bereits in die Adjuvanz geschafft.
Was aber, wenn Patient*innen unter CDK4/6-I eine Progression oder Resistenzen entwickeln?
Ca. 40% der Patient*innen mit HR-Positivität weisen eine aktivierende Mutation (m) im Gen PI3KCA auf, die zu einer Hyperaktivierung der α-Isoform führt.9 Alpelisib ist ein α-spezifischer PIK3-I, der spezifisch die α-Untereinheit von PIK3CA blockiert. Die Substanz wurde basierend auf den Ergebnissen der Studie SOLAR-110 in Kombination mit Fulvestrant (FUL) für postmenopausale Patient*innen mit HR-positiven, HER2-negativen ABC oder MBC mit Nachweis einer PIK3CAm bei Progression nach einer endokrinen Vortherapie zugelassen.11 In SOLAR-1 wurde in der PIK3CAm-Kohorte vs. eine FUL-Monotherapie mit 11,0 gegenüber 5,7 Monate beinahe eine Verdoppelung des progressionsfreien Überlebens (PFS), des primären Endpunkts, erzielt (p=0,65; p<0,001). Demgegenüber wurde in der Kohorte mit PIK3CA-Wildtyp eine Reduktion des Risikos für eine Progression oder den Tod um nur 15% nachgewiesen (HR: 0,85), womit sich der PIK3CA-Status als prädiktiver Parameter bestätigt hat.10
Als wesentlichste und häufigste Alpelisib-assoziierte Nebenwirkung (AE) ist Hyperglykämie zu erwähnen: Sie wurde in SOLAR-1 bei 64% der Patient*innen verzeichnet.10 Ursache dafür ist, dass PI3KCA-I die intrazellulären Effekte von Insulin auf die Leber und die Muskeln blockieren, sodass daraus eine Hyperglykämie resultiert. PI3KA spielt sogar eine Schlüsselrolle in der Glukosehämostase, sodass diese AE nicht unterschätzt werden darf.12 „Der Umgang mit Hyperglykämie ist speziell für Nicht-Internist*innen schwierig. Diese Thematik sollte immer in Rücksprache mit den Diabetolog*innen gemanagt werden“, betonte Priv.-Doz. Dr. Michael Hubalek, Bezirkskrankenhaus Schwaz, der auch die Relevanz der Kontrolle des Nüchternblutzuckerwertes und des Glukosemonitorings hervorhob.
Zudem sei es notwendig, vor Therapiestart Patient*innen zu identifizieren, die Risikofaktoren für die Entwicklung einer Hyperglykämie bzw. eines Diabetes mellitus (DM) aufweisen. Bereits wenn einer der folgenden Faktoren vorliegt, fallen Patient*innen in die HR-Gruppe und sollten vor Therapiestart prophylaktisch 500mg Metformin erhalten:
-
Nüchternblutzucker ≥100mg/dl oder HbA1c ≥5,7%
-
HDL-Cholesterin <35mg/dl und/oder Triglyzeride >250mg/dl
-
BMI (Body-Mass-Index) ≥25kg/m2
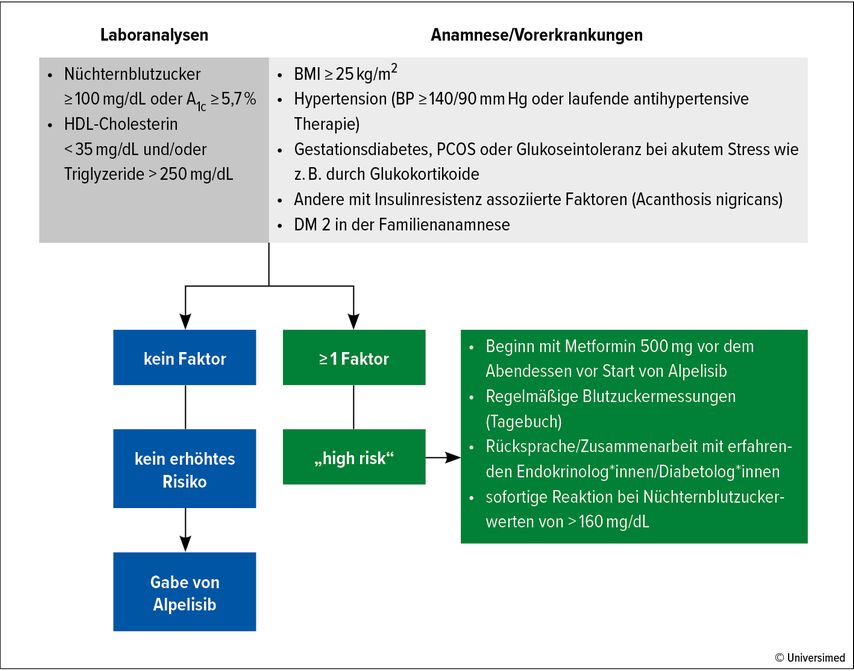
Zu den Komorbiditäten bzw. den anamnestischen Faktoren, die als Risikofaktoren gelten, zählen Hypertonie (Blutdruck ≥140/90mmHg) oder laufende antihypertensive Therapie, Gestationsdiabetes in der Anamnese und DM Typ 2 in der Familienanamnese (Abb. 2).12 Zu weiteren häufigen AE zählen Diarrhö, Stomatitis und Ausschläge10 – „also AE, wie wir sie schon von Everolimus kennen, das ja auch am gleichen Signalweg ansetzt wie Alpelisib“, ergänzte Hubalek. Bei entsprechender Vorsicht und mit regelmäßigem Monitoring seien die Alpelisib-assoziierten AE jedoch managebar.12
Abb. 2: Alpelisib-assoziierte Hyperglykämie: Risikofaktoren und Vorgehensweise. Modifiziert nach Rugo HS et al.12
SERD – eine neue Substanzklasse bei ESR1m
„Eine Resistenzentwicklung beim HR-positiven BC kann Östrogenrezeptor(ER)-unabhängig sein – bedingt durch Aktivierung anderer Signalwege wie bei PIK3CA, dann ist eine Add-on-Therapie nötig. Sie kann aber auch ER-abhängig sein – z.B., indem eine ESR1m zu einer Überaktivierung des ER führt. In dem Fall ist der Switch auf eine andere ET erforderlich. Die Substanzklasse der SERD („selective estrogen receptor degrader“) wurde mit dem Ziel entwickelt, dass dadurch ESR1m-Zellen in die Apoptose geführt werden“, erklärte Assoc. Prof. Priv.-Doz. Dr Georg Pfeiler.
Eine dieser vielversprechenden Substanzen ist Camizestrant. Die Daten aus der Phase-II-Studie SERENA-2 wurden im Dezember 2022 in San Antonio präsentiert. Postmenopausale Patient*innen mit HR-positivem, HER2-negativem ABC (n=240), die unter mehr als einer endokrinen Therapie (ET), die nicht FUL sein durfte, ein Rezidiv oder eine Progression entwickelt hatten, wurden im 1:1:1:1-Design zum Erhalt von Camizestrant, 300mg oder 75mg oder 150mg bzw. FUL randomisiert.
Als primärer Endpunkt war das PFS definiert. Die beiden Dosierungen 75mg und 150mg (die 300-mg-Dosierung floss in die Auswertung nicht ein) führten in vergleichbarem Ausmaß zu einer signifikanten und klinisch bedeutsamen PFS-Verlängerung vs. FUL (7,2 bzw. 7.7 vs. 3,7 Monate; p=0,0124 bzw. 0,0161; HR: 0,58 bzw. 0,67). Die Subgruppenanalyse bestätigte, dass nur Patient*innen mit ESR1m diesen Benefit generiert hatten, in der ESR1-negativen Population war das PFS im Vergleich zur FUL-Gruppe nicht verlängert.
Außerdem wurde nachgewiesen, dass unter Camizestrant nahezu oder gar nicht mehr detektierbare Spiegel an ESR1m und ct(zirkulierende Tumor)DNA erzielt wurden. „Somit handelt es sich bei ESR1m um einen prädiktiven Parameter, der eine Vorhersage bezüglich des Ansprechens auf eine SERD-Therapie ermöglicht. Dass die ESR1m-Zellen abgetötet werden, zeigt, dass die Substanz das umsetzt, was wir von ihr erwarten“, kommentierte Pfeiler diese Ergebnisse. Die AE-Rate war mit jener von FUL vergleichbar.13 Derzeit ist die Phase-III-Studie SERENA-6 (NCT04964934) im Gange: HR-positive, HER2-negative MBC-Patient*innen ohne Nachweis einer Progression und einer bestätigten ESR1m, die unter einer ET (Anastrozol oder Letrozol) plus einem CDK4/6-I (Abemaciclib oder Palbociclib) stehen, werden zum Wechsel auf Camizestrant unter Beibehaltung des CDK4/6-I bzw. zur Fortsetzung der bisherigen Therapie randomisiert.
IO-assoziierte Nebenwirkungen
„Im Grunde wissen wir, dass immunassoziierte AE (irAE) Autoimmunerkrankungen simulieren. In der Pathophysiologie von Autoimmunerkrankungen spielen Polymorphismen, z.B. von PD-L1 oder CTLA-4, eine große Rolle“, informierte OA Dr. Daniel Reimer, MU Innsbruck, der über die Gabe von Immuntherapien (IO) bei Autoimmunerkrankungen und über das Management von irAE referierte. Für rheumatische Erkrankungen wurde gezeigt, dass die Patient*innen unter einer Anti-PD-1-Therapie gehäuft Schübe entwickeln, für Colitis war das unter CTLA-4-gerichteter Therapie der Fall.14 Tang H et al. haben diese Beobachtung in einer Metaanalyse mit 804 Patient*innen aus 17 Studien bestätigt.15
„Interessant ist, dass nur wenige Therapieabbrüche erfolgt sind, und dies v.a. aufgrund von AE, nicht wegen einer Verstärkung der Grunderkrankung“, merkte Reimer dazu an.
Leitliniengemäß16–18 ist bei irAE des Grades I bis auf Myokarditis keine Kortisongabe erforderlich. Meist ist ein engmaschiges Monitoring ausreichend – ausgenommen bei Hyperthyreoiditis, Pneumonitis und Myokarditis. Bei einer Grad-II-Myokarditis ist ein Therapieabbruch indiziert. Bei allen anderen irAE des Grades II ist die Verabreichung von Kortison erforderlich. Bei Grad-III-irAE – ausgenommen bei Pneumonitis, bei der ein Therapieabbruch erfolgen muss – sind ebenso eine Kortisontherapie und ein Zuwarten bis zur Rückbildung der AE auf Grad I oder bis zu einer erforderlichen Kortisondosis von <10mg/Tag notwendig. Bei Grad-IV-irAE jeglicher Art muss ein permanenter Therapiestopp erfolgen.
Bezüglich der Prophylaxe einer ir („immune-related“) Colitis konnte in einer Arbeit des Dana-Farber Cancer Institute nachgewiesen werden, dass die prophylaktische Langzeiteinnahme von Vitamin D unter IO zu einer Reduktion des Risikos für die Entwicklung einer Colitis um 65% führte (Odds-Ratio: 35%). Die Autor*innen berichten, dass sich diese mit den entsprechenden Ergebnissen bei Colitis ulcerosa decken.19
Bezüglich Wechselwirkungen liegen die besten Daten zur Antibiotika(AB)-Gabe vor. „Wir wissen, dass sie das Microenvironment des Darmmikrobioms beeinflussen – dieses ist aber wichtig für das Ansprechen auf die IO“, erklärte Reimer. In einer rezenten Metaanalyse wurden bei Patient*innen unter AB-Therapie ein etwas kürzeres PFS und OS nachgewiesen als bei jenen, die keine AB benötigten. Dies traf im Speziellen auf Breitband-AB zu.20
Quelle:
31. Wissenschaftliche Tagung der Arbeitsgemeinschaft für Gynäkologische Onkologe. 19.–22. April 2023, Salzburg
Literatur:
1 Timmerman D et al.: Int J Gynecol Cancer 2021; 31: 961-82 2 Imterat M et al.: Imterat Int J Gynecol Cancer 2022 3 Trimbos JB: Int J Gynecol Cancer 2000; 10: 8-11 4 Minig L et al.: Surg Oncol 2017; 24: 2720-6 5 Myuldermans K et al.: Eur J Cancer 2013; 49: 1600-8 6 Oseledchyk A et al.: Ann Oncol 2017; 28: 2985-93 7 Shu CA et al.: Gynec Oncol 2015; 139: 236-41 8 Johnston SRD et al.: J. Clin Oncol 2020; 38: 3987-98 9 Cancer Genome Atlas Network. Nature 2012; 490: 61-70 10 André F et al.: N Engl J Med 2019; 380: 1929-40 11 Fachinformation Alpelisib, Stand: Februar 2023 12 Rugo HS et al.: Breast 2022; 61: 156-67 13 Oliveira M et al.: SABCS 2022; Abstract #GS3-02 14 Abdel Wahab N et al.: Ann Intern Med 2018; 168: 121-30 15 Tang H et al.: Front Oncol 2021 16 Haanen J et al.: Ann Oncol 2022; 33: 1217-38 (ESMO) 17 Brahmer JR et al.: J Immunother Cancer2021 18 Schneider BJ et al.: J Clin Oncol 2021; 39: 4073-126 (ASCO) 19 Grover S et al.: Cancer 2020; 126: 3758-67 20 Jiang S et al.: Front Oncol 2022; online unter doi.org/10.3389/fonc.2022.823705
Das könnte Sie auch interessieren:
Adjuvantes Osimertinib reduziert ZNS-Rezidive bei EGFR-mutierter Erkrankung
Etwa 30% der Patienten mit nicht kleinzelligem Lungenkarzinom (NSCLC) präsentieren sich mit resezierbarer Erkrankung und werden einer kurativen Operation unterzogen. Viele Patienten ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...