Neue Standards bei kolorektalen Karzinomen
Autoren:
Dr. Suman Vangala
Prof. Dr. Dirk Behringer1
Hämatologie, Onkologie & Palliativmedizin
Augusta Kliniken Bochum Hattingen
1 Korrespondenzautor
E-Mail: d.behringer@augusta-bochum.de
Rezente Studien haben die Therapie kolorektaler Karzinome (CRC) vorangebracht: Multimodale kurative Therapiekonzepte ermöglichen den Organerhalt als Behandlungsziel beim Rektumkarzinom; maßgeschneiderte, auf die Tumoreigenschaften zugeschnittene systemische Therapien gewinnen an Bedeutung.
Keypoints
-
Beim lokal fortgeschrittenen Rektumkarzinom führt die totale neoadjuvante Therapie (TNT) zu einem signifikant verlängerten Langzeitüberleben und eröffnet die Möglichkeit eines Organerhalts ohne Operation.
-
Beim fortgeschrittenen BRAF-mutierten kolorektalen Karzinom bleibt Bevacizumab in Kombination mit Chemotherapie der Erstlinienstandard, in der Zweitlinie steht der BRAF-Inhibitor Encorafenib in Kombination mit Cetuximab zur Verfügung.
-
Eine Immuntherapie mit dem PD-1-Inhibitor Pembrolizumab ist beim mikrosatelliteninstabilen fortgeschrittenen kolorektalen Karzinom der neue Erstlinienstandard mit signifikant verlängertem Gesamtüberleben und deutlich reduziertem Nebenwirkungsspektrum.
Epidemiologie
Trotz einer fallenden Inzidenz und Mortalität über alle Altersgruppen ist seit den 90er-Jahren eine Zunahme der CRC-Erkrankungshäufigkeit bei den unter 50-Jährigen („early onset colorectal cancer“) zu verzeichnen.1 Bei dieser jüngeren Altersgruppe sind im Vergleich zur älteren folgende Punkte wichtig:
-
Die gastrointestinalen Nebenwirkungen unter Chemotherapie stehen gegenüber den hämatologischen Nebenwirkungen im Vordergrund; gleichwohl komplettieren mehr jüngere Patienten die adjuvante Therapie.
-
In der Hochrisikogruppe im Stadium III (T4 und/oder N2) ist das Rezidiv- und Sterberisiko bei den Jüngeren höher als bei den Älteren (um 26% bzw. 19%).2
-
Themen wie sexuelle Gesundheit (Infertilitätsrisiko), finanzielle und berufliche Einschränkungen werden zu selten angesprochen und sind in den Leitlinien nicht ausreichend berücksichtigt.
Besonderheit Rektumkarzinom – Kuration und lokale Kontrolle
Für die erfolgreiche Behandlung des Rektumkarzinoms steht neben dem kurativen Ziel die Lokalkontrolle mit Erhalt einer hohen funktionellen Lebensqualität im Vordergrund. Dabei geht die verbesserte Lokalkontrolle nicht immer einher mit einem verlängerten metastasenfreien Überleben. Mit dem bisherigen Therapiestandard einer präoperativen Therapie (simultane Radiochemotherapie oder Kurzzeitbestrahlung) werden Lokalrezidivraten ≤5% erzielt.3
Die totale neoadjuvante Therapie in drei großen Studien
Drei große Studien aus dem Jahr 2020 (RAPIDO, PRODIGE 23, OPRA) haben eine alternative Therapiestrategie untersucht: die totale neoadjuvante Therapie (TNT). Hierbei wird die neoadjuvante Radio(chemo)therapie ergänzt durch eine mehrmonatige Chemotherapie (Pyrimidinanalogon und Oxaliplatin) noch vor der Operation.
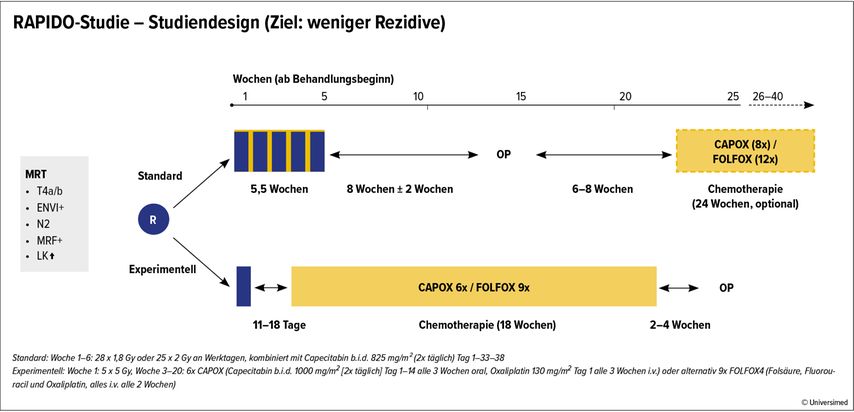
Die RAPIDO-Studie verglich die Standardtherapie (5 Wochen Radiochemotherapie – OP – optional adjuvante Chemotherapie) mit einer TNT bestehend aus 5x 5Gy Bestrahlung und 18-wöchiger Chemotherapie (CAPOX/FOLFOX) mit anschließender Operation (Abb. 1). Hierbei zeigte der neue Ansatz einen deutlich höheren Anteil an pathologischen Komplettremissionen (28 vs. 14%) sowie eine signifikante Senkung der Rezidivrate mit distanten Metastasen um 7%.4 Mit einem krankheitsfreien Überleben von ≥75% in allen drei Studien zeigt sich durch die TNT eine Verbesserung im Vergleich zur bisherigen Standardtherapie.
Abb. 1: Therapieprotokoll der RAPIDO-Studie als Beispiel der totalen neoadjuvanten Therapie („experimentell“) gegenüber der klassischen präoperativen kombinierten Radiochemotherapie, Operation und optional adjuvante Chemotherapie. MRF, Mesorektale Faszie. Modifiziert nach 4
Verzicht auf Operation möglich?
Die OPRA-Studie stellte die Frage, inwieweit die Abfolge der Therapieblöcke einer TNT (kombinierte Radiochemotherapie gefolgt von Chemotherapie [Konsolidierung] oder umgekehrt [Induktion]) den Verzicht auf eine Operation ermöglicht. In einer standardisierten Verlaufskontrolle nach TNT beurteilten die Untersucher mittels endoskopischer und digital-rektaler Einschätzung und Verzicht auf Biopsien das Therapieergebnis im Verlauf und entschieden über das weitere Vorgehen: Beobachtung bei komplettem Ansprechen, Operation bei inkomplettem Ansprechen, in der Gruppe „nahezu komplette Remission“ entschied der Untersucher über das weitere Vorgehen (Abb. 2).
Ein Organerhalt nach 3 Jahren wurde bei 78% der Patienten mit Komplettremissionen und bei 45% der nahezu kompletten Remissionen dokumentiert. Weitere Endpunkte wie das krankheitsfreie Überleben und die Metastasenfreiheit waren ebenso im Vergleich zu historischen Kontrollen verbessert. Die Möglichkeit zum organerhaltenden Vorgehen war bei Patienten mit Radiochemotherapie gefolgt von Chemotherapie signifikant häufiger im Vergleich zu einer der kombinierten Radiochemotherapie vorgeschalteten Chemotherapie.5
Die TNT kann aufgrund dieser Ergebnisse und der Empfehlungen der Fachgesellschaften als neue Standardtherapie des lokal fortgeschrittenen Rektumkarzinoms betrachtet werden; dabei sollte, insbesondere mit dem Ziel der Erhöhung der Rate an klinischen Komplettremissionen und Option auf Organerhalt, die Konsolidierungstherapie bevorzugt werden.
Ein Watch-&-Wait-Konzept soll konsequent im Tumorboard diskutiert und in enger Abstimmung mit dem Patienten erfolgen. Bei Nichterreichen einer Komplettremission sollte die Operation genauso erfolgen wie sie auch im Rahmen der Standardtherapie durchgeführt worden wäre. Kontrollintervalle sollen außerhalb von Studien während des ersten Jahres im 4-Monats-Intervall (digital-rektale Untersuchung, Endoskopie und Magnetresonanztomografie [MRT]) und in den Jahren 2–5 alle 6 Monate durchgeführt werden.
Für die Beratung der Patienten mit Rektumkarzinom sollten das Ziel eines Organerhalts und die Folgen früh thematisiert und in das therapeutische Konzept einbezogen werden.6
Therapie des fortgeschrittenen kolorektalen Karzinoms
Für die Therapie der lokal nicht behandelbaren fortgeschrittenen kolorektalen Karzinome hat sich die detaillierte prätherapeutische gewebliche Analyse von Biomarkern als unverzichtbar für die Wahl geeigneter Therapien etabliert; dazu gehören neben KRAS und NRAS die Untersuchung auf BRAF und Mikrosatelliteninstabilität (MSI).
BRAF-Mutation
Die BRAF-Mutation geht mit einer deutlich reduzierten Gesamtüberlebenszeit von 18 Monaten gegenüber 30 Monaten beim BRAF-Wildtyp einher. Eine intensive Chemotherapie (FOLFOXIRI) in Kombination mit dem Angiogenesehemmer Bevacizumab gilt als Standard.
In der FIRE4.5-Studie wurde diese Kombination mit dem Einsatz des EGFR(epidermaler Wachstumsfaktor-Rezeptor)-Antikörpers Cetuximab erstmals prospektiv überprüft. Hierbei ergab sich ein signifikant verlängertes progressionsfreies Überleben in der Bevacizumab-Gruppe bei vergleichbarem Gesamtüberleben, dies bestätigte den bisherigen Standard.
Vor dem Hintergrund dieser ernüchternden Therapieergebnisse wird in der Breakwater-Studie die bislang in der Zweitlinie zugelassene Kombination von Cetuximab mit dem BRAF-Inhibitor Encorafinib bei therapienaiven Patienten mit der Hinzunahme einer Chemotherapie (FOLFOX/FOLFIRI) prospektiv verglichen.
Immuntherapie: neuer Standard
Die KEYNOTE-117-Studie konnte bei Patienten im fortgeschrittenen Stadium mit Mikrosatelliteninstabilität (MSI-H) in der Erstlinie durch den PD-1(„programmed cell death protein 1“)-Inhibitor Pembrolizumab im Vergleich zur Standardchemotherapie (5-FU-basiert +/– EGFR-Antikörper) ein signifikant verlängertes progressionsfreies (42 vs. 11% nach 36 Monaten) sowie Gesamtüberleben (61 vs. 50% nach 36 Monaten) erreichen. Die Häufigkeit schwerer Nebenwirkungen war unter Pembrolizumab deutlich geringer als im Chemotherapiearm.7 Eine Pembrolizumab-Monotherapie gilt somit als Therapiestandard in der Erstlinie des MSI-H kolorektalen Karzinoms.
Für die Zweitlinientherapie konnte basierend auf der CheckMate-142-Studie eine Empfehlung als Therapieoption für die Kombination aus Nivolimab und Ipilimumab ausgesprochen werden. Hierbei wurden im Rahmen einer offenen Kohortenstudie MSI-H-Patienten mit mindestens einer Vortherapie eingeschlossen; die Gesamtüberlebensrate lag bei 70,5% nach 52 Monaten, das mediane Überleben war zuletzt noch nicht erreicht. Ein Vergleich mit Daten aus der Flatiron-Datenbank ergab ein signifikant verlängertes Gesamtüberleben.8 Ob die Kombination von Nivolumab mit Ipilimumab in der Erstlinie vorteilhaft ist, wird derzeit überprüft.
Literatur:
1 Siegel RL et al.: Colorectal cancer statistics. CA Cancer J Clin 2020; 70(3): 145-64 2 Fontana E et al.: Early-onset stage II/III colorectal adenocarcinoma in the IDEA database: Treatment adherence, toxicities, and outcomes from adjuvant fluoropyrimidine and oxaliplatin. J Clin Oncol 2021; 39(15_suppl): 3517 3 Guren M et al.: Nationwide improvement of rectal cancer treatment outcomes in Norway, 1993–2010. Acta Oncologica 2015; 54(10): 1714-22 4Hospers G et al.: Short-course radiotherapy followed by chemotherapy before TME in locally advanced rectal cancer: The randomized RAPIDO trial. J Clin Oncol 2020; 38(15_suppl): 4006 5 Thompson H et al.: Survival and organ preservation according to clinical response after total neoadjuvant therapy in locally advanced rectal cancer patients: A secondary analysis from the organ preservation in rectal adenocarcinoma (OPRA) trial. J Clin Oncol 2021; 39(15_suppl): 3509 6 AIO, ACO und ARO: Konsentierte Stellungnahme der ACO, der AIO und der ARO zum „Watch and wait“-Konzept mit intendiertem Organerhalt bei Rektumkarzinomen des mittleren und unteren Drittels. 2020. Online unter www.aio-portal.de. Abgerufen am 10.03.22 7 André T et al.: Pembrolizumab in microsatellite-instability-high advanced colorectal cancer. N Engl J Med 2020; 383(23): 2207-18 8 DGHO: Stellungnahme zur Nutzenbewertung gemäß § 35a SGB V Nivolumab (neues Anwendungsgebiet: metastasiertes kolorektales Karzinom, dMMR oder MSI-H, vorbehandelte Patient*innen, Kombination mit Ipilimumab). Vorgangsnummer 2021-08-01-D-717. IQWiG Bericht Nr. 1230. 1. November 2021. Online unter www.dgho.de. Abgerufen am 10.03.22
Das könnte Sie auch interessieren:
Adjuvantes Osimertinib reduziert ZNS-Rezidive bei EGFR-mutierter Erkrankung
Etwa 30% der Patienten mit nicht kleinzelligem Lungenkarzinom (NSCLC) präsentieren sich mit resezierbarer Erkrankung und werden einer kurativen Operation unterzogen. Viele Patienten ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...