Neue Daten zum nicht kleinzelligen Bronchialkarzinom
Bericht:
Dr. Kassandra Settele
Review von:
OA Dr. Maximilian Hochmair
Leiter der pneumo-onkologischen Ambulanz + Tagesklinik
Abteilung für Innere Medizin und Pneumologie
Karl-Landsteiner-Institut für Lungenforschung und pneumologische Onkologie
Klinik Floridsdorf, Wien
Wie üblich wurden beim Jahreskongress der American Society of Clinical Oncology (ASCO), auch im Vergleich zu anderen Kongressen, sehr viele Studien zum Lungenkarzinom vorgestellt. Darunter fanden sich einige hochinteressante Ergebnisse. ImFolgenden finden Sie eine Zusammenfassung der wichtigsten Highlights.
Frühstadium
IMpower010
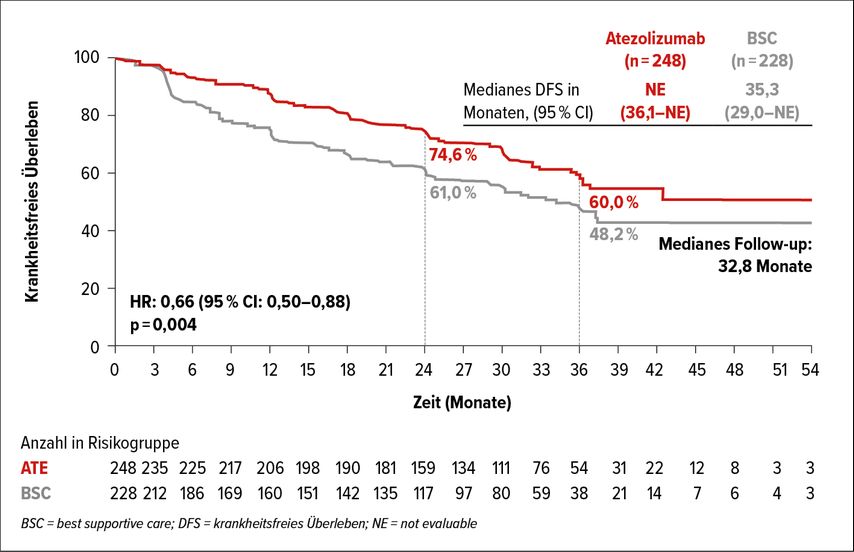
Was das nicht kleinzellige Bronchialkarzinom (NSCLC) im Frühstadium betrifft, war die IMpower010-Studie das größte Highlight des diesjährigen ASCO-Kongresses. Die randomisierte Phase-III-Studie untersuchte die adjuvante Gabe des PD-L1-Inhibitors Atezolizumab gegen „best supportive care“ nach adjuvanter Chemotherapie bei über 1000 Patienten mit komplett reseziertem NSCLC im Stadium IB–IIIA. Primärer Endpunkt war das krankheitsfreie Überleben (DFS), welches hierarchisch zunächst in der PD-L1-positiven Subgruppe im Stadium II–IIIA getestet wurde. Diesbezüglich zeigte sich nach einem medianen Follow-up von 32,8 Monaten ein klar positives Ergebnis mit einer Hazard-Ratio von 0,66 für Atezolizumab (Abb. 1). Die HR für alle randomisierten Patienten im Stadium II–IIIA lag etwas höher, bei 0,79, während sich in der Intention-to-treat-Population keine klare statistische Signifikanz abzeichnete. Die Daten zum Gesamtüberleben (OS) sind zum aktuellen Zeitpunkt noch nicht reif, wobei es auch hier einen Trend zu einem verlängerten OS in der PD-L1-positiven Gruppe gibt.
Abb. 1: Krankheitsfreies Überleben in der PD-L1-positiven Subpopulation im Stadium II–IIIA in der IMPOWER010-Studie (nach Wakelee et al.)1
In der Subgruppenanalyse wurde gezeigt, dass der Benefit von Atezolizumab bei hoher PD-L1-Expression besonders hoch war. In der Studie wurden keine neuen unerwünschten Wirkungen berichtet. Aufgrund der positiven Ergebnisse in Hinblick auf die PD-L1-positive Subgruppe ist davon auszugehen, dass die Immuntherapie in Zukunft im adjuvanten Setting einen deutlichen Stellenwert haben wird.1
CheckMate 816
Zur CheckMate-816-Studie, die bereits beim AACR-Meeting präsentiert wurde, gab es beim ASCO-Kongress ein Update. In dieser randomisierten Phase-III-Studie wird die neoadjuvante Gabe von Nivolumab zusätzlich zur Chemotherapie untersucht. Beim AACR-Meeting wurden bereits die positiven Effektivitätsdaten hinsichtlich pathologisch kompletter Remission (pCR) mit einer Rate von 24,0% vs. 2,2% und hinsichtlich des pathologischen Ansprechens (36,9% vs. 8,9%) im Vergleich zur Chemotherapie alleine präsentiert.
Nun wurden die chirurgischen Outcomes vorgestellt: Mehr Patienten in der Nivolumab-Gruppe wurden tatsächlich operiert (83% vs. 75%) und auch die Tiefe des Ansprechens war unter der Kombination mit Nivolumab besser. Thorakotomien wurden in der Gruppe, die lediglich mit Chemotherapie behandelt worden war, häufiger durchgeführt (59% vs. 63%) und ein Wechsel von einer minimal invasiven Operation zur offenen Operation fand in dieser Gruppe häufiger statt (11 vs. 16%). Ein wichtiger Gesichtspunkt ist auch die Häufigkeit von Pneumonektomien, die wiederum in dieser Gruppe vermehrt vorkamen (17% vs. 25%). Die Nivolumab-Gruppe wies hingegen einen höheren Anteil an R0-Resektionen auf (83% vs. 78%). Kein Unterschied fand sich jedoch bezüglich der Aufenthaltsdauer im Spital. Wenn man die Lebensqualität der Patienten 90 Tage nach Operation betrachtet, kam es in der Nivolumab-Gruppe seltener zu Schmerzen (8% vs. 16%), was vermutlich an der geringeren Rate an offenen Operationen liegt.2
ctDNA kann Rezidiv voraussagen
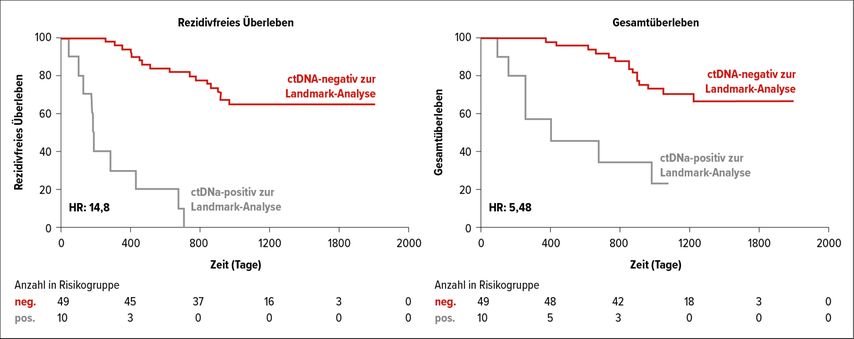
Eine weitere Studie untersuchte die Wertigkeit von zirkulierender Tumor-DNA (ctDNA) im Monitoring beim NSCLC im Frühstadium. U.a. wurde ein Patientenbeispiel vorgestellt, bei dem das Wiederauftreten der Erkrankung anhand von ctDNA bereits 174 Tagen nach Operation gesehen wurde, das Wiederauftreten jedoch erst nach 398 Tagen festgestellt werden konnte. Bei allen Patienten, bei denen ctDNA detektiert wurde, kam es während der Studie zum Krankheitsprogress. Die Detektion von ctDNA war assoziiert mit einem kürzeren rezidivfreien Überleben (RFS) und OS (Abb. 2). Die ctDNA könnte in diesem Sinne voraussagen, welche Patienten eine stärkere adjuvante Therapie benötigen werden.3
Abb. 2: Die Detektion von ctDNA ist assoziiert mit einem kürzeren rezidivfreien Überleben und Gesamtüberleben (nach Gale et al.)3
5-Jahres-Update der PACIFIC-Studie
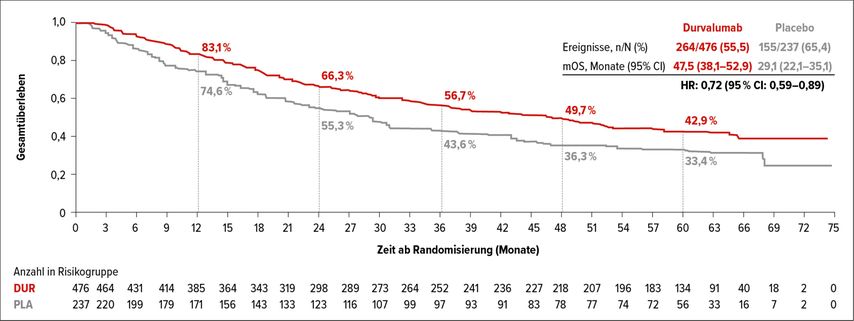
Das Update der PACIFIC-Studie war ein weiteres großes Highlight des diesjährigen ASCO-Kongresses. Hierbei handelt es sich um eine randomisierte, placebokontrollierte Phase-III-Studie, in der die Gabe von Durvalumab bei Patienten mit nicht resezierbarem NSCLC im Stadium III nach einer platinbasierten Chemotherapie überprüft wurde. Die Rate des 5-Jahres-OS betrug 42,9% unter Durvalumab vs. 33,4% unter Placebo mit einer HR von 0,72 (Abb.3). Auch die 5-Jahres-Rate in Hinblick auf das progressionsfreie Überleben (PFS) war unter Durvalumab höher: 33,1% vs. 19,0%. Mit diesen Ergebnissen wurde Durvalumab als Goldstandard im Anschluss an eine Chemoradiotherapie klar bestätigt.4
Zielgerichtete Therapien
Kombinationstherapie Amivantamab/Lazertinib
Amivantamab ist ein bispezifischer, monoklonaler Antikörper, der sowohl an den EGFR-Rezeptor als auch an MET bindet. Bei Lazertinib handelt es sich um einen Tyrosinkinase-Inhibitor (TKI) der dritten Generation. Man geht davon aus, dass diese Wirkstoffkombination nach Versagen von Osimertinib besonders wirksam ist: Beim Versagen von Osimertinib kommt es zu verschiedenen Resistenzen, bei denen sowohl EGFR als auch MET eine entscheidende Rolle spielen. In die Studie eingeschlossen waren 45 Patienten, mit metastasiertem/nicht resezierbarem NSCLC und EGFR-Exon-19-Deletion oder L858R-Mutation, die nach Gabe von Osimertinib progredient waren. Das mediane PFS betrug 4,9 Monate und die allgemeine Ansprechrate (ORR) 36%, wobei die mediane Dauer des Ansprechens (DOR) bei 9,6 Monaten lag. Bei jenen Patienten, bei denen eine EGFR-/MET-basierte Resistenz identifiziert werden konnte, lag die Ansprechrate etwas höher. Die Testung von MET spielt dabei eine besondere Rolle: Bei einer MET-basierten Resistenz lag die Ansprechrate bei 75%. Möglicherweise lässt sich die Suszeptibilität mittels immunhistochemischer Färbung festmachen. In der Studie sprachen neun von zehn Patienten, die immunhistochemisch positiv für eine EGFR/MET-Expression waren, auf die Kombinationstherapie an.5
Patritumab-Deruxtecan
Das Antikörper-Wirkstoff-Konjugat Patritumab-Deruxtecan wird ebenfalls bei Patienten nach Versagen von Osimertinib getestet. Patritumab-Deruxtecan bindet an HER3, welches bei 83% der NSCLC exprimiert wird. Der primäre Endpunkt dieser Phase-I-Dosiseskalations-Studie war die ORR nach RECIST 1.1, sekundäre Endpunkte beinhalteten DOR, PFS und Sicherheit. Der Großteil der eingeschlossenen Patienten war auf die Gabe von Osimertinib progredient, die übrigen Patienten hatten zuvor andere TKI erhalten. Die ORR betrug sowohl unter Vortherapie mit Osimertinib als auch unter Vortherapie mit anderen TKI 39%. Das mediane PFS lag jeweils bei 8,2 Monaten und die DOR bei 7,0 Monaten bei Osimertinib-Vorbehandlung bzw. 6,9 Monaten bei Vorbehandlung mit anderen TKI. Die Substanzkombination zeigte unabhängig vom Resistenzmechanismus und auch bei Vorliegen von Hirnmetastasen Wirkung. Das Nebenwirkungsprofil mit vorrangig Thombozytopenie, Neutropenie und Fatigue ist bereits bekannt. Patritumab-Deruxtecan wird im Rahmen von Phase-II-Studien weiter untersucht.6
CodeBreaK100
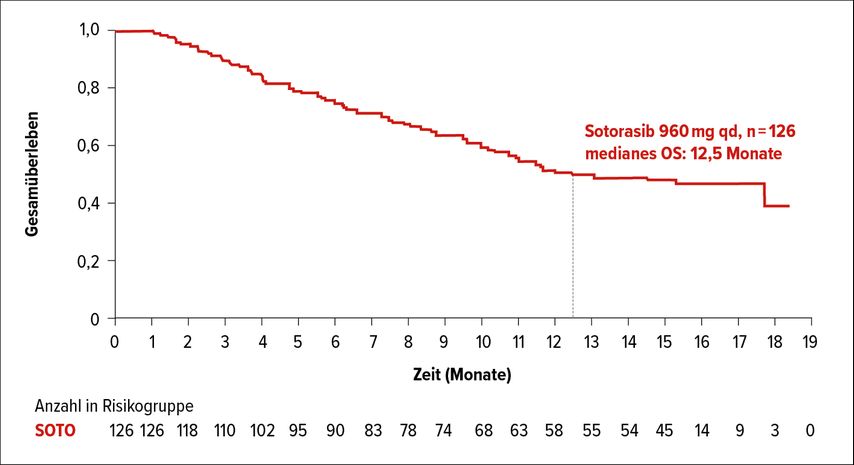
Zur CodeBreaK100-Studie, die Sotorasib untersucht, gab es ein Update zum OS und zur Subgruppenanalyse. Eingeschlossen waren 136 vortherapierte Patienten mit KRASG12C-Mutation. Die ORR lag bei 37,1%, mit einer Krankheitskontrollrate von 80,6%. In dieser Patientenpopulation mit schlechter Prognose betrug das mediane PFS 6,8 Monate und das mediane OS 12,5 Monate (Abb. 4). Es zeigten sich keine neuen unerwünschten Wirkungen, mehrheitlich kam es zu gastrointestinalen Beschwerden. Sotorasib ist insgesamt eine gut verträgliche Substanz.
In der Subgruppenanalyse zeigte sich, dass Patienten mit vorangegangener Anti-PD-(L)1-Therapie, aber ohne Platin-basierte Chemotherapie ein besonders gutes Ansprechen und langes medianes OS aufwiesen. Alle untersuchten Subgruppen profitierten von der Therapie mit Sotorasib. Die einzige Gruppe, die zwar prinzipiell profitierte, aber etwas schlechter abschnitt, war die Subgruppe der STK11- und KEAP1-Mutationen.7 Die Substanz ist im NPU-Programm oder im Rahmen einer Studie in Wien, Graz und Krems derzeit verfügbar.
(Chemo-)Immuntherapien imStadium IV
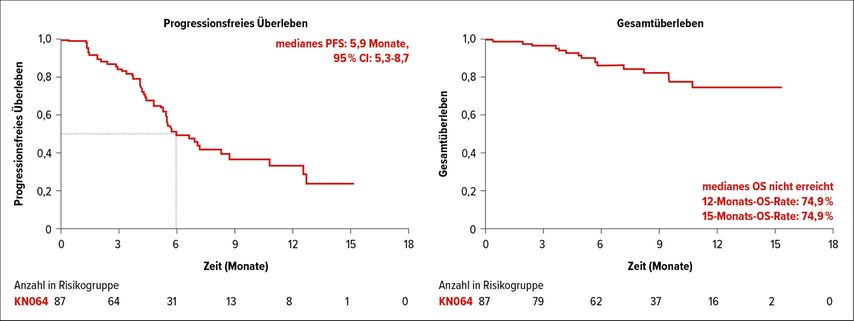
KN046
KN064 ist ein neuer bispezifischer Antikörper gegen PD-1 und CTLA-4 mit guter Verträglichkeit. Seine Effektivität in Kombination mit Chemotherapie wurde im Rahmen einer Phase-II-Studie evaluiert. Sowohl bei Plattenepithel- als auch bei Nicht-Plattenepithel-NSCLC konnte die Kombination eine gute Effektivität zeigen. Die ORR lag insgesamt bei 50,6% und die Krankheitskontrollrate bei 87,7%. Das mediane PFS betrug 5,9 Monate und das mediane OS war noch nicht erreicht (Abb. 5).8
CheckMate 9LA
Zur CheckMate-9LA-Studie wurde das 2-Jahres-Update präsentiert. Die Studie vergleicht Nivolumab plus Ipilimumab plus zwei Zyklen Chemotherapie mit vier Zyklen Chemotherapie alleine. In Bezug auf das OS zeigt sich auch nach zwei Jahren weiterhin ein Vorteil für die Dreifachkombination mit einer 2-Jahres-Rate von 38% vs. 26%. Die HR lag bei 0,72. Auch die Zwei-Jahres-PFS-Rate war höher mit 20% vs. 8%. Ein anhaltendes Ansprechen wiesen nach zwei Jahren 34% vs. 12% der Patienten auf. Die Subgruppenanalyse legt nahe, dass besonders Patienten mit einem Plattenepithelkarzinom von der Therapie profitieren. Bei positiver PD-L1-Expression zeigte sich eine ähnliche Wirksamkeit wie bei den Patienten ohne PD-L1-Expression. Interessanterweise wiesen 56% der Patienten, die die Therapie aufgrund unerwünschter Wirkungen abbrechen mussten, ein Jahr nach Therapieabbruch weiterhin ein Ansprechen auf.9
Immunvermittelte unerwünschte Wirkungen
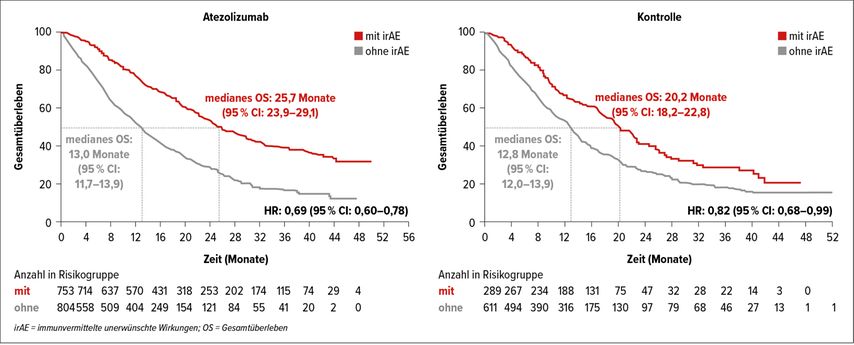
Eine gepoolte Analyse untersuchte immunvermittelte unerwünschte Wirkungen und Wirksamkeit in den Studien IMpower130, IMpower132 und IMpower150. Alle diese Studien hatten die Kombination Atezolizumab + Chemotherapie getestet. Es zeigte sich, dass Patienten, bei denen es zu immunvermittelten unerwünschten Wirkungen kam, ein längeres Gesamtüberleben aufwiesen – sowohl im Atezolizumab beinhaltenden Arm als auch im Chemotherapie-Arm (Abb. 6). Auch die Ansprechrate war in dieser Patientengruppe höher. Trotzdem profitierten Patienten von der Therapie mit Atezolizumab, unabhängig davon, ob es zu unerwünschten Wirkungen kam oder nicht.10
Abb. 6: Immunvermittelte unerwünschte Nebenwirkungen und Gesamtüberleben unter Therapie mit Atezolizumab plus Chemotherapie bzw. Chemotherapie alleine (nach Socinski et al.)10
Akkermansia muciniphila
Abseits der typischen Studien, die sich auf Wirkstoffe konzentrieren, gab es in diesem Jahr auch eine Untersuchung zum Mikrobiom. In dieser Studie wurde der Zusammenhang zwischen dem Vorkommen von Akkermansia munciniphila im Stuhl und der ORR bzw. dem OS analysiert, um die prognostische Signifikanz dieses Darmkeims beim fortgeschrittenen NSCLC validieren zu können. Es konnte klar gezeigt werden, dass das Vorkommen von Akkermansia muciniphila mit einer höheren ORR (27% vs. 17%) und einer höheren Rate des 12-Monats-OS (57% vs. 42%) korrelierte. In Zukunft sollte man prospektiv untersuchen, ob die Gabe dieses Keims ähnliche Benefits bringt.11
VARGADO: Kohorte C
Die Auswertung von Kohorte C der VARGADO-Studie wurde bereits mit Spannung erwartet. Kohorte C analysierte diejenige Patientengruppe, die in der Erstlinie Chemotherapie plus Immuncheckpoint-Inhibitoren erhalten hatte und in der Zweitlinie die Kombination Nintedanib plus Docetaxel. Das mediane PFS lag bei 4,4 Monaten und bestätigte die Gabe der Wirkstoffkombination in dieser Situation.12
Literatur:
1 Wakelee et al.: IMpower010: Primary results of a phase III global study of atezolizumab versus best supportive care after adjuvant chemotherapy in resected stage IB-IIIA non-small cell lung cancer (NSCLC). ASCO 2021, Abstr. #8500 2 Spicer et al.: Surgical outcomes from the phase 3 CheckMate 816 trial: Nivolumab (NIVO) + platinum-doublet chemotherapy (chemo) vs chemo alone as neoadjuvant treatment for patients with resectable non-small cell lung cancer (NSCLC). ASCO 2021, Abstr. #8503 3 Gale D et al.: Residual ctDNA after treatment predicts early relapse in patients with early-stage NSCLC. ASCO 2021, Abstr. #8517 4 Spigel et al.: Five-year survival outcomes with durvalumab after chemoradiotherapy in unresectable stage III NSCLC: An update from the PACIFIC trial. ASCO 2021, Abstr. #8511 5 Bauml J et al.: Amivantamab in combination with lazertinib for the treatment of osimertinib-relapsed, chemotherapy-naïve EGFR mutant (EGFRm) non-small cell lung cancer (NSCLC) and potential biomarkers for response. ASCO 2021, Abstr. #9006 6 Janne PA et al.: Efficacy and safety of patritumab deruxtecan (HER3-DXd) in EGFR inhibitor-resistant, EGFR-mutated (EGFRm) non-small cell lung cancer (NSCLC). ASCO 2021, Abstr. #9007 7 Skoulidis F et al.: Overall survival and exploratory subgroup analyses from the phase 2 CodeBreaK 100 trial evaluating sotorasib in pretreated KRAS p.G12C mutated non-small cell lung cancer. ASCO 2021, Abstr. #9003 8 Yang Y et al.: A phase 2, open-label, multicenter study to evaluate the efficacy, safety, and tolerability of KN046 in combination with chemotherapy in subjects with advanced non-small cell lung cancer. ASCO 2021, Abstr. #9060 9 Reck et al.: First-line nivolumab (NIVO) plus ipilimumab (IPI) plus two cycles of chemotherapy (chemo) versus chemo alone (4 cycles) in patients with advanced non-small cell lung cancer (NSCLC): Two-year update from CheckMate 9LA. ASCO 2021, Abstr. #9000 10 Socinski et al.: Pooled analyses of immune-related adverse events (irAEs) and efficacy from the phase 3 trials IMpower130, IMpower132, and IMpower150. ASCO 2021, Abstr. #9002 11 Derosa L et al.: Intestinal Akkermansia muciniphila predicts overall survival in advanced non-small cell lung cancer patients treated with anti-PD-1 antibodies: Results a phase II study. ASCO 2021, Abstr. #9019 12 Grohé C et al.: Second-line nintedanib plus docetaxel for patients with lung adenocarcinoma after failure on first-line immune checkpoint inhibitor combination therapy: Initial efficacy and safety results from VARGADO Cohort C. ASCO 2021, Abstr. #9033
Das könnte Sie auch interessieren:
Adjuvantes Osimertinib reduziert ZNS-Rezidive bei EGFR-mutierter Erkrankung
Etwa 30% der Patienten mit nicht kleinzelligem Lungenkarzinom (NSCLC) präsentieren sich mit resezierbarer Erkrankung und werden einer kurativen Operation unterzogen. Viele Patienten ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...