Innovative Behandlung primärer und sekundärer Lebertumoren
Autoren:
Dr. med. Christoph Kümmerli1
PD Dr. med. Philip C. Müller1
Prof. Dr. med. Philipp Dutkowski1
Prof. Dr. med. Dieter Köberle2
OA Dr. med. Ernesto Olcina Aguado2
Prof. Dr. med. Adrian T. Billeter, PhD1
Prof. Dr. med. Beat P. Müller1
1 Viszeralchirurgie, Clarunis Universitäres Bauchzentrum Basel, Universitätsspital und St.Claraspital Basel
2 Onkologie, St. Claraspital, Basel, Schweiz
Korrespondenz:
E-Mail: beat.mueller@clarunis.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die intraarterielle Chemotherapie stellt eine effektive Erweiterung des Behandlungsspektrums bei fortgeschrittenen primären und sekundären Lebermalignomen dar. Durch die lokale Chemotherapie können hohe Dosen mit geringer systemischer Wirkung verabreicht werden. Primär inoperable Lebertumoren und Metastasen können damit teilweise kurativ behandelt werden. Die erzielten Ergebnisse erlauben eine lokale Kontrolle oder gar eine Reduktion der Tumormasse, sodass eine kurative Resektion möglich wird.
Keypoints
-
Intraarterielle Chemotherapie ist ein Instrument der multimodalen Therapie von primären und sekundären Lebermalignomen. Diese ermöglicht eine hoch dosierte Chemotherapie bei gleichzeitig geringer systemischer Wirkung.
-
Für nichtresektable kolorektale Lebermetastasen ist das Ziel die Konversion zu resektabler Tumormasse. Die Ansprechraten nach intraarterieller Chemotherapie liegen bei 40–76%. Damit geht eine sekundäre Resektabilität von bis zu 50% einher. Die intraarterielle Chemotherapie erfolgt in Kombination mit systemischer Chemotherapie.
-
Für das hepatozelluläre und cholangiozelluläre Karzinom steht die lokale Tumorkontrolle im Vordergrund. Eine Konversion zu chirurgisch resektablen Befunden ist seltener möglich.
-
Die Chemopumpe wird mittels minimalinvasiven, roboterassistierten Verfahrens implantiert. Die Therapie sollte an hochspezialisierten viszeralonkologischen Zentren mit ausgewiesener Erfahrung in komplexer Leberchirurgie erfolgen.
Die Leber hat eine einmalige anatomische Konfiguration mit dualer Blutversorgung durch die Pfortader und die Leberarterie. Tumorenin der Leber beziehen ihre Blutversorgung vor allem durch die Leberarterie. Dies macht man sich bei der intraarteriellen Applikation von Chemotherapie zunutze. Die intraarterielle Chemotherapie wird über eine in der Bauchdecke implantierte Pumpe verabreicht. Dabei gibt ein Katheter über die Arteria gastroduodenalis (GDA) die Chemotherapie in die Leberarterie ab (Abb.1). Im Vergleich zur systemischen Chemotherapie können bei der intraarteriellen Chemotherapie bis zu 400-fach höhere Medikamentenkonzentrationen in der Leber erreicht werden. Die Metabolisierung der Chemotherapeutika in der Leber und der damit verbundene hohe First-Pass-Effekt sorgen für eine tiefe systemische Konzentration bei geringen Nebenwirkungen.
In diesem Übersichtsartikel wird auf die häufigsten Indikationen für intraarterielle Chemotherapie eingegangen:
Kolorektale Lebermetastasen
Primäre Lebertumoren
Kolorektale Karzinome stellen mit einer Inzidenz von über 1,9 Millionen Fällen die vierthäufigste Krebsart weltweit dar. Kolorektale Lebermetastasen (CRLM) sind für die onkologische Langzeitprognose ausschlaggebend. So sind bei der Diagnosestellung bereits bei 25% der Patient:innen synchrone Lebermetastasen nachweisbar und weitere 25% entwickeln später metachrone Lebermetastasen.
In der initialen Bildgebung sind nur 20–30% der Lebermetastasen resektabel und somit kurativ behandelbar. Folglich wird oft ein multimodales Therapiekonzept individuell auf die Patient:innen zugeschnitten. Dabei werden systemische und lokale Therapien eingesetzt, mit dem Ziel der Konversion in eine resektable Erkrankung. Die aktuelle systemische Therapie umfasst Chemotherapeutikakombinationen mit 5-Fluorouracil (5-FU), Leucovorin und/oder Oxaliplatin oder Irinotecan. Häufig werden diese mit Biologika kombiniert und es werden mit 70% hohe Ansprechraten erreicht. Dadurch können bis zu 40% der initial nichtresektablen CRLM in ein resektables Stadium überführt werden.
Das hepatozelluläre Karzinom (HCC) und das cholangiozelluläre Karzinom (CCC) sind primäre Lebertumoren.Mit jährlich 0,9 Millionen Neuerkrankungen sind sie seltener als CRLM. Sie werden häufig erst in einem fortgeschrittenen Stadium diagnostiziert. Gerade beim CCC, dasgenerell schwierig zu diagnostizieren und zu behandeln ist, ist eine Reduktion der Tumormasse entscheidend, um ein Downstaging in eine resektable Erkrankung zu erreichen.
Aktuelle Indikationen für die intraarterielle Chemotherapie umfassen Downstaging nichtresektabler Tumoren der Leber, die adjuvante Therapie nach Resektion von CRLMsowiedie palliative Therapie zur Tumorkontrolle. Die intraarterielle Chemotherapie wird häufig mit einer systemischen Chemotherapie kombiniert. Im Folgenden wird auf die Indikation und die aktuelle Evidenz zum Thema eingegangen.
Indikationen und Kontraindikationen
Die präoperative Aufarbeitung schliesst anatomische Faktoren und die Leberfunktion mit ein.
Arterielle Anatomie
Eine Voraussetzung für die intraarterielle Chemotherapie ist die singuläre arterielle Versorgung der Leber, ohne dass arterielle Äste von der Leberarterie in benachbarte Organe abgegeben werden oder die Leber zusätzliche arterielle Zuflüsse hat. Die GDA muss offen sein und einen adäquaten Durchmesser zur Katheterplatzierung aufweisen. Präoperativ lässt sich dies am besten mit einer hochauflösenden CT-Angiografie beurteilen.
Leberfunktion
Eine Schädigung des Leberparenchyms ist bei primären Lebertumoren häufig bereits aufgetreten und hat zur Tumorgenese beigetragen, zusätzlich muss jedoch auch eine Parenchymschädigung durch die Toxizität der Chemotherapie antizipiert werden.
Vorbestehende Lebererkrankungen und portale Hypertonie können die Morbidität bei der Platzierung der Infusionspumpe erhöhen und auch die Verträglichkeit der Chemotherapie verringern, was wiederum den Therapieeffekt beeinflusst. Derzeit gibt es jedoch keine evidenzbasierten Grenzwerte, unterhalb deren die Leberfunktion für eine intraarterielle Chemotherapie als unzureichend angesehen wird. Intraarterielle Chemotherapie bei Patient:innen mit Child-Pugh-A-Lebererkrankung hat sich als sicher erwiesen und kann bei Patient:innen mit Child-Pugh-B-Zirrhose möglicherweise eine weniger toxische Behandlungsoption bieten als eine systemische Monotherapie.
Kolorektale Lebermetastasen
Kombination intraarterieller mit systemischer Chemotherapie
Evidenzlevel 2a
Die alleinige Anwendung der intraarteriellen Chemotherapie ohne systemische Therapie wurde aufgrund des Risikos des extrahepatischen Tumorprogresses und dadurch begrenzten Nutzens aufgegeben. Die Bedeutung der Systemtherapie für die Resektabilität von CRLM wurde von Lam et al. in einer randomisierten Studie hervorgehoben. Die Ansprechrate lag bei 64%, von denen 23% eine kurative Resektion erhielten.1
Eine mit intraarterieller Chemotherapie kombinierte Systemtherapie zur Verbesserung der Ansprechrate und des progressionsfreien Überlebens ist ein attraktiver Behandlungsansatz, um den Downstaging-Effekt weiter zu erhöhen. Die erste Studie, die intraarterielle Chemotherapie in Kombination mit Systemtherapie beschreibt, wurde 1989 von Safi et al. als Phase-I-Studie veröffentlicht. Hier wurde der Einsatz von Floxuridin (auch bekannt als FUDR), das zu 5-Fluorouracil verstoffwechselt wird, mit Floxuridin in Kombination mit Systemtherapie verglichen, jedoch ohne signifikanten Unterschied mit Ansprechraten von jeweils 50%.2 Während der 36-monatigen Nachbeobachtungszeit zeigte sich in keiner der beiden Gruppen eine Erhöhung der Überlebenswahrscheinlichkeit, jedoch verlängerte sich die Überlebenszeit in einer Subgruppe, die auf intraarterielle Chemotherapie ansprach.
Die aktuell höchste Evidenz und meiste Erfahrung stammen von einer grossen Kohorte des Memorial Sloan Kettering Cancer Center (MSKCC) in New York.
Eine Phase-II-Studie, in der intraarterielle Chemotherapie mit Systemtherapie kombiniert wurde, ergab, dass die gemeinsame Gabe sicher und wirksam ist. D’Angelica et al. kombinierten Floxuridin mit der besten Systemtherapie auf der Grundlage vorheriger Chemotherapien der Patient:innen.3 Bei 76% der Patient:innen wurde ein Tumoransprechen erreicht, bei 47% sogar die Konversion in eine resektable Erkrankung mit erhöhter Überlebenswahrscheinlichkeit. Auch die Kombination von Floxuridin mit Bevacizumab wurde untersucht. Diese zeigte aber eine erhöhte Toxizität der Gallenwege. Die Autor:innen rieten daher von dieser Kombinationstherapie ab. Die Langzeitergebnisse dieser MSKCC-Kohorte von zuvor inoperablen CRLM beschrieben eine noch höhere Konversionsrate von 52%. Die 5-Jahres-Überlebensrate in dieser einarmigen Studie lag bei ausgezeichneten 36%.4
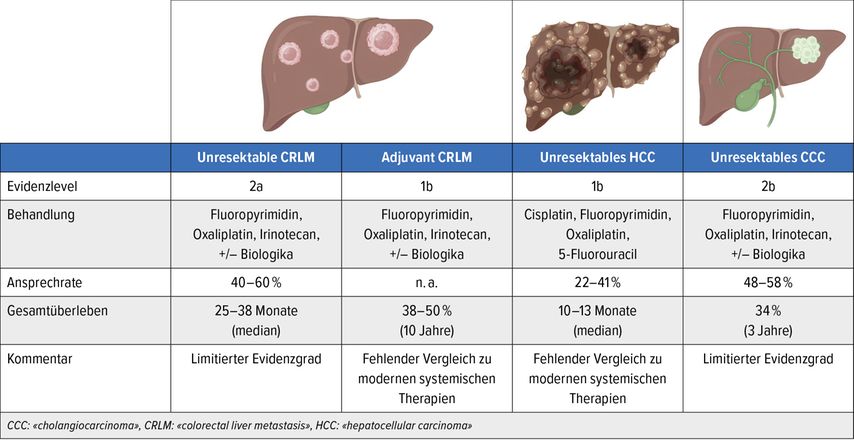
Die Anwendung von Irinotecan, Oxaliplatin und 5-FU in Kombination mit intravenös verabreichtem Cetuximab erreichte eine Ansprechrate von 41% bei einem Gesamtüberleben von 25,5 Monaten. Etwa 30% der Patient:innen konnten reseziert werden. Kemeny et al. berichteten sogar über eine Ansprechrate von 92% und eine Resektabilitätsrate von 47% beim Vergleich von intraarteriellem 5-FU und Systemtherapie mit Oxaliplatin und Irinotecan (Abb.1).5,6
Abb. 1: Zusammenfassung der Anwendungsbereiche der intraarteriellen Chemotherapie und der jeweiligen Ergebnisse
Adjuvante Therapie
Evidenzlevel 1b
Eine kürzlich publizierte Metaanalyse identifizierte acht randomisierte Studien mit 652 Patient:innen. Die Hazard-Ratio (HR) für das Gesamtüberleben betrug 0,91 (95% CI: 0,72–1,14) und zeigte keinen Unterschied zwischen Patient:innen mit und ohne intraarterielle Chemotherapie. Die Hälfte der Studien verglich die Anwendung mit Systemtherapie als Kontrolle, die andere Hälfte mit keiner adjuvanten Therapie als Kontrolle. Sobaldnichtrandomisierte Studien miteingeschlossen wurden, zeigtesich ein Vorteil der intraarteriellen Chemotherapie in Bezug auf das Gesamtüberleben (HR: 0,77; 95% CI: 0,64–0,93). Wichtig für die Interpretation der Ergebnisse ist, dass nach 2010 nur zwei randomisierte Studien veröffentlicht wurden.
In weiteren Subgruppenanalysen nichtrandomisierter Studien zeigte sich ein Nutzen überwiegend unter Verwendung von Floxuridin (HR: 0,76; 95% CI: 0,62–0,94)sowie unter der Kombination von intraarterieller Chemotherapie mit adjuvanter Systemtherapie (HR: 0,75; 95% CI: 0,59–0,90). Eine wesentliche Einschränkung der eingeschlossenen Studien ist erneut die Heterogenität bezüglich Tumorlast, der Beurteilung des Ansprechens und der Resektabilität. Systemtherapien sind hauptsächlich eine Kombination aus 5-FU, Oxaliplatin und Irinotecan, aber verschiedene neue Biologika können hinzugefügt werden. Mit modernen Wirkstoffen, die intraarteriell angewendet werden, erhöhen sich die Ansprechraten. Die Möglichkeit, eine intraarterielle Chemotherapie bei Patient:innen zu initiieren, deren Erkrankung unter Systemtherapie auch nach mehreren Behandlungslinien fortschreitet, ist eine vielversprechende Erweiterung der Therapieoptionen bei einer schwer zu behandelnden fortgeschrittenen Erkrankung.
Auch in diesem Anwendungsgebiet stammt die grösste Studie aus dem MSKCC. Bei Patient:innen, die sich einer vollständigen Resektion und anschliessender intraarterieller Chemotherapie unterzogen, betrug die Gesamtüberlebenswahrscheinlichkeit über zehn Jahre 51%, verglichen mit 31% bei Patient:innen, die nur eine adjuvante Systemtherapie erhielten.7 Die Daten zur Überlebenswahrscheinlichkeit nach zehn Jahren wurden mit Daten aus der institutionellen Datenbank aktualisiert und ergänzt. Zusammen ergab sich eine erhöhte Rate des Gesamtüberlebens von 57%.8 Zu bemerken ist, dass nur wenige internationale Zentren mehr als eine initiale Serie veröffentlichten und es daher an Konsens und Benchmarkwerten in Bezug auf anzustrebende Ergebnisse mangelt.
Primäre Lebertumoren
Hepatozelluläres Karzinom
Evidenzlevel 1b
Die Behandlung des HCC richtet sich nach dem Barcelona-Clinic-Liver-Cancer-Algorithmus (BCLC), der 2022 aktualisiert wurde.9 Eine chirurgische Resektion wird nur Patient:innen mit kleinen HCC ohne makrovaskuläre Invasion und bei erhaltener Leberfunktion angeboten. Eine Transplantation ist in den meisten Ländern Patient:innen mit HCC nach den Milan-Kriterien oder angepassten Versionen davon vorbehalten.10
Für HCC im mittleren oder fortgeschrittenen Stadium gibt es mehrere Optionen für lokale und systemische Therapien. Transarterielle Therapien spielen eine Rolle bei der Behandlung von HCC ausserhalb der Transplantationskriterien oder als Überbrückungsmassnahme respektive Downstaging vor Transplantation. Neben kathetergestützter Embolisation wie transarterieller Chemoembolisation (TACE) oder lokaler Bestrahlung ist die intraarterielle Chemotherapie Teil der multimodalen Therapieoptionen in diesem Algorithmus. In der Praxis wird die intraarterielle Chemotherapie meist mit einer systemischen Therapie kombiniert, da sich in der alleinigen Anwendung kein Überlebensvorteil gezeigt hat.
Die Wirksamkeit einer Kombination aus Sorafenib und intraarterieller Chemotherapie wurde in mehreren RCT untersucht.11–14 Ikeda et al. wiesen dreifach höhere Ansprechraten (7,3% vs. 21,7%; p=0,09) und ein verlängertes medianes Überleben nach, wenn die Patient:innen mit Sorafenib und intraarteriellem Cisplatin im Vergleich zu Sorafenib allein behandelt wurden (10,6 vs. 8,7 Monate; HR: 0,68; 95% CI: 0,44–1,05; p=0,073). Ähnliche Ergebnisse lieferten He et al. in einer randomisierten multizentrischen Studie. Die Autor:innen verglichen den Einsatz intaarterieller Chemotherapie mit FOLFOX zu Sorafenib mit dem Einsatz von Sorafenib allein bei Patient:innen mit HCC und Pfortaderinvasion. Hier zeigten sich eine deutlich höhere Ansprechrate (40,8% vs. 2,5%; p<0,001) und ein fast doppelt so langes Überleben (13,4 Monate statt 7,1; HR: 0,35; 95% CI: 0,26–0,48; p<0,001).Die grösste randomisierte, multizentrische Phase-III-Studie mit 206 Patient:innen fand dagegen keinen signifikanten Unterschied im Gesamtüberleben bei der Kombination von Sorafenib mit intraarterieller Chemotherapie mit niedrig dosiertem Cisplatin und 5-FU (11,5 vs. 11,8 Monate; p=0,955). Eine weitere kleine randomisierte Studie, in der auch Patient:innen mit Pfortaderthrombose eingeschlossen wurden, zeigte höhere Ansprechraten bei der Kombinationstherapie von Sorafenib und Oxaliplatin/5-FU intraarteriell gegenüber Sorafenib allein (41% vs. 3%; p<0,001). Ausserdem betrug das mediane Überleben 16,3 Monate mit Sorafenib plus intraarterieller Chemotherapie und 6,5 Monate mit Sorafenib alleine (HR: 0,28; 95% CI: 0,15–0,53; p<0,001). In den genannten Studien war die Rate unerwünschter Ereignisse in der Gruppe mit intraarteriellerChemotherapie mit jener der Kontrollgruppe vergleichbar. Katheterbedingte Komplikationen waren mit einer Inzidenz von 6–12% gering. Bemerkenswert ist, dass in den vier Studien nur eine Reoperation aufgrund eines unerwünschten Ereignisses unter der intraarteriellen Chemotherapie nötig war.
Während die randomisierten Studien die Durchführbarkeit der arteriellen Chemotherapie belegten, war der zusätzliche Überlebensvorteil der Kombination mit Sorafenib aber nicht konstant nachweisbar. Letztlich ist eine grosse multizentrische Studie zur Bestätigung oder Widerlegung eines Nutzens von intraarterieller Chemotherapie beim HCC erforderlich.
Cholangiozelluläres Karzinom
Evidenzlevel 2b
Patient:innen mit CCC weisen häufig ein fortgeschrittenes Krankheitsstadium mit entsprechend kurzer Überlebenszeit auf. Beim intrahepatischen CCC (iCCC) im Frühstadium kann eine Operation die 5-Jahres-Überlebensrate um bis zu 40% erhöhen.15 Die Rolle der Transplantation bei inoperabler Erkrankung ist nach wie vor umstritten, da die Selektionskriterien derzeit nicht genau definiert sind. Darüber hinaus wurden bei der systemischen Behandlung von Patient:innen mit fortgeschrittenem CCC zwar Fortschritte erzielt, doch liegt die mediane Überlebenszeit mit den neusten Therapieschemata nach wie vor bei knapp zwölf Monaten. Lokale Behandlungsmethoden wie die Radio- und Chemoembolisation oder die intraarterielle Chemotherapie sind daher attraktive Behandlungsoptionen, solange der Tumor auf die Leber beschränkt ist.
Für die intraarterielle Chemotherapie beim iCCC gibt es nur wenig Evidenz. In einer einarmigen Phase-III-Studie mit intraarteriellem Floxuridin in Kombination mit systemischem Gemcitabin und Oxaliplatin zeigten 38 Patient:innen mit ursprünglich inoperablen Tumoren eine radiologische Ansprechrate von 58% und eine Tumorkontrolle in 86%. Der Effekt war dabei unabhängig vom Lymphknotenstatus. Vier Patient:innen (11%) konnten sogar in ein resektables Stadium konvertiert werden.16
Bei Patient:innen mit inoperablem iCCC zeigen Langzeitdaten aus prospektiven Studien ebenfalls eine ausgezeichnete Tumorkontrolle bei der Behandlung mit intraarterieller Chemotherapie. So hatten 48% der Patient:innen ein partielles Ansprechen und eine 3-Jahres-Überlebensrate von fast 40%, selbst ohne Resektion. Kasai berichtete über eine Fallserie von 20 Patient:innen mit fortgeschrittenem iCCC mit einer Ansprechrate von 60%, wenn die Patient:innen eine kombinierte Therapie mit 5-FU und pegyliertem Interferon mit intraarterieller Chemotherapie erhielten. Allerdings hatte ein Viertel der Patient:innen in dieser Kohorte bereits pulmonale Metastasen. Ghiringhelli et al. berichteten über eine Krankheitskontrollrate von 91% in einer Serie von zwölf Patient:innen, die mit einer Kombination aus Gemcitabin und Oxaliplatin behandelt wurden.17
Die neuste biinstitutionelle Studie, an der 268 Patient:innen aus den Niederlanden und dem MSKCC teilnahmen, zeigte einen deutlichen Überlebensvorteil in einer intraarteriell behandelten Kohorte im Vergleich zur systemischen Gabe von Gemcitabin und Cisplatin (Gesamtüberleben nach drei Jahren 34,3% vs. 3,5%).18 Die Überlebenswahrscheinlichkeit im beobachteten Zeitraum war mit intraarterieller Chemotherapie knapp viermal höher.
In einer retrospektiven multizentrischen Analyse wurde die Behandlung von histologisch nachgewiesenem multifokalem iCCC mit intraarteriellem 5-FU bei 141 Patient:innen mit der Resektion bei 178 Patient:innen verglichen.19 Die über einen Zeitraum von 18 Jahren behandelten Patient:innen wiesen in der Gruppe mit intraarterieller Chemotherapie eine höhere Tumorlast auf. Die 30-Tage-Sterblichkeit war in der Resektionsgruppe 8-malhöher (intraarterielle Chemotherapie: 0,8% vs. Resektion: 6,2%), während das mediane Gesamtüberleben vergleichbar war (20 Monate vs. 19 Monate). Auf Grundlage dieser Ergebnisse muss die Indikation zur Resektion multifokaler iCCC überdacht werden, wenn kein Überlebensvorteil im Vergleich zur intraarteriellen Chemotherapie erzielt werden kann – zumal das Mortalitätsrisiko einer chirurgischen Resektion deutlich höher war.
Patienten mit inoperablem mit intraarteriellem Floxuridin behandeltem iCCC zeigten in einer Metaanalyse von vier Studien und 144 Patient:innen, einschliesslich der oben erwähnten Phase-II-Studie, eine deutlich erhöhte Überlebenswahrscheinlichkeit über drei Jahre mit 39,5% verglichen mit 0% für SCT.
Zusammenfassend kann die intraarterielle Chemotherapie die Raten von Ansprechen und Resektabilität erhöhen und das Langzeitüberleben bei selektionierten Patient:innen mit primären und sekundären Lebermalignomen verlängern. Die Kombination mit systemischer Chemotherapie ist besonders vielversprechend für die Konversionstherapie von ursprünglich inoperablen Tumoren. Des Weiteren sind die adjuvante Behandlung von Patient:innen mit Lebererkrankungen oder die palliative Behandlung von auf die Leber limitierten Erkrankungen attraktiv, mit dem Potenzial, die systemischen Nebenwirkungen zu minimieren.
Literatur:
1 Lam VW et al.: A systematic review of clinical response and survival outcomes of downsizing systemic chemotherapy and rescue liver surgery in patients with initially unresectable colorectal liver metastases. Ann Surg Oncol 2012; 19(4): 1292-1301 2 Safi F et al.: Regional chemotherapy for hepatic metastases of colorectal carcinoma (continuous intraarterial versus continuous intraarterial/intravenous therapy). Results of a controlled clinical trial. Cancer 1989; 64(2): 379-87 3 DʼAngelica MI et al.: Phase II trial of hepatic artery infusional and systemic chemotherapy for patients with unresectable hepatic metastases from colorectal cancer: conversion to resection and long-term outcomes. Ann Surg 2015; 261(2): 353-60 4 Pak LM et al.: Prospective phase II trial of combination hepatic artery infusion and systemic chemotherapy for unresectable colorectal liver metastases: long term results and curative potential. J Surg Oncol 2018; 117(4): 634-43 5 Kemeny NE et al.: Conversion to resectability using hepatic artery infusion plus systemic chemotherapy for the treatment of unresectable liver metastases from colorectal carcinoma. JClin Oncol 2009; 27(21): 3465-71 6 Boige V et al.: Hepatic arterial infusion of oxaliplatin and intravenous LV5FU2 in unresectable liver metastases from colorectal cancer after systemic chemotherapy failure. Ann Surg Oncol 2008; 15(1): 219-26 7 Srouji R et al.: Addition of adjuvant hepatic artery infusion to systemic chemotherapy following resection of colorectal liver metastases is associated with reduced liver-related mortality. J Surg Oncol 2020; 121(8): 1314-9 8 Ecker BL et al.: Genomic stratification of resectable colorectal liver metastasis patients and implications for adjuvant therapy and survival. Ann Surg 2022; 275(2): 371-81 9 Reig M et al.: BCLC strategy for prognosis prediction and treatment recommendation: the 2022 update. J Hepatol 2022; 76(3): 681-93 10 Tschuor C et al.: Allocation of liver grafts worldwide - is there a best system? J Hepatol 2019; 71(4): 707-18 11 Ikeda M et al.: Sorafenib plus hepatic arterial infusion chemotherapy with cisplatin versus sorafenib for advanced hepatocellular carcinoma: randomized phase II trial. Ann Oncol 2016; 27(11): 2090-6 12 He M et al.: Sorafenib plus hepatic arterial infusion of oxaliplatin, fluorouracil, and leucovorin vs sorafenib alone for hepatocellular carcinoma with portal vein invasion: a randomized clinical trial. JAMA Oncol 2019; 5(7): 953-60 13 Kudo M et al.: Sorafenib plus low-dose cisplatin and fluorouracil hepatic arterial infusion chemotherapy versus sorafenib alone in patients with advanced hepatocellular carcinoma (SILIUS): a randomised, open label, phase 3 trial. Lancet Gastroenterol Hepatol 2018; 3(6): 424-32 14 Zheng K et al.: Sorafenib plus hepatic arterial infusion chemotherapy versus sorafenib for hepatocellular carcinoma with major portal vein tumor thrombosis: a randomized trial. Radiology 2022; 303(2): 455-64 15 Marcus R et al.: Systemic therapy is associated with improved oncologic outcomes in resectable stage II/III intrahepatic cholangiocarcinoma: an examination of the National Cancer Database over the past decade. Cancers (Basel) 2022; 14(17): 4320 16 Cercek A et al.: Assessment of hepatic arterial infusion of floxuridine in combination with systemic gemcitabine and oxaliplatin in patients with unresectable intrahepatic cholangiocarcinoma: aphase 2 clinical trial. JAMA Oncol 2020; 6(1): 60-7 17 Ghiringhelli F et al.: Hepatic arterial infusion of gemcitabine plus oxaliplatin as second-line treatment for locally advanced intrahepatic cholangiocarcinoma: preliminary experience. Chemotherapy 2013; 59(5): 354-60 18 Franssen S et al.: Gemcitabine with cisplatin versus hepatic arterial infusion pump chemotherapy for liver-confined unresectable intrahepatic cholangiocarcinoma. Ann Surg Oncol 2024; 31(1): 115-124 19 Franssen S et al.: Comparison of hepatic arterial infusion pump chemotherapy vs resection for patients with multifocal intrahepatic cholangiocarcinoma. JAMA Surg 2022; 157(7): 590-6
Das könnte Sie auch interessieren:
Adjuvantes Osimertinib reduziert ZNS-Rezidive bei EGFR-mutierter Erkrankung
Etwa 30% der Patienten mit nicht kleinzelligem Lungenkarzinom (NSCLC) präsentieren sich mit resezierbarer Erkrankung und werden einer kurativen Operation unterzogen. Viele Patienten ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...