Innovationen in der Brustkrebstherapie
Bericht:
Ingeborg Morawetz, MA
Univ.-Prof. Dr. Michael Gnant fasst die Highlights des Jahrestreffens 2022 der American Society of Clinical Oncology (ASCO) zur Mammakarzinomtherapie zusammen. Besonders die DESTINY-Breast04-Studie bei Low-HER2-Patient*innen brachte richtungsweisende Erkenntnisse hervor. Mit der ABCSG-18-Studie war auch die österreichische Forschung wieder beim ASCO-Jahrestreffen vertreten.
In mehrerer Hinsicht bemerkenswert – so beschreibt Prof. Dr. Gnant das diesjährige Jahrestreffen der ASCO. Im Vergleich zu den letzten Jahren war es vor allem innovationsgetrieben.
DESTINY-Breast04: richtungsweisend
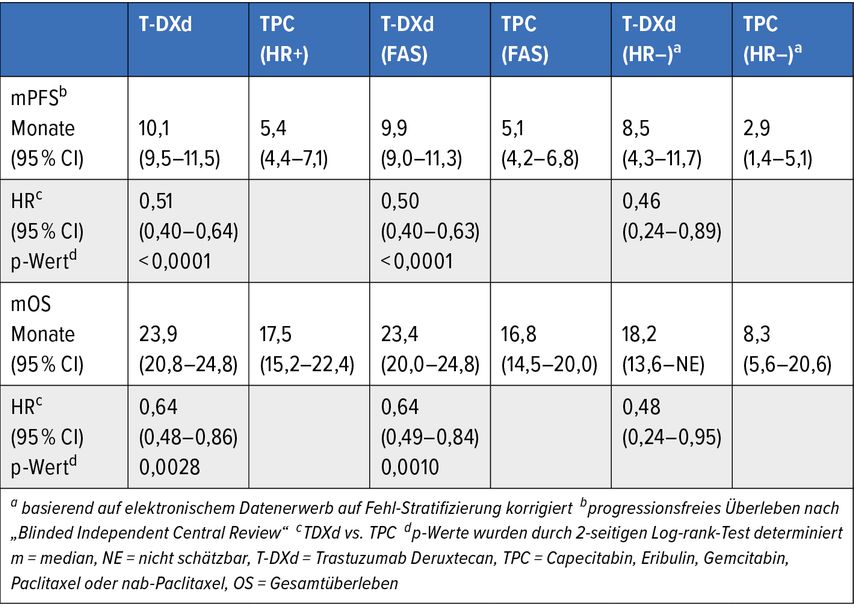
Als überragend hervorzuheben sind hierbei die Ergebnisse der randomisierten, multizentrischen, „open-label“ Phase-III-Studie DESTINY-Breast04, die ebenfalls präsentiert wurden (Tab. 1). Sie demonstrieren, dass auch eine geringe Expression von HER2 dazu genutzt werden kann, einen aktiven Wirkstoff an die Karzinomzellen heranzubringen. So können Patient*innen mit Metastasen, die wegen ihres geringen HER2-Wertes vormals als HER2-negativ galten, erfolgreich mit HER2-zielgerichteter Therapie behandelt werden.
Unter dem primären Endpunkt progressionsfreies Überleben (PFS) wurde das Antikörper-Wirkstoff-Konjugat Trastuzumab Deruxtecan (T-DXd) gegen eine Chemotherapie mit einem einzelnen Wirkstoff (Capecitabin, Eribulin, Gemcitabin, Paclitaxel oder nab-Paclitaxel [TPC]) getestet. Patient*innen, die mit T-DXd behandelt wurden, profitierten in späterer Linie im Vergleich zu „Physician’s choice“-Chemotherapie dramatisch. Prof. Dr. Gnant schätzt dieses Ergebnis vor allem deswegen als bedeutend ein, da es in Bezug auf die Therapiemöglichkeiten einen ganz neuen Typ von Mammakarzinom definiert – es ist „richtungsweisend in der neuen Therapieentscheidung“.1
Klarer DFS-Vorteil in ASTRRA-Studie
Ein Update nach acht Jahren zur ASTRRA-Studie zählt zu Prof. Dr. Gnants persönlichen Favoriten, da es eine für den klinischen Alltag sehr wichtige Frage behandelt. In der prospektiven randomisierten Phase-III-Studie ASTRRA wurde bei Patient*innen die Wirkung von ovarieller Suppression (OFS) in Ergänzung zur Gabe von Tamoxifen getestet. Die inkludierten Patient*innen hatten ER-positiven Brustkrebs und waren nach Chemotherapie weiterhin prämenopausal und/oder hatten eine fortgesetzte ovarielle Aktivität.
Ein Follow-up nach median 63 Monaten zeigte, dass zwei Jahre zusätzliche OFS zur Tamoxifen-Gabe signifikant das krankheitsfreie Überleben (DFS) verlängerte. Ein weiteres nach 106,4 Monaten bestätigt diesen Vorteil (85,4% vs. 80,2% [HR 0,67; 95% CI: 0,51–0,87]). Im zweiten primären Endpunkt Gesamtüberleben (OS) gab es jedoch keine signifikante Verlängerung. Es besteht die Hoffnung, dass sich bei weiterer Nachverfolgung auch für das OS ein Vorteil ergeben wird.2
UNICANCER ASTER 70s mit geriatrischen Patient*innen
Die finalen Resultate der prospektiven randomisierten Phase-III-Studie UNICANCER ASTER 70s zu endokriner Therapie ± Chemotherapie bei Patient*innen ≥70 Jahre erlauben es nun, eine informierte Entscheidung dazu zu treffen, wann Chemotherapie bei älteren Menschen Vorteile bringt und wann sie eine vermeidbare Belastung darstellt. Die inkludierten Patient*innen hatten ER- und HER2-positiven Brustkrebs und wurden anhand ihres „Tumour Genetic Grade“-Indexes (GGI) evaluiert. Jene mit hohem GGI wurden auf die Arme endokrine Therapie und endokrine Therapie + Chemotherapie randomisiert.
Das primäre Ziel war, in der ITT-Population einen OS-Vorteil für Chemotherapie nachzuweisen. Diese formale Testung erbrachte nur einen kleinen Vorteil von 0,7%, der statistisch nicht signifikant war. Die Ergebnisse für die sekundären Endpunkte Brustkrebs-spezifisches Überleben (BCSS), metastasenfreies Überleben (iDFS), ereignisfreies Überleben (EFS), konkurrierende Ereignisse, Kosteneffizienz und Q-TwiST-Analyse, geriatrische Dimensionen, Bereitwilligkeit und Lebensqualität werden erwartet.3
Denosumab punktet in ABCSG-18
In einem medianen Follow-up nach acht Jahren wurden die Langzeitergebnisse der österreichischen prospektiven, doppelblinden, placebokontrollierten Phase-III-Studie ABCSG-18 präsentiert. Wie schon 2015 beim ASCO-Jahrestreffen erläutert und im Journal „The Lancet“ beschrieben, reduziert adjuvantes Denosumab die Knochenfrakturen bei postmenopausalen HR-positiven Patient*innen, die mit Aromataseinhibitoren behandelt werden, im Vergleich zu Placebo beinahe um die Hälfte. Dieses Jahr konnte außerdem gezeigt werden, dass das DFS, das knochenmetastasenfreie Überleben und das OS um ungefähr 20% verlängert wurden.
Diese Ergebnisse sind insbesondere deshalb bemerkenswert, weil das Ende der randomisierten Therapie für diePatient*innen dieser Studie eigentlich bereits fünf Jahre zurückliegt. Es gab zwar ein Cross-over nach dem Primärergebnis, dennoch wird deutlich, dass mit der recht wenig invasiven Intervention mit Denosumab (2x s.c. pro Jahr) das OS verlängert werden kann. Die Studie ist zwar eher als formal deskriptiv zu werten, sie ist aber die einzige weltweit, die mit diesem Setting gearbeitet und so diese Ergebnisse erbracht hat.4
CALGB 9741 (Alliance): SET2,3 als neuer Biomarker
In einer Präsentation zur CALGB-9741- (Alliance)-Studie wurden die Ergebnisse zur prognostischen Aussagekraft des neuen Biomarkers SET2,3 vorgestellt. SET2,3 misst die endokrine Sensitivität in Form von nicht proliferativer Hormonrezeptor-bezogener Transkription. Der neuartige Prognoseindex wurde über Tumorgröße, Lymphknoteninvolvierung und einen molekularen Subtyp aus vier Genen kreiert.Zuvor waren in der CALGB-9741-Studie bei prä- und postmenopausalen ER-negativen Patient*innen Vorteile bei DFS und OS nachgewiesen worden, wenn sie statt einer dreiwöchigen Chemotherapie eine zweiwöchige mit höherer Dosierung erhielten. Mit dem ROR-PT-Score zur Voraussage von Rezidiven konnte dieser Vorteil jedoch nicht prognostiziert werden. Im Gegensatz dazu erwies sich der SET2,3-Index bei ER-positiven Patient*innen als stark prognostisch für die guten Ergebnisse der zeitlich verkürzten Chemotherapie.5
LUMINA: Radiotherapie ja oder nein?
Die Ergebnisse der LUMINA-Studie können in Zukunft dabei helfen, bei Patient*-innen mit klinisch-pathologisch niedrigem Rezidivrisiko eine Entscheidung für oder gegen adjuvante Radiotherapie zu treffen. Die prospektive multizentrische Kohortenstudie inkludierte 501 Patient*innen ≥55 Jahre, die mit brusterhaltender Resektion von Tumoren Grad 1–2 (T1,N0) mit ≥1mm Resektionsrändern und adjuvanter endokriner Therapie behandelt wurden. Ihr Brustkrebs war vom Luminal- A-Subtyp (ER 1, PR >20%, HER2-negativ, Ki67 ≤13,25%) und damit vom Subtyp mit dem geringsten Rezidivrisiko.
Für ein positives Ergebnis der Studie musste bei den Patient*innen unter der Annahme einer Rezidivrate von 3,5% nach fünf Jahren nachgewiesen werden, dass die obere Grenze des zweiseitigen CI von 90% unter 5% lag. Diese Voraussetzung wurde erfüllt. Bei Patient*innen, die die Inklusionskriterien der LUMINA-Studie erfüllen, ist das Risiko für ein lokales Rezidiv niedrig genug, um auf die unter Umständen belastende Radiotherapie verzichten zu können.6
BMI: zusätzliche Analyse zur PALLAS-Studie
Der Body-Mass-Index (BMI) hat eine Auswirkung auf Risiko und Prognose von Brustkrebs. Für den BMI als prognostischen Faktor für den Vorteil endokriner Therapie gibt es jedoch bisher nur widersprüchliche Ergebnisse. In der PALLAS-Studie wurde die Therapie mit dem CDK4/6-Inhibitor Palbociclib und endokriner Therapie (ET) oder ET alleine untersucht. In einer weiteren Analyse wurden nun die Effekte des BMI auf die Behandlung mit Palbociclib und ET näher beleuchtet.
5698 Patient*innen mit metastasiertem HR-positivem Brustkrebs wurden inkludiert. Sie wurden entsprechend ihrem BMI eingeteilt in untergewichtig, normalgewichtig, übergewichtig und adipös (BMI <18,5kg/m2, 18,5–24,9kg/m2, 25–29,9kg/m2, 30kg/m2). Neutropenie trat als Haupttoxizität und häufigster Grund auf, die Behandlung mit Palbociclib abzubrechen. Sie kam bei normalgewichtigen Patient*innen in 88,5% der Fälle vor, bei übergewichtigen in 85,7% und bei adipösen in 74,7%. In der Gruppe mit Kombinationstherapie führte sie bei 21,1% der normalgewichtigen, 14,0% der übergewichtigen und 5,9% der adipösen Patient*innen zu einem Abbruch der Behandlung. Beim metastasenfreien Überleben zeigten sich bisher keine Unterschiede zwischen den BMI-Gruppen.7
Kommentar
Echte Neuheiten in der Behandlung des Mammakarzinoms
Das ASCO-Jahrestreffen 2022 war nicht nur bemerkenswert, weil endlich wieder 30000 Ärzt*innen und Forscher*innen persönlich zusammenkamen, sondern auch, weil diesmal einige echte Neuheiten in der Behandlung des Mammakarzinoms als Highlights hervorstachen:
Über die unmittelbare Studiensituation hinaus Bedeutung hat das – auch zeitgleich im „New England Journal of Medicine“ veröffentlichte – Ergebnis von DESTINY-Breast04. Es zeigt, dass das Prinzip des Antibody-Drug-Konjugats auch dann funktionieren kann, wenn der „identifizierende“ Biomarker nur mäßig oder gar schwach ausgeprägt ist. Naturgemäß muss nach diesem spektakulären Ergebnis nun eine Fülle von weiteren Fragen gerade der klinischen Anwendung in früheren Linien bzw. Krankheitsstadien beantwortet werden – aber das Prinzip ist geeignet, neue Optionen in der Onkologie zu eröffnen.
Die Beforschung besonderer Patient*innengruppen, also z.B. sehr junger Frauen wie in der ASTRRA-Studie oder älterer Patient*innen in der ASTER-70s-Studie, ist besonders wichtig. Gerade mit immer komplexeren Therapiealgorithmen besteht sonst die Gefahr, keine wissenschaftlichen Antworten für diese Subgruppen zu erhalten. Besonders die französische UNICANCER-Gruppe ist hier dafür zu beglückwünschen, dass sie für die – im Alltag so häufige – Patient*innengruppe betagter Brustkrebspatient*innen eine wichtige Richtschnur für die Anwendung adjuvanter Chemotherapie erarbeitet hat.
Biomarker können sowohl zur weiteren Individualisierung der Therapie als auch zur weiteren Deeskalation führen – dieser Megatrend der Onkologie ist unumkehrbar. Er stellt uns zwar beim Studiendesign vor zunehmend komplexere Herausforderungen, ist aber letztlich für die Fortschritte in der Präzisionsonkologie unerlässlich.
Dass bei einem so bedeutenden globalen Kongress auch Ergebnisse aus Österreich im Rampenlicht gestanden sind (ABCSG-18, PALLAS-BMI), darf uns nicht nur aus Nationalstolz freuen – es ist die Voraussetzung dafür, dass wir auch in Zukunft Innovationen zeitgerecht nach Österreich bekommen und unser kleines Land auf der weltweiten Forschungslandkarte positionieren, wovon letztlich unsere Patient*innen nachhaltig profitieren.
Univ.-Prof. Dr. Michael Gnant, Wien
Literatur:
1 Modi S et al.: Trastuzumab deruxtecan (T-DXd) versus treatment of physician’s choice (TPC) in patients (pts) with HER2-low unresectable and/or metastatic breast cancer (mBC): Results of DESTINY-Breast04, a randomized, phase 3 study. J Clin Oncol 2022; 40(suppl 17): Abstr. #LBA3 2 Baek SY et al.: Adding ovarian function suppression to tamoxifen in young women with hormone-sensitive breast cancer who remain premenopausal or resume menstruation after chemotherapy: 8-year follow-up of the randomized ASTRRA trial. J Clin Oncol 2022; 40(suppl 16): Abstr. #506 3 Brain E et al.: Final results from a phase III randomized clinical trial of adjuvant endocrine therapy ± chemotherapy in women ≥ 70 years old with ER+ HER2- breast cancer and a high genomic grade index: The Unicancer ASTER 70s trial. J Clin Oncol 2022; 40(suppl 16): Abstr. #500 4 Gnant M et al.: Long-term outcomes of adjuvant denosumab in breast cancer: Fracture reduction and survival results from 3,425 patients in the randomised, double-blind, placebo-controlled ABCSG-18 trial. J Clin Oncol 2022; 40(suppl 16): Abstr. #507 5 Metzger O et al.: Measurement of endocrine activity (SET2,3) related to prognosis and prediction of benefit from dose-dense (DD) chemotherapy in estrogen receptor-positive (ER+) cancer: CALGB 9741 (Alliance). J Clin Oncol 2022; 40(suppl 16): Abstr. #505 6 Whelan TJ et al.: LUMINA: A prospective trial omitting radiotherapy (RT) following breast conserving surgery (BCS) in T1N0 luminal A breast cancer (BC). JClin Oncol 2022; 40(suppl 17): Abstr. #LBA501 7 Pfeiler G et al.: Impact of body mass index on treatment and outcomes in patients with early hormone receptor-positive breast cancer receiving endocrine therapy with or without palbociclib in the PALLAS trial. J Clin Oncol 2022; 40(suppl 16): Abstr. #518
Das könnte Sie auch interessieren:
Adjuvantes Osimertinib reduziert ZNS-Rezidive bei EGFR-mutierter Erkrankung
Etwa 30% der Patienten mit nicht kleinzelligem Lungenkarzinom (NSCLC) präsentieren sich mit resezierbarer Erkrankung und werden einer kurativen Operation unterzogen. Viele Patienten ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...