Herausforderungen nach neoadjuvanter Immuntherapie aus Sicht der Radiologie
Autor*innen:
Daria Kifjak, PhD1,2
Assoc. Prof. Priv.-Doz. Dr. Helmut Prosch1
PD Dr. Lucian Beer1
1Department of Biomedical Imaging and Image-Guided Therapy, Medical University of Vienna, Vienna, Austria // Universitätsklinik für Radiologie und Nuklearmedizin, MUW
2Department of Radiology, UMass Memorial Medical Center and University of Massachusetts Chan Medical School, Worcester, MA, USA
Korrespondenz:
E-Mail: lucian.beer@meduniwien.ac.at
Die Immuncheckpoint-Inhibitor-Therapie (ICIT) hat in die Therapieschemata der frühen Stadien des nichtkleinzelligen Lungenkarzinoms Einzug gehalten. Die neoadjuvante ICIT in Kombination mit Chemotherapie führt zu einer hohen Rate (~25%) an kompletten pathologischen Remissionen und verbessertem Outcome. Was dieses neue Therapiekonzept für den radiologischen Befund bedeutet, bedarf einer näheren Betrachtung.
Keypoints
-
Neoadjuvante Chemo-Immuntherapie führt zu einer hohen Rate an kompletten pathologischen Remissionen.
-
Die residuale Tumorgröße sowie die Veränderungen (z.B. Abnahme) der Tumorgröße korrelieren nicht zwangsläufig mit dem histopathologischen Ansprechen.
-
Metabolische Untersuchungen wie die [18F]-FDG-PET/CT ermöglichen es, den Therapieerfolg besser zu überprüfen als rein morphologische Untersuchungen.
-
Neoadjuvante Chemo-Immuntherapie kann neben immunvermittelten Nebenwirkungen in seltenen Fällen ungewöhnliche Tumor-Reaktionsmuster wie einen „Nodal Immune Flare“ induzieren.
Neoadjuvante Therapiemöglichkeiten für Patient*innen mit nichtkleinzelligem Lungenkarzinom (NSCLC) in frühen (I–IIIa) und damit möglicherweise operablen Stadien befinden sich kontinuierlich im Wandel. Die neoadjuvante Kombination einer Immuncheckpoint-Inhibitor-Therapie (ICIT) mit Chemotherapie führt zu einer hohen Rate der kompletten pathologischen Tumorremission und verbessert klinische Endpunkte.1 In Europa befindet sie sich gegenwärtig in der Phase der klinischen Zulassung.
Nicht nur für die klinische Behandlung bedeutet dies eine Umstellung, sondern auch für die radiologische Evaluation dieser Patient*innen. Kombinationstherapien können – im Gegensatz zu klassischen zytotoxischen Chemotherapien – atypische Ansprechmuster zeigen.2 Für die Radiolog*innen ist die Kenntnis solcher Tumor-Reaktionsmuster wichtig, um einen wertvollen Beitrag zur korrekten Behandlung liefern zu können.
Diese Übersichtsarbeit soll sowohl zum besseren Verständnis des radiologischen Ansprechens als auch der aktuellen Rolle und Herausforderungen der Bildgebung bei Patient*innen mit nichtkleinzelligem Lungenkarzinom in einem frühen Stadium nach einer neoadjuvanten Immuncheckpoint-Inhibitor-Therapie dienen.
Histopathologisches Ansprechen
Das Tumoransprechen wird anhand der Ausdehnung des vitalen Tumorgewebes, der Tumornekrosen sowie der reaktiven Veränderungen ermittelt. Mithilfe mikroskopischer Untersuchungen können drei Kategorien des Ansprechens festgehalten werden: pathologische Komplettremission (keine vitalen Tumorzellen im Resektat), tiefes pathologisches Ansprechen (MPR: ≤10% vitale Tumorzellen im Resektat) und Nicht-MPR (>10% vitale Tumorzellen im Resektat).
Das histopathologische Tumoransprechen ist wichtig, da es als Prädiktor für einen klinischen Nutzen im Sinne eines progressionsfreien Überlebens dient.1,3
Radiologisches Ansprechen
Bei der Mehrzahl der Patient*innen mit neoadjuvanten ICIT in Kombination mit Chemotherapie lässt sich ein klassisches radiologisches Tumoransprechen finden. Dies bedeutet, dass eine radiologische Größenregression mit einer pathologischen Regression assoziiert ist. Jedoch gibt es nur sehr selten Fälle(<5%), bei denen es radiologisch zu einem kompletten Therapieansprechen kommt.
Dem gegenüber stehen zumindest 25% der Patient*innen, welche eine komplette pathologische Remission haben.1 Hier zeigt sich somit das Dilemma der radiologischen Befundinterpretation. Neoadjuvante ICIT in Kombination mit Chemotherapie führen zu einer lokalen Immunreaktion, welche Nekrose und Fibrose hervorruft. Die routinemäßig eingesetzte Computertomografie (CT) kann jedoch nicht zwischen vitalem Tumorgewebe und entzündlichen/fibrotischen Residuen unterscheiden. Dies erklärt die Diskrepanz zwischen nur <5% kompletter radiologischer Remission und ~25% kompletter pathologischer Remission.
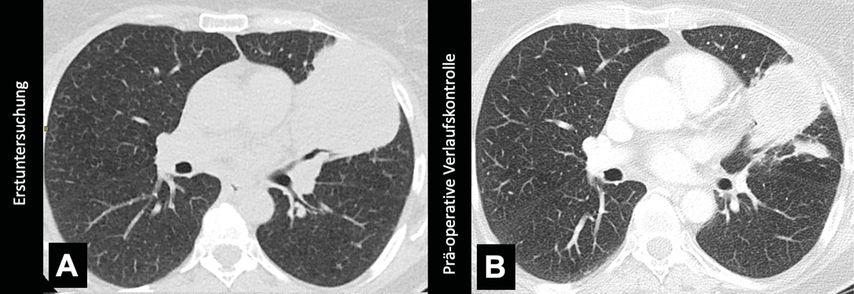
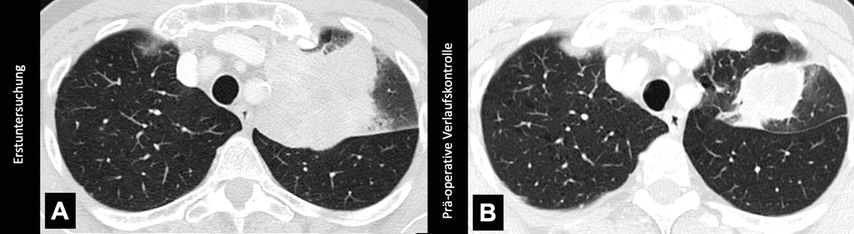
Die Verwendung traditioneller Kriterien, die das Therapieansprechen beurteilen (z.B. RECIST 1.1),ist somit nicht geeignet, um das histopathologische Ansprechen vorherzusagen.1 Dies ist exemplarisch an zwei Patienten veranschaulicht, welche beide radiologisch ein partielles Ansprechen zeigten und sich nicht unterschieden. Histopathologisch fand sich im ersten Fall eine komplette Tumorremission (Abb. 1), während im zweiten Fall noch reichlich vitales Tumorgewebe nachweisbar war (Abb. 2).
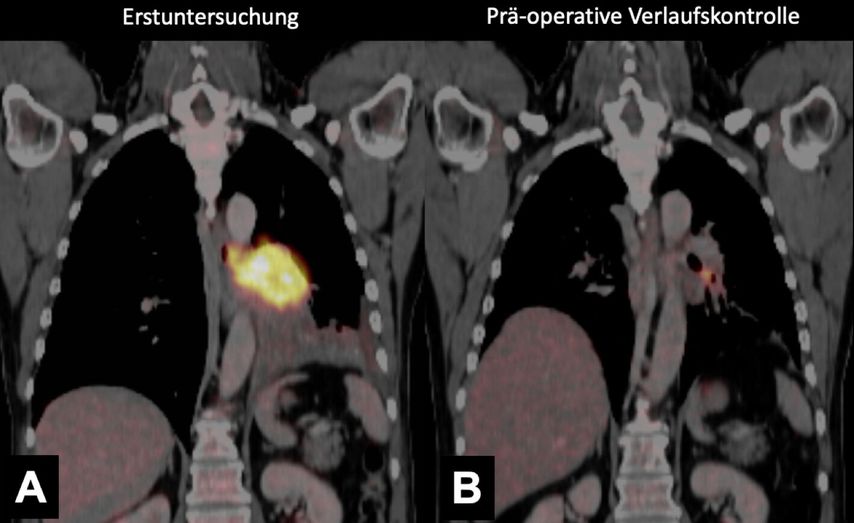
Die [18F]-FDG-PET/CT kann im Gegensatz zur CT auch metabolische Informationen zur Verfügung stellen und somit besser zwischen vitalem Tumorgewebe und Fibrose unterscheiden (Abb. 3).4,5 Aktive Inflammation zeigt jedoch auch einen erhöhten Glukosestoffwechsel und somit [18F]-FDG. Daher ist es selbst mit der [18F]-FDG-PET/CT bei neoadjuvanter ICIT nicht sicher möglich, zwischen malignen und entzündlichen Geweben zu unterscheiden.6
Abb. 1: Axiale CT-Rekonstruktionen eines 66-jährigen Patienten mit einem Adenokarzinom der Lunge im klinischen Stadium cT3, N1, M0 im linken Oberlappen und einer PD-L1-Expression von 20% (A). Nach einer neoadjuvanten Therapie mit Immuncheckpoint-Inhibitor (Pembrolizumab) in Kombination mit Chemotherapie zeigt der Patient ein Teilansprechen (B). Die histopathologische Untersuchung zeigte eine Komplettremission
Abb. 2: Axiale CT-Rekonstruktionen eines 60-jährigen Patienten mit einem Adenokarzinom des linken Oberlappens im klinischen Stadium cT3, N1, M0 (A). Nach einer neoadjuvanten Therapie mit Immuncheckpoint-Inhibitor (Pembrolizumab) in Kombination mit Chemotherapie zeigt der Patient ein Teilansprechen (B). Die histopathologische Untersuchung zeigte einen vitalen Tumorrest von 60% im Resektat
Abb. 3: Axiale CT-Rekonstruktionen eines 40-jährigen Patienten mit einem Adenokarzinom der Lunge. In der Erstuntersuchung zeigte sich ein klinisches Stadium cT3, N0, M0 (A). Nach einer neoadjuvanten Therapie mit Immuncheckpoint-Inhibitor (Pembrolizumab) in Kombination mit Chemotherapie zeigt der Patient ein metabolisches sowie morphologisches Teilansprechen (B). Die histopathologische Untersuchung zeigte ein tiefes pathologisches Ansprechen mit einem verbleibenden vitalen Tumorrest von ca. 1%
Atypische Tumor-Reaktionsmuster und immunvermittelte Nebenwirkungen
Der „Nodal Immune Flare“, die Pseudoprogression sowie die Hyperprogression gehören zu den sogenannten atypischen Tumor-Reaktionsmustern bei Patient*innen unter neoadjuvanter ICIT. Unter „Nodal Immune Flare“ versteht man eine Entzündungsreaktion der Lymphknoten unter ICIT. Diese ist radiologisch charakterisiert durch eine Größenzunahme und vermehrte [18F]-FDG-Aufnahme. Weder die CT noch [18F]-FDG-PET/CT können zwischen Tumorprogress und „Nodal Immune Flare“ unterscheiden.6In diesen Fällen hilft es jedoch, die Reaktion des Primus zu beurteilen. Eine Größenabnahme oder eine reduzierte [18F]-FDG-Aufnahme des Primärtumors machen einen „Nodal Immune Flare“ am wahrscheinlichsten. Im Gegensatz dazu deutet eine Größenprogredienz des Primus auf eine Tumorprogression mit maligner Lymphadenopathie hin.
Der „Nodal Immune Flare“ ist eine Form der Pseudoprogression. Im Rahmen der klassischen Pseudoprogression wird der Primärtumor in der Zwischenuntersuchung größer und nimmt in der Folgeuntersuchung an Größe ab. Unter Hyperprogression hingegen versteht man ein um das Doppelte erhöhtes Tumorwachstum. Sowohl die Pseudoprogression als auch die Hyperprogression treten eher im Zusammenhang mit adjuvanter Immuntherapie auf, können jedoch, wenn auch seltener, im neoadjuvanten Immuntherapie-Setting beobachtet werden.
Literatur:
1 Forde PM et al.: Neoadjuvant nivolumab plus chemotherapy in resectable lung cancer. N Engl J Med 2022; 386: 1973-85 2 Beer L et al.: Particular findings on lung CT in patients undergoing immunotherapy for bronchogenic carcinoma. Wiener Klinische Wochenschrift 2020; 132: 467-74 3 Provencio-Pulla M et al.: Nivolumab + chemotherapy versus chemotherapy as neoadjuvant treatment for resectable stage IIIA NSCLC: primary endpoint results of pathological complete response (pCR) from phase II NADIM II trial. J Clin Oncol 2022; 40: 8501 4 Chen ZY et al.: Dynamic (18) F-FDG PET/CT can predict the major pathological response to neoadjuvant immunotherapy in non-small cell lung cancer. Thorac Cancer 2022; 13: 2524-31 5 Ma T et al.: Pathological complete response to neoadjuvant chemoimmunotherapy correlates with peripheral blood immune cell subsets and metastatic status of mediastinal lymph nodes (N2 lymph nodes) in non-small cell lung cancer. Lung Cancer 2022; 172: 43-52 6 Cascone T et al.: Nodal immune flare mimics nodal disease progression following neoadjuvant immune checkpoint inhibitors in non-small cell lung cancer. Nat Commun 2021; 12: 5045
Das könnte Sie auch interessieren:
Adjuvantes Osimertinib reduziert ZNS-Rezidive bei EGFR-mutierter Erkrankung
Etwa 30% der Patienten mit nicht kleinzelligem Lungenkarzinom (NSCLC) präsentieren sich mit resezierbarer Erkrankung und werden einer kurativen Operation unterzogen. Viele Patienten ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...