Die Immuntherapien der Zukunft
Unser Gesprächspartner:
Prof. Dr. med. Christoph Renner
Onkozentrum Hirslanden, Zürich
E-Mail:
christoph.renner@hirslanden.ch
Das Interview führte
Dr. Nicole Leitner
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Der diesjährige Kongress der American Society of Clinical Oncology (ASCO) bot eine Fülle interessanter Daten zu den Lymphomen. Im Mittelpunkt standen immunonkologische Ansätze, sowohl mit einer Behandlung durch Checkpoint-Inhibitoren als auch mit der «Chimeric antigen receptor»(CAR)-T-Zell-Therapie. Wir sprachen mit Prof. Dr.med. Christoph Renner vom Onkozentrum Hirslanden darüber, wie er die neuen Ergebnisse interpretiert und welche Auswirkungen sie seiner Meinung nach auf die klinische Praxis haben werden.
Bei Patienten mit rezidiviertem klassischem Hodgkin-Lymphom verglich die KEYNOTE-204-Studie Pembrolizumab mit Brentuximab Vedotin. Was waren die Ergebnisse dieser Studie?
C. Renner: Die KEYNOTE-204-Studie beschäftigt sich mit der Frage, welches die optimale Therapieform beim refraktären/rezidivierten klassischen Hodgkin-Lymphom (r/r cHL) darstellt. In der Schweiz ist die Immuntherapie mit Checkpoint-Inhibitoren (CPI) bei dieser Indikation bislang erst in der dritten oder vierten Linie nach einer Behandlung mit dem CD30-spezifischen Immuntoxin Brentuximab Vedotin (BV) zugelassen.
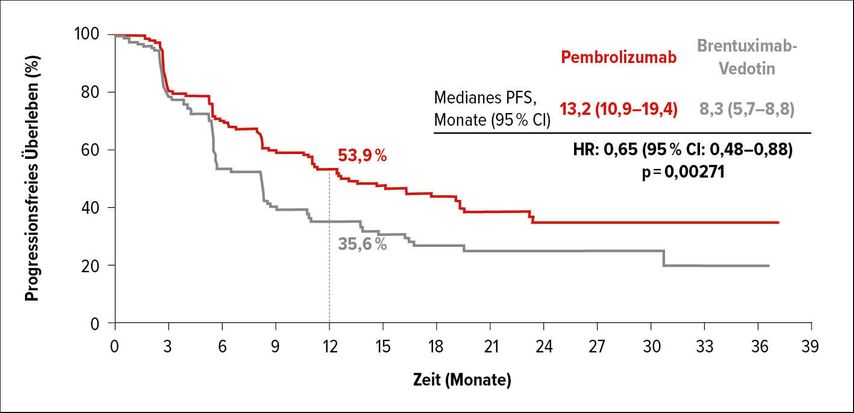
In der randomisierten Phase-III-Studie wurde nun Pembrolizumab (Pembro) mit Brentuximab Vedotin (BV) verglichen. 150 Patienten pro Studienarm waren miteingeschlossen. Ein Drittel der Patienten hatte vor Studienbeginn eine autologe Stammzelltransplantation (ASCT) erhalten. Zwei Drittel der Patienten waren refraktär oder rezidivierten innert 12 Monaten auf die vorhergehende Therapielinie. Es handelte sich also um ein recht ungünstiges Kollektiv.
Das progressionsfreie Überleben (PFS) konnte unter Pembro im Vergleich zu BV in etwa verdoppelt werden (Abb. 1). Insbesondere refraktäre oder prognostisch ungünstige Patienten sprachen präferenziell auf die immunonkologische Therapieform an.
Meiner Meinung nach handelt es sich bei der KEYNOTE-204 um eine sehr wichtige Studie, die sogar als «practice changing» eingestuft werden kann. Bleibt nur zu hoffen, dass die Zulassungsbehörden dem schnell folgen werden. Zumindest sollte aber eine Kostenrücksprache mit den Krankenkassen versucht werden.
Die ASPEN-Studie verglich die BTK-Inhibitoren Zanubrutinib und Ibrutinib bei Patienten mit Morbus Waldenström. Wie schätzen Sie die Ergebnisse dieser Studie ein?
C. Renner: Generell stehen derzeit drei Bruton-Tyrosinkinase(BTK)-Inhibitoren zur Verfügung, und zwar Zanubrutinib, Ibrutinib und Acalabrutinib, wobei Ibrutinib am breitesten eingesetzt wird.
Beim Morbus Waldenström (MW) ist Ibrutinib in der Rezidivtherapie zugelassen. In der ASPEN-Studie wurde Zanubrutinib versus Ibrutinib in der Primärtherapie verglichen. Das PFS und das Gesamtüberleben (OS) zeigten sich äquivalent, die Ansprechraten zeigten einen leichten Vorteil für Zanabrutinib.
Ein signifikanter Unterschied konnte jedoch bei den Nebenwirkungen beobachtet werden. Unter Zanabrutinib wurden im Vergleich zu Ibrutinib eher Neutropenien, nicht aber mehr schwere Infekte beobachtet. Interessant ist, dass deutlich weniger kardiale Nebenwirkungen unter Zanabrutinib auftraten. Die Rate an Vorhofflimmern war signifikant niedriger und hat sich nicht akkumuliert. Hypertensive Krisen und Vorhofflimmern stellen ja ein grosses Problem unter der Therapie mit Ibrutinib dar.
Zusammenfassend zeigen beide BTK-Inhibitoren ein ähnliches Wirkungsprofil, jedoch wurde unter Zanabrutinib eine geringere Toxizität beobachtet. Bei entsprechender Zulassung könnte ich mir vorstellen, dass bevorzugt Zanabrutinib als BTK-Inhibitor zur Anwendung kommen wird.
Bei Patienten mit rezidiviertem follikulärem Lymphom oder Marginalzonen-Lymphom wurde die CAR-T-Zell-Studie ZUMA-5 präsentiert. Wie sehen Sie diese Ergebnisse?
C. Renner: Es wurde eine Interimsanalyse der Phase-II-Studie ZUMA-5 präsentiert, die die «Chimeric antigen receptor»(CAR)-T-Zell-Therapie Axicabtagen Ciloleucel (Axi-cel) bei Patienten mit rezidiviertem follikulärem Lymphom oder Marginalzonen-Lymphom untersucht.
Es konnten sehr hohe Ansprechraten erzielt werden. Etwas enttäuschend ist für mich jedoch das PFS von 24 Monaten beim follikulären Lymphom und von 12 Monaten beim Marginalzonen-Lymphom. Allerdings ist die Nachbeobachtungszeit noch nicht sehr lang und es handelt sich um stark vorbehandelte Patienten. Die Wirksamkeit ist gegeben, es wurde allerdings kein Plateau wie bei aggressiven Lymphomen erzielt.
Ob diese Daten für eine Zulassung ausreichen werden, wird sich noch zeigen. Die Toxizität blieb im erwarteten Rahmen. Ein Drittel der Patienten litt unter zum Teil schweren Nebenwirkungen wie dem Zytokin-Freisetzungssyndrom und Neurotoxizität, was bei Erkrankungen, die bisher eher im indolenten Bereich verortet werden, nicht unwesentlich ist. Es müsste also sowohl die Wirksamkeit als auch die Toxizität entscheidend verbessert werden.
Der Stellenwert von Axi-cel in der Therapie des rezidivierten follikulären Lymphoms oder des Marginalzonen-Lymphoms ist dementsprechend noch schwer einzuschätzen, u.a. auch angesichts des Aufkommens anderer neuer Therapieoptionen wie der Tyrosinkinase-Inhibitoren (TKI) oder der BTK-Inhibitoren.
In der ALPHA-Studie wurden allogene Anti-CD19-CAR-T-Zell-Produkte bei Patienten mit rezidiviertem grosszelligem B-Zell-Lymphom (DLBCL) oder follikulärem Lymphom getestet. Wie schätzen Sie diesen Ansatz ein?
C. Renner: Bei allogenen CAR-T-Zell-Produkten handelt es sich um Zellen, welche ursprünglich von einem gesunden Spender entnommen wurden. Dies bietet einige entscheidende Vorteile: Das Produkt kann im Voraus hergestellt und gelagert werden, womit bei Bedarf jederzeit auf ein bereits fertiges Produkt zurückgegriffen werden kann. Ausserdem liesse sich so eine Kostensenkung erzielen.
Um Unverträglichkeitsreaktionen zu vermeiden, wurde der endogene T-Zell-Rezeptor ausgeschaltet. Ebenso wurde das CD52-Antigen ausgeschaltet, um damit die Lymphodepletion mittels eines Anti-CD52-Antikörpers zu verbessern.
In der ALPHA-Phase-I-Studie wurden 9 Patienten mit rezidiviertem grosszelligem B-Zell-Lymphom oder follikulärem Lymphom behandelt. Die Ansprechrate lag bei knapp 75%. Die Verträglichkeit blieb im zu erwartenden Masse und es traten keine schweren Graft-versus-Host-Reaktionen auf.
Dieser Ansatz eines allogenen CAR-T-Zell-Produktes, welches mit Gene Silencing hergestellt wird, wurde von einem erfahrenen Team entwickelt und ist aufgrund der oben genannten Vorteile eines allogenen Produktes hochspannend. Da die Langzeitdaten fehlen, ist es jedoch noch zu früh, um ein abschliessendes Urteil fällen zu können.
Die Phase-I-Studie Alexander untersuchte bei rezidivierten DLBCL-Patienten CD19/CD22-gerichtete CAR-T-Zellen mit einem PD-1-Inhibitor. Was waren die Ergebnisse dieser Studie?
C. Renner: Bei der Weiterentwicklung der autologen CAR-T-Zell-Therapie steht vor allem im Mittelpunkt, die Toxizität zu reduzieren und Resistenzen und refraktäre Situationen zu verhindern. In der Phase-I-Studie Alexander wurde an Patienten mit rezidiviertem/refraktärem DLBCL (r/r DLBCL) ein CAR-T-Zell-Produkt getestet, welches sowohl gegen CD19 als auch CD22 gerichtet ist. Somit könnte der Verlust eines der beiden Antigene aufgefangen werden. Das neue CAR-T-Zell-Konstrukt zeigte eine gute Verträglichkeit, mit geringem Auftreten des Zytokin-Freisetzungssyndroms und geringer Neurotoxizität.
Zusätzlich wurde der PD-1-Inhibitor Pembrolizumab verabreicht, um zu verhindern, dass T-Zellen im Tumor ausgeschaltet werden. Da dies nicht randomisiert erfolgt ist, lässt sich der Nutzen dieser kombinierten Therapie noch nicht abschätzen. Die Pembrolizumab-Gabe erfolgte jedenfalls an Tag –1, d.h. am Tag vor der Verabreichung der autologen CAR-T-Zell-Therapie.
Es handelt sich hier also um eine technisch aufwendige, aber sehr interessante Variante der CAR-T-Zell-Therapie. In weiterführenden Studien soll das Konstrukt in der ambulanten Therapie getestet werden, was schon allein aus Kostengründen fantastisch wäre. Für ein abschliessendes Urteil ist es meiner Meinung nach aber noch zu früh.
Mithilfe der Datenbank des Center for International Blood and Marrow Transplant Research (CIBMTR) wurde der Stellenwert der ASCT bei rezidivierten, chemosensitiven Patienten mit DLBCL untersucht. Wie würden Sie diese Ergebnisse interpretieren?
C. Renner: Es handelte sich hierbei um eine retrospektive Analyse, die zeigte, dass die Häufigkeit, mit der eine ASCT nach vorhergegangener Hochdosis-Chemotherapie bei Patienten mit DLBCL im Rezidiv verabreicht wurde, in den letzten Jahren massiv abgenommen hat. Die entsprechenden Zahlen sind um bis zu 45% eingebrochen. Als Erklärung bietet sich hier an, dass viele Patienten nun direkt einer CAR-T-Zell-Therapie zugeführt werden. Es gibt allerdings keine Studie, die diese Vorgehensweise unterstützt, sondern es handelt sich um eine gefühlsbasierte Entscheidung, die nicht wissenschaftlich untermauert ist.
Die Analyse zeigte, dass die Patienten unter Hochdosis-Chemotherapie und ASCT in der PET/CT (Positronen-Emissionstomografie/Computertomografie) eine komplette oder partielle Remission und mit Abstrichen eine Plateau-Phase erreichen können. Die langfristige PFS-Rate liegt bei gut 40%.
Es gilt also nach wie vor, dass rezidivierte DLBCL-Patienten mit chemosensitiver Erkrankung eine Hochdosis-Chemotherapie mit ASCT erhalten sollten. Laufende 1:1-randomisierte Studien, in welchen der Standard mit der CAR-T-Zell-Therapie verglichen wird, sollten meiner Meinung nach auf jeden Fall abgewartet werden, ehe die gängige Praxis geändert wird.
Das könnte Sie auch interessieren:
Adjuvantes Osimertinib reduziert ZNS-Rezidive bei EGFR-mutierter Erkrankung
Etwa 30% der Patienten mit nicht kleinzelligem Lungenkarzinom (NSCLC) präsentieren sich mit resezierbarer Erkrankung und werden einer kurativen Operation unterzogen. Viele Patienten ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...