Beeindruckende Ergebnisse mit großer klinischer Relevanz
Autor:
OA Dr. Maximilian Hochmair
Leiter der pneumo-onkologischen Ambulanz und Tagesklinik
Abteilung für Innere Medizin und Pneumologie
Karl Landsteiner Institut für Lungenforschung und pneumologischeOnkologie, Klinik Floridsdorf, Wien
Am diesjährigen ASCO-Kongress war das Angebot an Studien zum Lungenkarzinom wieder sehr groß und es ist nicht einfach, eine Auswahl zu treffen. Ich habe Studien mit klinischer Relevanz herausgesucht, unter anderem aus den Bereichen „Early Stage“ und „Targeted Therapy“ beim nicht kleinzelligen Lungenkarzinom sowie zum kleinzelligen Lungenkarzinom, die ich im Folgenden vorstelle.
NeoADAURA: neoadjuvante Therapie mit Osimertinib
Die NeoADAURA-Studie entstand unter unserer Co-Autorenschaft, weshalb ich allen Zuweiser:innen danke, die dazu beigetragen haben. Untersucht wurde, ob die neoadjuvante Gabe des EGFR-TKI Osimertinib (Osi) bei resezierbarem EGFR-mutiertem nichtkleinzelligem Lungenkarzinom (NSCLC) das chirurgische und das Langzeit-Outcome verbessern kann. Eingeschlossen waren mehr als 350 Patient:innen mit resezierbarem NSCLC der Stadien II–IIIB. Sie wurden 1:1:1 randomisiert und erhielten Osi mono, Osi plus Chemotherapie (CTx) oder CTx plus Placebo. Anschließend erfolgte die Operation, gefolgt von drei Jahren adjuvanter Osi-Therapie. Primärer Endpunkt war die MPR („major pathological response“). Zu den sekundären Endpunkten gehörten die komplette pathologische Remission (pCR), das ereignisfreie Überleben (EFS) und die Sicherheit.1
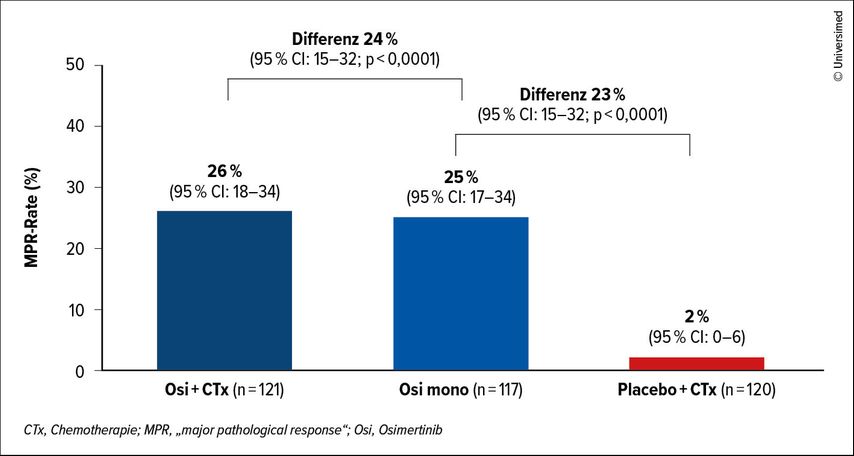
Nach der neoadjuvanten Therapie konnten 92% (Osi+CTx), 97% (Osi mono) und 89% (CTx) der Patient:innen operiert werden, wobei in jeweils mehr als 90% (Osi mono: 95%) der Fälle eine R0-Resektion möglich war. Insgesamt erhielten 91% der Operierten anschließend eine adjuvante Osi-Therapie. Die MPR-Raten betrugen 26% (Osi+CTx), 25% (Osi mono) und 2% (CTx) (Abb.1). Zudem konnte in den Osi-Armen in mehr als 50% der Fälle ein Downstaging erreicht werden (vs. CTx 21%). Die Nebenwirkungen waren konsistent mit früheren Studien.1
Abb. 1: NeoADAURA-Studie: signifikant höhere MPR-Raten in den Osimertinib-Armen im Vergleich zur Chemotherapie (modifiziert nach He J et al.)2
Das Fazit lautet, dass eine neoadjuvante Osi-Therapie mit/ohne Chemotherapie geeigneten NSCLC-Patient:innen angeboten werden sollte.1
ALNEO: Alectinib neoadjuvant beiALK-positivem NSCLC
Ebenfalls sehr interessant war die finale Auswertung der Phase-II-Studie ALNEO, die die neoadjuvante Therapie mit Alectinib bei ALK-positivem NSCLC untersuchte. Eingeschlossen waren 33 Patient:innen mit resezierbarem ALK-transloziertem NSCLC im Stadium III, von denen 28 operiert wurden. Das Design war ähnlich wie bei NeoADAURA: zunächst neoadjuvant Alectinib, gefolgt von der Operation und adjuvanter Alectinib-Therapie. Primärer Endpunkt war die MPR, sekundäre Endpunkte waren unter anderem pCR, EFS und Sicherheit. Die MPR-Rate lag bei 46% (n=15), die pCR-Rate bei 12% (n=4). In 48% der Fälle konnte ein Downstaging erzielt werden.3 Obwohl es nur eine kleine Studie ist, sind die Resultate eindeutig klinisch relevant.
CheckMate 816: Langzeit-OS-Daten
Von dieser Studie wurden die mit Spannung erwarteten 5-Jahres-Daten zum Gesamtüberleben (OS) präsentiert. Eingeschlossen waren NSCLC-Patient:innen der Stadien IB–IIIA ohne EGFR- und ALK-Veränderungen. Sie erhielten neoadjuvant entweder Nivolumab (Nivo) plus CTx oder nur CTx, anschließend wurden sie operiert und optional adjuvant weiterbehandelt. Das OS war ein Haupt-Sekundärendpunkt.
Bei einer medianen Nachbeobachtungszeit von 68 Monaten ergab sich für Nivo/CTx ein statistisch signifikanter OS-Vorteil im Vergleich zur alleinigen CTx (Median nicht erreicht [NR] vs. 73,7 Mo.; p=0,0479). Die OS-Raten betrugen 65% vs. 55%, wobei Patient:innen in höheren Stadien und mit PD-L1-Positivität am meisten von Nivo profitierten. Dabei hatten Patient:innen, die mit Nivo+CTx eine pCR erreichen konnten, eine nachhaltigere OS-Verlängerung im Vergleich zu jenen ohne pCR, mit 5-Jahres-OS-Raten von 95% vs. 56%. Auch das EFS war im Vergleich zur CTx weiterhin verlängert (59,6 vs. 21,1 Mo.); die 5-Jahres-EFS-Raten lagen bei 49% vs. 34%. Neue Sicherheitssignale wurden nicht beobachtet.4
CheckMate 77T: Update zum EFS und erster OS-Trend
Für diese der Studie CheckMate 816 ähnliche Studie mit neoadjuvanter Gabe von Nivo + CTx vs. CTx bei resektablem NSCLC wurden ein Update zum langfristigen EFS-Vorteil und zur Bedeutung der ctDNA sowie ein erster OS-Trend vorgestellt. Perioperatives Nivo zeigte weiterhin einen langfristigen EFS-Vorteil und einen günstigen OS-Trend im Vergleich zur CTx; neue Sicherheitssignale traten nicht auf. In explorativen Analysen waren die präoperative ctDNA-Clearance und das Erreichen einer pCR mit einem EFS-Vorteil verbunden. Der EFS-Vorteil von Nivo war unabhängig vom KRAS-, STK11- und KEAP1-Mutationsstatus.5
SWOG/NRG S1914: Atezolizumab plus SBRT versus SBRT
Die stereotaktische Radiotherapie (SBRT) ist die Standardbehandlung (SoC) für ein inoperables NSCLC im Frühstadium. In der Phase-III-Studie SWOG/NRG S1914 wurde der SoC verglichen mit dem Zusatz von Atezolizumab (Atezo) zur SBRT.6 Hintergrund waren frühere Daten, die einen Vorteil der kombinierten Therapie für das EFS gezeigt hatten.7 Die Studie wurde nach der ersten Interimsanalyse von 400 Patient:innen gestoppt, da sich weder beim OS noch beim PFS ein Benefit von Atezo gegenüber dem SoC gezeigt hatte. Gleichzeitig war die Rate an Nebenwirkungen im Atezo-Arm deutlich höher.6
HERTHENA-Lung02: negatives Outcome
An dieser Studie waren wir mit fünf Patient:innen beteiligt, weshalb wir die Ergebnisse mit Spannung erwartet haben. Beim EGFR-mutierten NSCLC besteht nach Progress unter einem TKI der 3. Generation Bedarf an Therapien mit höherer Wirksamkeit und vertretbaren Sicherheitsprofilen. Hier kommt die Targeted Therapy mit dem Antikörper-Wirkstoff-Konjugat (ADC) Patritumab Deruxtecan (HER3-DXd) ins Spiel. In der Phase-II-Studie HERTHENA-Lung01 erreichte es Responseraten von 30%.8
In HERTHENA-Lung02 wurden rund 600 NSCLC-Patient:innen eingeschlossen, die unter Osi progredient gewesen waren. Sie wurden randomisiert und erhielten entweder HER3-DXd oder den damaligen SoC, eine platinbasierte CTx. Primärer Endpunkt war das PFS, Hauptsekundärendpunkt das OS. HER3-DXd senkte im Vergleich zur CTx das Progressionsrisiko signifikant (HR: 0,77; 95% CI: 0,63–0,94; p=0,011). Zu Monat 9 lag die PFS-Rate bei 29% (vs. CTx 19%). Die objektive Responserate (ORR) betrug 35,2% (vs. CTx 25,3%). Ob ein PFS-Unterschied von 0,4 Monaten (5,8 vs. 5,4 Mo.) zugunsten des ADC allerdings klinisch relevant ist, ist zu diskutieren. Enttäuschend ist, dass es beim OS (16 vs. 15,9 Mo.) keinen Unterschied der beiden Studienarme gab.9
LOXO-RAS-20001 und KRYSTAL-7: beeindruckendes Ansprechen
LOXO-RAS-20001 untersuchte die Wirksamkeit und Sicherheit von Olomorasib (Olo), einem hochselektiven KRASG12C-Inhibitor, in Kombination mit Pembrolizumab (Pembro) als Erstlinientherapie bei fortgeschrittenem KRASG12C-mutiertem NSCLC. Es zeigte sich ein beeindruckendes Ansprechen mit einer ORR von 74%, bei PD-L1-Positivität ≥50% sogar von 90%, und einer PFS-Rate von 80%. Die Ansprechdauer (DOR) und das mPFS sind bei einer Follow-up-Dauer von 5,6 (DOR) und 7,5 Monaten(mPFS) noch nicht erreicht. Zu beachten sind die Nebenwirkungen – neben Diarrhö vor allem eine Lebertoxizität.10 Derzeit werden Patient:innen für die Zulassungsstudie SUNRAY-01 (Olo/Pembro bei metastasiertem NSCLC) rekrutiert, auch in Österreich.*
Die einarmige Phase-II-Studie KRYSTAL-7 verfolgte das gleiche Konzept wie die LOXO-Studie, wobei hier Adagrasib (Ada) anstelle von Olo eingesetzt wurde. Eingeschlossen waren 149 Patient:innen mit metastasiertem KRASG12C-mutiertem NSCLC. Primärer Endpunkt war die ORR, sekundäre Endpunkte waren unter anderem DOR, PFS und OS. Die ORR über alle PD-L1-Gruppen hinweg lag bei 44%, bei PD-L1 ≥50% gar bei 61%, mit einer 12-Monats-DOR von 73%. Das mPFS betrug 11 Monate mit einer 18-Monats-PFS-Rate von 37,6%; das mOS betrug 18,3 Monate mit einer 18-Monats-OS-Rate von 51,8%. Auch hier profitierten Patient:innen mit hohem PD-L1-Status (≥50%) am meisten.11
TROPION-Lung02: vor Therapie aufTROP2 testen
In dieser Studie wurde in der Erstlinientherapie das TROP2-gerichtete ADC Datopotamab Deruxtecan (Dato-DXd) plus Pembro mit/ohne CTx bei fortgeschrittenem NSCLC untersucht. Primärer Endpunkt war die Sicherheit, sekundärer Endpunkt die Wirksamkeit.
Hauptnebenwirkungen von Dato-DXd/Pembro waren Stomatitis, Übelkeit und Alopezie, bei der Triplet-Therapie vor allem Übelkeit und Anämie. Die ORR unter Dato-DXd/Pembro betrug 55%, das mPFS 11,2 Monate, das mOS wurde noch nicht erreicht. Im Triplet-Arm lag die ORR bei 56%, das mPFS bei 6,8 Monaten und das mOS bei 17,4 Monaten.12 Allerdings waren in diesem Arm auch etwas mehr Patient:innen mit Hirnmetastasen. Man muss sich anschauen, was die Ursache für das doch etwas enttäuschende PFS ist. Es hat sich aber auch gezeigt, dass Patient:innen, die TROP2-positiv waren, mehr von Dato-DXd profitierten als jene, die keinen TROP2-Rezeptor aufwiesen. Daher sollte vor der Dato-DXd-Behandlung immer auf TROP2 getestet werden.
Kleinzelliges Lungenkarzinom
IMforte: Lichtblick für die Patient:innen
Untersucht wurden Lurbinectedin (Lurbi) plus Atezo als Erstlinien-Erhaltungstherapie bei fortgeschrittenem SCLC (ES-SCLC). Dazu erhielten nicht systemisch vorbehandelte SCLC-Patient:innen zuerst eine Induktionstherapie mit Atezo, Carboplatin und Etoposid. Patient:innen, die dadurch eine komplette oder teilweise Remission (CR, PR) oder eine stabile Krankheit (SD) erreichten (438/660), wurden in die Erhaltungsphase aufgenommen und bekamen entweder Lurbi/Atezo oder Atezo. Primäre Endpunkte waren PFS und OS.13
Bei einem medianen Follow-up von 15 Monaten verlängerte die Kombination im Vergleich zur Monotherapie das PFS signifikant (5,4 vs. 2,1 Mo.; p<0,0001). Das Gleiche fand sich beim OS mit 12-Monats-OS-Raten von 56,3 vs. 44,1% und einem mOS unter Lurbi/Atezo von 13,2 vs. 10,6 Monate (p=0,0174).13 Nicht überraschend war die höhere Rate an Nebenwirkungen unter der Kombination, aber für fitte Patient:innen ist sie dennoch eine gute Option.
DeLLphi-304: neuer SoC in der 2nd Line?
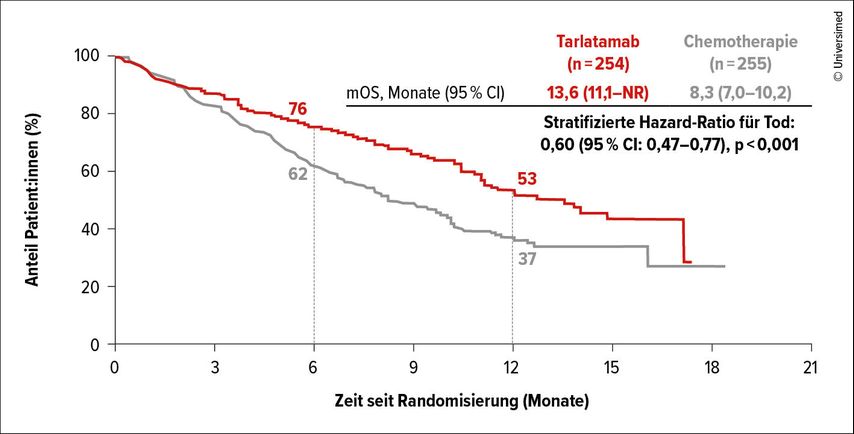
Die DeLLphi-Studie war eines der absoluten Highlights des ASCO-Kongresses. Sie verglich Tarlatamab, einen bispezifischen T-Zell-Engager (BiTE), mit CTx in der Zweitlinie nach Progress unter platinbasierter CTx mit/ohne PD-L1-Inhibitor. Es wurden mehr als 500 SCLC-Patient:innen randomisiert. Die Ergebnisse sind beeindruckend: Bei einer medianen Nachbeobachtungszeit von elf Monaten war das mOS im Tarlatamab-Arm signifikant länger (13,6 vs. 8,3 Mo.; p<0,001) (Abb.2). Das mPFS war unter Tarlatamab ebenfalls signifikant länger als im CTx-Arm (4,2 vs. 3,2 Mo.; p<0,001). Tarlatamab verbesserte im Vergleich zu CTx zudem die krebsbedingten Symptome Dyspnoe und Husten.
Abb. 2: DeLLphi-Studie: signifikant höhere OS-Raten und längeres mOS unter Tarlatamab (modifiziert nach Rudin CM et al.)14
Als Nebenwirkungen wurden vor allem Blutbildveränderungen und unter Tarlatamab das Zytokin-Release-Syndrom (CRS) beschrieben, Letzteres war aber in nur 1% der Fälle von Grad 3. Außerdem trat bei einigen Patient:innen das Immun-Effektorzell-assoziierte Neurotoxizitätssyndrom (ICANS) auf.14 Wenn das Medikament in Österreich zugelassen ist, sind wir daher gefragt, uns und unser Team entsprechend zu schulen, um diese Nebenwirkungen rechtzeitig zu erkennen. Doch Tarlatamab könnte der bevorzugte SoC in der Zweitlinie beim SCLC werden.
* Kontakte für die Zuweisung zur Studie SUNRAY-01:
-
Klinik Floridsdorf, Wien, Tel.: 01 27700 2212
-
Ordensklinikum Linz Elisabethinen, Tel.: 0732 7676 4203
-
Landeskrankenhaus Feldkirch, Tel.: 05522 303 2681
Literatur:
1 Chaft JE et al.: https://doi.org/10.1200/JCO.2025.43.16_suppl.8001 2 He J et al.: JCO2500883 (doi: 10.1200/JCO-25-00883) 3 Leonetti A et al.: https://doi.org/10.1200/JCO.2025.43.16_suppl.8015 4 Forde PM et al.: https://doi.org/10.1200/JCO.2025.43.17_suppl.LBA8000 5 Cascone T et al.: https://doi.org/10.1200/JCO. 2025.43.17_suppl.LBA8010 6 Simone CB et al.: https://doi.org/10.1200/JCO.2025.43.16_suppl.8003 7 Chang JY et al.: Lancet 2023; 402(10405): 871-81 8 Yu HA et al.: J Clin Oncol 2023; 41(35): 5363-75 9 Mok TSK et al.: https://doi.org/10.1200/JCO.2025.43.16_suppl.8506 10 Dragnev KH et al.: https://doi.org/10.1200/JCO.2025.43.16_suppl.8519 11 Jänne PA et al.: https://doi.org/10.1200/JCO.2025.43. 16_suppl.8500 12 Levy BP et al.: https://doi.org/10.1200/JCO.2025.43.16_suppl.8501 13 Paz-Ares LG et al.: https://doi.org/10.1200/JCO.2025.43.16_suppl.8006 14 Rudin CM et al.: https://doi.org/10.1200/JCO.2025.43.17_suppl.LBA8008
Das könnte Sie auch interessieren:
Adjuvantes Osimertinib reduziert ZNS-Rezidive bei EGFR-mutierter Erkrankung
Etwa 30% der Patienten mit nicht kleinzelligem Lungenkarzinom (NSCLC) präsentieren sich mit resezierbarer Erkrankung und werden einer kurativen Operation unterzogen. Viele Patienten ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...