Pulsed Field Ablation – Beginn einer neuen Ära?
Autor:innen:
Dr. Marie Muthspiel
OA Dr. Florian Tinhofer
III. Medizinische Abteilung mit Kardiologie und Intensivmedizin
Klinik Ottakring, Wien
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Mit der Pulsed Field Ablation (PFA) hält ein neuartiges, nichtthermisches, gewebsselektives Ablationsverfahren Einzug in die interventionelle Therapie des Vorhofflimmerns. Aktuelle klinische Daten belegen eine hohe Effektivität bei gleichzeitig günstigem Sicherheitsprofil und eröffnen damit neue Perspektiven für die künftige Standardtherapie der Pulmonalvenenisolation.
Keypoints
-
Die PFA bietet eine im Vergleich zu thermischen Verfahren gleichwertige Wirksamkeit in der Behandlung des paroxysmalen Vorhofflimmerns.
-
Sie überzeugt durch ein günstiges Sicherheitsprofil mit deutlich selteneren thermisch bedingten Komplikationen.
-
Sie ermöglicht sehr kurze Prozedurzeiten bei gleichzeitig einfacher Handhabung.
Abb. 1: Exemplarischer Pulsed Field Ablation Catheter. Image provided courtesy of Boston Scientific
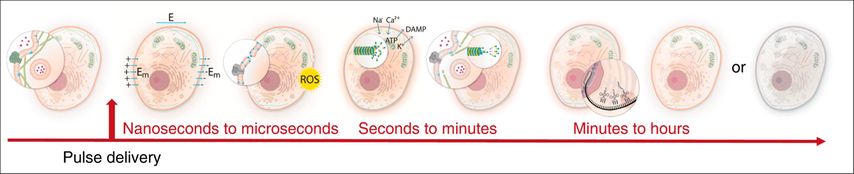
Die weltweit steigende Prävalenz von Vorhofflimmern erhöht die Nachfrage nach effektiven und sicheren Behandlungsmethoden der Pulmonalvenenisolation.1 Die PFA beruht auf dem Prinzip der irreversiblen Elektroporation. Über einen Katheter applizierte elektrische Hochspannungsimpulse erzeugen Defekte in der Zellmembran der Kardiomyozyten, welche zu einem irreversiblen Verlust der Membranintegrität führen (Abb.1). Die daraus resultierenden Elektrolytverschiebungen bewirken einen intrazellulären Anstieg der Kalziumkonzentration. Dies führt, über bislang nicht vollständig verstandene apoptotische und nekrotische Signalwege, innerhalb weniger Sekunden bis Stunden zum Zelltod (Abb.2).2 Der Schwellenwert der irreversiblen Elektroporation variiert je nach Zelltyp und bildet den zentralen Mechanismus, der die selektive Wirkung auf Kardiomyozyten ermöglicht. Da der myokardspezifische Schwellenwert vergleichsweise niedrig ist, werden angrenzende Strukturen wie Nerven, der Ösophagus oder das Gefäßendothel mit höheren Schwellenwerten weitgehend geschont.3
Die PFA ist somit im Gegensatz zu den herkömmlichen Ablationsverfahren wie Radiofrequenzablation (RFA) und Kryoablation (CBA) ein gewebsselektives, nichtthermisches Verfahren.
Effektivität
Aktuelle randomisierte Studien und Metaanalysen belegen, dass die PFA hinsichtlich der Wirksamkeit etablierten thermischen Ablationsverfahren (RFA, CBA) nicht unterlegen ist.3–5 So zeigt die ADVENT-Studie eine vergleichbare 1-Jahres-Erfolgsrate bezüglich der Freiheit von paroxysmalem Vorhofflimmern (PFA 73,3% vs. thermische Ablation 71,3%; Differenz 2,0 Prozentpunkte; 95% BCI: −5,2 bis 9,2) bei gleichzeitig nicht inferiorem Sicherheitsprofil.3 Zudem zeichnet sich die PFA aufgrund ihrer einfacheren Handhabung durch eine signifikant kürzere Prozedurdauer aus (ca. 30–40min.).3
Sicherheitsprofil
Die PFA gilt als nichtthermales, gewebsselektives Verfahren mit einem sehr günstigen Sicherheitsprofil.6 Die ADVENT-Studie zeigt eine insgesamt niedrige und zwischen den Behandlungsgruppen (PFA vs. thermisch) vergleichbare Inzidenz schwerwiegender Komplikationen (2,1% PFA vs. 1,5% thermisch, Differenz 0,6 Prozentpunkte; 95% BCI: −1,5 bis 2,8).3 Erste Real-World-Daten liefert die MANIFEST-17k-Studie.6 Hervorzuheben sind in diesem Zusammenhang insbesondere die Vorteile des Verfahrens hinsichtlich der Gewebeselektivität, die sich in einer äußerst niedrigen Inzidenz schwerwiegender, typischerweise thermisch induzierter Komplikationen, wie Pulmonalvenenstenose, persistierender Phrenikusparese und ösophagealer Fistel, widerspiegeln.6 Aktuelle Daten zeigen zudem, dass die PFA bereits in der frühen Anwendungsphase mit einer niedrigen Komplikationsrate einhergeht. Mit zunehmender Erfahrung verbessert sich die Prozedurensicherheit nur geringfügig. Im Vergleich zu thermischen Verfahren wird das Effizienzplateau somit früher erreicht, was eine sichere Anwendung der PFA auch von weniger erfahrenen Operateur:innen ermöglicht.6 Dies birgt einen wesentlichen Vorteil für eine breite klinische Implementierung mit hoher Sicherheit für Patient:innen.
Eine Elektroporation weiterer Zelltypen, die sich unmittelbar im elektrischen Hochspannungsfeld befinden, wie beispielsweise Erythrozyten, kann dennoch nicht vollständig vermieden werden.3 Im Vergleich zur RFA geht die PFA daher mit einer stärkeren periprozeduralen intravasalen Hämolyse einher. Die Hämolyse ist dosisabhängig und nimmt mit der Anzahl der PFA-Applikationen zu. Dennoch kommt es in der Regel innerhalb von 24 Stunden zu einer Normalisierung der Hämolyseparameter, klinisch relevante renale Komplikationen sind selten (0,03%).7 Ebenso kann die Elektroporation eine Depolarisation von Nervenzellen verursachen. Bedingt durch die anatomische Lagebeziehung liegt die Annahme nahe, dass eine Stimulation des Nervus vagus für die nach PFA beobachtete, reversible Bradykardie verantwortlich ist.8 Die Anwendung von PFA in unmittelbarer Nähe zu den Koronararterien, insbesondere bei Ablationen im Bereich des Mitral- oder Cavotrikuspidalisthmus, kann zudem vaskuläre Veränderungen verursachen. Akute Koronarspasmen treten in bis zu 0,14% der Fälle auf, verlaufen in der Mehrzahl jedoch subklinisch und bilden sich nach Gabe von Nitroglycerin zurück. Gelegentlich können symptomatische Verläufe mit ST-Streckenhebungen und arrhythmischen Ereignissen auftreten. Zudem zeigen intrakoronare Bildgebungsstudien, dass es zu einer leichten, aber signifikanten Verringerung der Koronarlumenfläche in bis zu 3 Monaten nach Ablation kommen kann. Zusammenfassend ist somit die Häufigkeit von Koronarereignissen nach PFA gering, allerdings etwas höher als bei herkömmlichen thermischen Verfahren.9
Herausforderungen und mögliche Limitationen
Bislang wurden keine Subgruppen mit paroxysmalem Vorhofflimmern identifiziert, für die eine Behandlung mittels PFA grundsätzlich ungeeignet wäre. Kollektive mit fortgeschrittener struktureller Herzerkrankung, kardialen Implantaten, stark vergrößertem linkem Vorhof oder ausgeprägter atrialer Fibrose sind allerdings bislang nicht ausreichend untersucht.3 In der Gruppe der Älteren (>75 Jahre) erscheint die PFA wirksam und sicher, insbesondere dürfte diese von der verkürzten Prozedurzeit profitieren. Große, randomisierte Studien zu jenem Patient:innenkollektiv stehen jedoch aus.10 Die Evidenz zur PFA basiert überwiegend auf Settings mit paroxysmalem Vorhofflimmern, sodass die aktuelle Datenlage zu persistierendem Vorhofflimmern, anderen atrialen Rhythmusstörungen oder komplexen Substraten als begrenzt gilt. Erste randomisierte, prospektive Studien wie ADVANTAGE AF zeigen jedoch vielversprechende Ergebnisse hinsichtlich der 1-Jahres-Erfolgsraten.11 Die derzeit noch eingeschränkte Verfügbarkeit von Ablationskathetern zur Durchführung linearer Ablationen limitiert allerdings aktuell den Einsatz dieser Technik abseits der Pulmonalvenen.
Zukunftsperspektiven
Angesichts der kurzen Prozedurzeiten legen gesundheitsökonomische Analysen nahe, dass die PFA kostengünstiger ist als herkömmliche, thermische Verfahren.12 Dank ihrer vergleichsweise einfachen Handhabung, der geringen Komplikationsrate und einer möglichen Indikationserweiterung auf persistierendes Vorhofflimmern und andere atriale Rhythmusstörungen positioniert sich die PFA zunehmend als vielversprechende Alternative und in manchen Bereichen sogar als neuer Standard der Katheterablation. Eine weitere innovative Methode der Pulmonalvenenisolation, die duale Energieablation mit RFA und PFA, wird aktuell hinsichtlich höherer Effektivität bei gleichzeitiger Reduktion von Komplikationen in der SmartfIRE-Studie evaluiert.13
Literatur:
1 Linz D et al.: Atrial fibrillation: epidemiology, screening and digital health. Lancet Reg Health Eur 2024; 37: 100786 2 Chun KJ et al.: State-of-the-art pulsed field ablation for cardiac arrhythmias: ongoing evolution and future perspective. Europace 2024; 26(6): euae134 3 Reddy VY et al.: Pulsed field or conventional thermal ablation for paroxysmal atrial fibrillation. N Engl J Med 2023; 389(18): 1660-71 4 Reichlin T et al.: Pulsed field or cryoballoon ablation for paroxysmal atrial fibrillation. N Engl J Med 2025; 392(15): 1497-507 5 Mariani MV et al.: Pentaspline pulsed field ablation versus high-power short-duration/very high-power short-duration radiofrequency ablation in atrial fibrillation: a meta-analysis. J Cardiovasc Electrophysiol 2025; 36(9): 2165-78 6 Ekanem E et al.: Safety of pulsed field ablation in more than 17,000 patients with atrial fibrillation in the MANIFEST-17K study. Nat Med 2024; 30(7): 2020-9 7 Osmancik P et al.: Periprocedural intravascular hemolysis during atrial fibrillation ablation: a comparison of pulsed field with radiofrequency ablation. JACC Clin Electrophysiol 2024; 10(7 Pt 2): 1660-71 8Tohoku S et al.: Impact of pulsed-field ablation on intrinsic cardiac autonomic nervous system after pulmonary vein isolation. JACC Clin Electrophysiol 2023; 9(9): 1864-75 9 Tam MTK et al.: Effect of pulsed-field ablation on human coronary arteries: a longitudinal study with intracoronary imaging. JACC Clin Electrophysiol 2025; 11(7): 1478-88 10 Nakasone K et al.: Pulsed field ablation in the elderly by a pentaspline multielectrode catheter: safety, efficacy, and comparison with cryoballoon and radiofrequency devices. Heart Rhythm 2025; 22(7): e30-e9 11 Reddy VY et al.: Pulsed field ablation for persistent atrial fibrillation: 1-year results of ADVANTAGE AF. J Am Coll Cardiol 2025; 85(17): 1664-78 12 Soleimani H et al.: Cost comparison of pulsed field ablation and conventional thermal ablation for atrial fibrillation: a systematic review. Pacing Clin Electrophysiol 2025; doi: 10.1111/pace.70081 13 De Potter T et al.: Dual energy for pulmonary vein isolation using focal ablation technology integrated with a three-dimensional mapping system: SmartfIRE 12-month results. Europace 2025; 27(9): euaf174
Das könnte Sie auch interessieren:
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
HFrEF: von der 4-Säulen-Therapie zur individualisierten Versorgung
In den letzten Jahren haben sich die therapeutischen Optionen bei HFrEF verändert. Neue Wirkstoffklassen, rasche Aufdosierungsalgorithmen und ein immer individualisierterer Ansatz prägen ...