„Gene silencing“ bei ATTR-Kardiomyopathie
Autor:innen:
Dr. Katharina Singer, LL.M., B.Sc.
Priv.-Doz. Dr. Christian Nitsche, PhD
Medizinische Universität Wien,
Universitätsklinik für Innere Medizin II,
Klinische Abteilung für Kardiologie
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Mit der Zulassung von Vutrisiran steht erstmals ein Transthyretin-Silencer für die Therapie der Transthyretin-Amyloidose mit Kardiomyopathie zur Verfügung. Mit Eplontersen und Nucresiran befinden sich weitere Silencer im Entwicklungsstand einer Phase-III-Studie. Im Folgenden eine Übersicht der verfügbaren und sich in Entwicklung befindlichen Silencer-Therapien sowie mögliche Implikationen für die Praxis.
Keypoints
-
TTR-Silencer hemmen die hepatische Transthyretinsynthese auf mRNA-Ebene und senken den Serum-TTR-Spiegel um ≥80%.
-
Vutrisiran reduzierte in der HELIOS-B-Studie die Gesamtmortalität und kardiovaskuläre Ereignisse signifikant, auch unter begleitender Tafamidis-Therapie.
-
Die Outcomedaten von Eplontersen werden für August 2026 erwartet.
-
Zukünftige Substanzen könnten von halbjährlich verabreichter siRNA über einmalige CRISPR-Cas9-basierte Therapien bis zu Amyloid-Depletern reichen.
-
Eine mögliche Kombination verschiedener Wirkmechanismen ist zu evaluieren.
Warum Silencer? Die pathophysiologische Rationale
Transthyretin (TTR) wird vorwiegend in der Leber synthetisiert und zirkuliert in Form eines Homotetramers im Serum. Bei der kardialen Transthyretin-Amyloidose (ATTR-CM) dissoziieren diese Tetramere in Mono- und Dimere, die sich im Herzmuskelgewebe zu sogenannten Amyloidfibrillen zusammenlagern können. Die Folge ist eine progrediente, infiltrative Kardiomyopathie mit diastolischer Funktionseinschränkung. Im Verlauf kann es zu Reizleitungsstörungen, anderen Herzrhythmusstörungen und systolischer Funktionseinschränkung kommen.1
TTR-Stabilisierer (Tafamidis, Acoramidis) verhindern die Tetramerdissoziation bis zu >90%. Für diese Substanzgruppe konnten bereits signifikante prognostische Verbesserungen bei Patient:innen mit ATTR-CM nachgewiesen werden.2,3
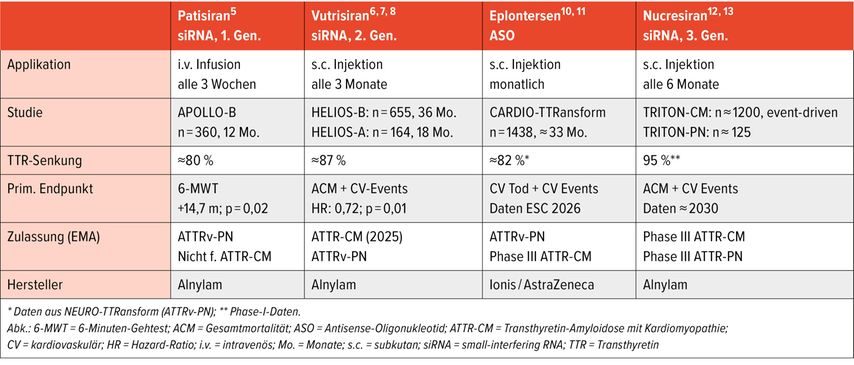
Silencer-Therapien setzen an früherer Stelle des Amyloid-Lebenszyklus an. Sie hemmen die TTR-Synthese auf Messenger-Ribonukleinsäure(mRNA)-Ebene und senken damit den Serum-TTR-Spiegel um 80–95%. Zwei Technologien stehen zur Verfügung: Antisense-Oligonukleotide (ASO; Inotersen, Eplontersen) und „small-interfering“ RNA (siRNA; Patisiran, Vutrisiran, Nucresiran). Beiden Mechanismen liegt eine Degradierung der mRNA zugrunde, die für TTR codiert. Die therapeutischen Strategien der Tetramerstabilisierung, Syntheseblockade und Fibrillenentfernung sind im Positionspapier der Europäischen Gesellschaft für Kardiologie (ESC) zur ATTR-CM zusammengefasst.4 Die raschen Entwicklungen auf diesem Gebiet machen sich auch im Applikationsmodus bemerkbar. Während Patisiran noch eine intravenöse Infusion alle drei Wochen erfordert, kommt man bei Vutrisiran mit einer vierteljährlichen subkutanen Injektion aus, und die nächste Generation Nucresiran soll nur noch halbjährlich subkutan verabreicht werden (Tab.1).
APOLLO-B: Lehren aus der ersten Generation
Patisiran, die siRNA der ersten Generation, wurde in der APOLLO-B-Studie bei 360 Patient:innen mit ATTR-CM durch intravenöse Infusion alle drei Wochen evaluiert. Nach zwölf Monaten zeigte sich eine Verbesserung der 6-Minuten-Gehstrecke (+14,7m vs. Placebo; p=0,02), harte klinische Endpunkte wurden jedoch nicht signifikant beeinflusst.5 Die kurze Studiendauer und geringe Fallzahl dürften die entscheidenden Limitationen gewesen sein. Dennoch lieferte APOLLO-B wichtige Hinweise auf positive Effekte der TTR-Senkung auf kardiale Biomarker und funktionelle Parameter, die den Weg für die größer angelegte HELIOS-B-Studie ebneten.
HELIOS-B: Vutrisiran überzeugt
In der HELIOS-B-Studie wurden 655 Patient:innen mit ATTR-CM 1:1 in Gruppen mit Vutrisiran (s.c. alle drei Monate) oder Placebo randomisiert. Rund 40% erhielten begleitend Tafamidis. Der primäre Kompositendpunkt aus Gesamtmortalität und wiederkehrenden kardiovaskulären Ereignissen nach 36 Monaten wurde in der Gesamtpopulation (HR: 0,72; p=0,01) und in der Monotherapiegruppe (HR: 0,67; p=0,02) erreicht.6
Eindrucksvollerweise sank die Gesamtmortalität nach 42 Monaten um 35% (HR: 0,65; 95%CI: 0,46–0,90; p=0,01). Die 6-Minuten-Gehstrecke verbesserte sich um 26,5m (Gesamtpopulation) bzw. 32,1m (Monotherapie), der Kansas City Cardiomyopathy Questionnaire Score (KCCQ-OS) um 5,8 bzw. 8,7 Punkte. Die Serum-TTR-Spiegel fielen rasch um ca. 87% und blieben über 30 Monate stabil gesenkt.6 Eine sekundäre echokardiografische Analyse bestätigte zudem, dass Vutrisiran die Zunahme der LV-Wanddicke und der LV-Masse bremst und den Abfall der Ejektionsfraktion sowie des „global longitudinal strain“ abschwächt.7
Eine kürzlich publizierte Metaanalyse der kardiovaskulären Outcomestudien bei ATTR-CM (ATTR-ACT, ATTRibute, APOLLO-B, HELIOS-B) zeigt: früh nach Therapiebeginn feststellbare Verbesserungen bei Biomarkern, Lebensqualität und funktioneller Kapazität führen bei ausreichender Therapiedauer zu einer Reduktion der Mortalität um 28% und der kardiovaskulären Ereignisse um 42%.9 Dabei ist jedoch zu beachten, dass sich die Studienpopulationen der einzelnen Studien signifikant hinsichtlich des Ausgangsrisikoprofils unterschieden und demnach keinen 1:1-Vergleich erlauben.
Eplontersen: monatliche Selbstinjektion in Phase-III-Studie
In der NEURO-TTRansform-Studie wurde die Effektivität von Eplontersen (ASO) bei Patient:innen mit hereditärer ATTR-Polyneuropathie getestet und es konnte eine signifikante Verbesserung der Neuropathiescores gegenüber Placebo gezeigt werden.10 Explorative Analysen bei Patient:innen mit gemischtem Phänotyp (Polyneuropathie und Kardiomyopathie) lieferten zudem Hinweise auf eine Stabilisierung kardialer Parameter und lieferten die Grundlage für die CARDIO-TTRansform-Studie.
In CARDIO-TTRansform werden 1438 Patient:innen mit ATTR-CM 1:1 auf Eplontersen (monatliche s.c. Selbstinjektion) oder Placebo randomisiert. Der primäre Endpunkt umfasst kardiovaskuläre Mortalität und wiederkehrende kardiovaskuläre Ereignisse bis Woche 140.11 Die Veröffentlichung der Ergebnisse werden für den ESC-Kongress 2026 in München erwartet.
Nucresiran: die dritte siRNA-Generation am Horizont
Nucresiran ist ein siRNA-Therapeutikum der 3.Generation, das in Phase-I-Studiendaten eine TTR-Senkung von über 95% bei halbjährlicher subkutaner Gabe gezeigt hat. Die TRITON-CM-Studie, eine globale, ereignisgesteuerte Phase-III-Studie, untersucht Nucresiran bei rund 1200 Patient:innen mit ATTR-CM (sowohl wildtyp [wt] als auch hereditär [v]). Der primäre Endpunkt ist eine Komposition aus Gesamtmortalität und kardiovaskulären Ereignissen. Eine Hintergrundtherapie mit TTR-Stabilisierern ist erlaubt. Die amerikanische Behörde für Lebens- und Arzneimittel (FDA) hat Nucresiran den „Fast-track“-Status für ATTR-CM verliehen. Ergebnisse werden für 2030 erwartet.12
Was kommt als Nächstes?
Neben den beschriebenen Substanzen sollten die Wirkmechanismen der CRISPR-Cas9-basierten Gentherapie und der Antikörper-basierten Amyloidentfernung („depleter“) Erwähnung finden. Die CRISPR-Cas9-basierte Substanz NTLA-2001 wird in der MAGNITUDE-Studie getestet und strebt durch einmalige Verabreichung eine dauerhafte Ausschaltung des Transthyretinproteins an.14 Andererseits befindet sich mit dem Antikörper NI006/ALXN2220 in der DepleTTR-Studie erstmals ein Amyloid-„Depleter“ in einer Phase-III-Studie.15
Praxistipp
Die frühzeitige Überweisung an ein spezialisiertes Amyloidosezentrum und die zeitnahe Einleitung einer adäquaten Therapie sind zentrale Voraussetzungen für eine optimale Versorgung. Es stehen derzeit drei Substanzen mit zwei Wirkmechanismen für die Therapie der ATTR-CM zur Verfügung. Die richtige Patient:innenselektion für die jeweilige Substanz stellt eine Herausforderung dar und wird nicht selten von Fragen der Kostenrückerstattung geprägt. Bitte beachten Sie: Da alle Silencer über die TTR-Senkung auch die Retinol-Transportkapazität reduzieren, wird eine begleitende Vitamin-A-Supplementierung empfohlen.Die Pipeline ist also breit gefächert: Von der halbjährlichen siRNA (Nucresiran) über das einmalige Gen-Editing (NTLA-2001) bis zur Amyloidentfernung (NI006) werden ganz unterschiedliche Angriffspunkte verfolgt.
In der klinischen Praxis stellt sich zunehmend die Frage, ob Kombinationstherapien den Einzelsubstanzen überlegen sind. Diese Frage wird derzeit jedoch aus Gründen der Kostenerstattung in den Hintergrund gedrängt. Gerade vor dem Hintergrund neuer Therapieoptionen gewinnen eine strukturierte Risikostratifikation und Patient:in-nenselektion zunehmend an Bedeutung. Rezent können durch eine Erweiterung des „National Amyloidosis Centre“(NAC)-Stagingsystems Patient:innen mit besonders hohem Risiko für frühe Mortalität identifiziert werden. Diese Gruppe könnte womöglich von einer intensivierten Therapiestrategie profitieren.16
Die Erfahrung in großen tertiären Zentren mit Amyloidoseschwerpunkt zeigt, dass frühzeitige Diagnose und rasche Therapieeinleitung weiterhin die größte Herausforderung, aber gleichzeitig eine Möglichkeit für größtmöglichen Nutzen darstellen. Optimale Patient:innenselektion für ein sich ausweitendes Spektrum an verfügbaren Substanzen und die Sicherstellung der Kostenerstattung bleiben weiterhin zentrale Herausforderungen.
Literatur:
1 Ruberg FL et al.: Transthyretin amyloid cardiomyopathy: JACC state-of-the-art review. J Am Coll Cardiol 2019; 73(22): 2872-91 2 Maurer MS et al.: Tafamidis treatment for patients with transthyretin amyloid cardiomyopathy. N Engl J Med 2018; 379(11): 1007-16 3 Gillmore JD et al.: Efficacy and safety of Acoramidis in transthyretin amyloid cardiomyopathy. N Engl J Med 2024; 390(2): 132-42 4 Garcia-Pavia P et al.: Diagnosis and treatment of cardiac amyloidosis. A position statement of the ESC working group on myocardial and pericardial diseases. Eur Heart J 2021; 42(16): 1554-68 5 Maurer MS et al.: Patisiran treatment in patients with transthyretin cardiac amyloidosis. N Engl J Med 2023; 389(17): 1553-65 6 Fontana M et al.: Vutrisiran in patients with transthyretin amyloidosis with cardiomyopathy. N Engl J Med 2025; 392(1): 33-44 7 Jering KS et al.: Effects of Vutrisiran on cardiac structure and function in ATTR-CM: secondary outcomes of HELIOS-B. Nat Med 2025; 31(10): 3560-8 8 Alnylam Pharmaceuticals: HELIOS-A: A Study of Vutrisiran (ALN-TTRSC02) in Patients With Hereditary Transthyretin Amyloidosis (hATTR Amyloidosis). NCT03759379 9 Autherith M et al.: Amyloid-specific medication in transthyretin amyloid cardiomyopathy: a systematic review and meta-analysis of cardiovascular outcome trials. J Card Fail 2025; doi: 10.1016/j.cardfail.2025.08.002 10 Coelho T et al.: Eplontersen for hereditary transthyretin amyloidosis with polyneuropathy. JAMA 2023; 330(15): 1448-58 11 Ionis Pharmaceuticals, Inc.: CARDIO-TTRansform: A study to evaluate the efficacy and safety of Eplontersen (formerly known as ION-682884, IONIS-TTR-LRx and AKCEA-TTR-LRx) in participants with transthyretin-mediated amyloid cardiomyopathy (ATTR CM). NCT04136171 12 Alnylam Pharmaceuticals: TRITON-CM – a study to evaluate Nucresiran in patients with transthyretin amyloidosis with cardiomyopathy. NCT07052903 13 Alnylam Pharmaceuticals: TRITON-PN: A Phase 3 Study to Evaluate the Efficacy and Safety of Nucresiran in Patients with Hereditary Transthyretin Amyloidosis with Polyneuropathy. NCT07223203 14 Intellia Therapeutics: MAGNITUDE: A phase 3 study of NTLA-2001 in participants with transthyretin amyloidosis with cardiomyopathy (ATTR-CM). NCT06128629 15 Alexion Pharmaceuticals, Inc.: Study of ALXN2220 versus placebo in adultswith ATTR-CM (depleTTR-CM). NCT06183931 16 Nitsche C et al.: Expansion of the national amyloidosis centre staging system to detect early mortality in transthyretin cardiac amyloidosis. Eur J Heart Fail 2024; 26(9): 2008-12
Das könnte Sie auch interessieren:
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
Sekundärprävention 2026
Die Mortalitätsrate des akuten Herzinfarktes (Nicht-ST- und ST-Hebungsinfarkt) ist trotz einer immer älter werdenden Bevölkerung zurückgegangen. Von 2011 bis 2022 ist sie bei Frauen um ...