Rezidivierende Polyposis nasi
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die chronische Rhinosinusitis mit Polyposis nasi ist nach dem bisherigen Behandlungsalgorithmus oft nicht ausreichend therapierbar und Rezidive sind häufig zu beobachten. Biologika, die auf bestimmte Entzündungsmediatoren abzielen, stellen hier eine vielversprechende Therapieoption dar.
Keypoints
-
CRSwNP ist mit herkömmlichen Therapieregimen oft nicht ausreichend behandelbar und hat deutliche Auswirkungen auf die Lebensqualität.
-
Insbesondere Patienten, die zusätzlich an Asthma oder NERD erkrankt sind, leiden häufig an Rezidiven.
-
IgE, die Zytokine IL-5, IL-33, TSLP sowie die Zytokinrezeptoren IL-4Rα und IL-5Rα spielen eine Schlüsselrolle in Typ-2-Entzündungsreaktionen bei CRSwNP und Asthma und sind das Ziel von Antikörpertherapien.
-
Die Anwendung von Biologika wird ein neues Zeitalter in der Behandlung der CRSwNP einleiten.
Chronische Rhinosinusitis mit Polyposis nasi
Die chronische Rhinosinusitis (CRS) ist eine häufige, komplexe und sehr heterogene Erkrankung. Obwohl die Prävalenzen sehr unterschiedlich angegeben werden, kann man davon ausgehen, dass zwischen 6 und 11% der Bevölkerung in Europa unter chronischen Nebenhöhlenbeschwerden leiden.1, 2 Die Symptome sind weitreichend. Neben einer Behinderung der Nasenatmung und Riechminderung, übermäßiger Sekretion und Schmerzen im Bereich der Nebenhöhlen können auch Auswirkungen auf die Konzentrations- und Leistungsfähigkeit sowie Schlafstörungen bestehen. Hierdurch entstehen hohe Kosten für das Gesundheitssystem, sowohl durch direkte Behandlungskosten als auch durch indirekte Kosten wie z.B. Ausfälle am Arbeitsplatz.
Unter dem Begriff der CRS werden sehr unterschiedliche Ausprägungen der Erkrankung zusammengefasst. Es lassen sich verschiedene Phänotypen beschreiben, klinisch wird zunächst zwischen CRS mit Polyposis (CRSwNP) und ohne Polyposis (CRSsNP) unterschieden. Eine Polyposis nasi tritt bei ca. 2,7–4,4% der Gesamtbevölkerung auf und geht – im Gegensatz zu CRSsNP – zumeist mit einer moderaten bis schweren Typ-2-Entzündungsreaktion einher.3 30–70% der Patienten mit CRSwNP leiden zusätzlich an Asthma.4–6 Etwa 30% der Patienten, die an CRSwNP und Asthma leiden, zeigen auch eine Unverträglichkeit von nichtsteroidalen Antirheumatika. Dieses Krankheitsbild wird als M. Widal, Samter Trias, „aspirin-exacerbated respiratory disease“ (AERD) oder „non-steroidal anti-inflammatory drug-exacerbated respiratory disease“ (NERD) bezeichnet. Rezidive treten häufig auf, besonders unter Asthma- und NERD-Patienten.7, 8 Eine Rezidivrate von 50% nach chirurgischer Intervention ist bei Endotypen mit eosinophiler Typ-2-Entzündungsreaktion beschrieben.9–11 Die Dunkelziffer kann noch deutlich höher liegen, da Rezidive zu einer Therapiefrustration, gefolgt von einem Rückzug vom Gesundheitssystem, führen können. Nur wenige Untersuchungen haben bisher den Anteil der Patienten mit unkontrollierten Symptomen erhoben. Eine Studie unter CRS-Patienten zeigte, dass etwa 40% trotz maximaler konservativer und chirurgischer Therapie symptomatisch blieben.12
Die Typ-2-Entzündungsreaktion beiCRSwNP ist vor allem durch die Zytokine Interleukin (IL)4, IL-5, IL-13, IL-33, thymisches stromales Lymphopoietin (TSLP) und Immunoglobulin E (IgE) charakterisiert. Diese Zytokinprofile zeigen sich auch bei einem Großteil der Patienten mit schwerem Asthma, wobei bei diesen eine Therapie mit Biologika bereits etabliert ist. Nun bieten diese Entzündungsmediatoren auch neue therapeutische Ansätze zur Behandlung der CRSwNP (Abb.1).
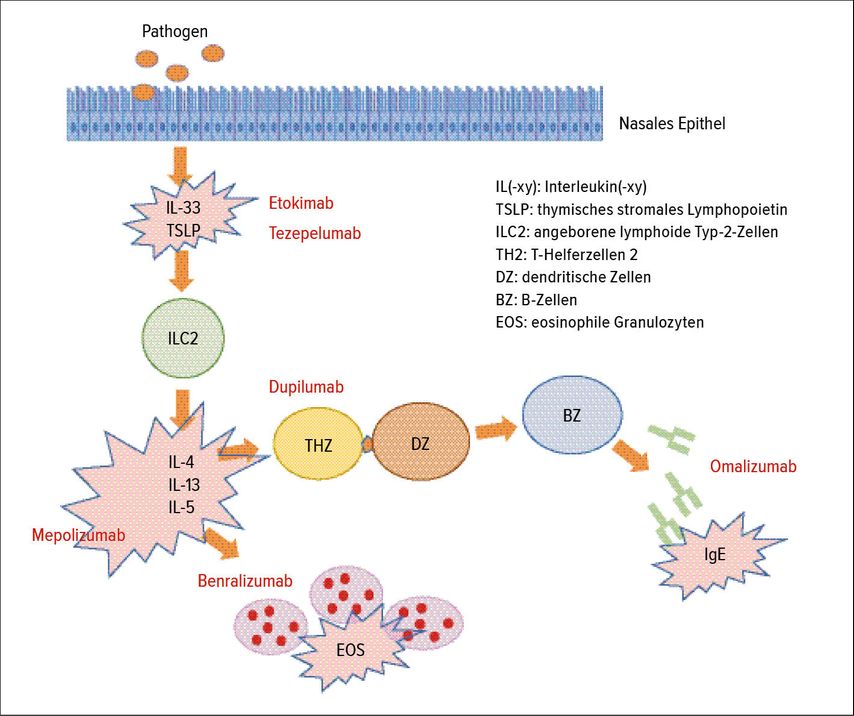
Abb. 1: Schematische Darstellung der Angriffspunkte von Antikörpertherapien bei chronischer Rhinosinusitis mit Polyposis nasi
Bisherige Therapie der CRSwNP
Nach dem bisherigen Behandlungsalgorithmus wird zunächst das konservative Therapiespektrum mit salinen Nasenspülungen, intranasalen Kortikosteroiden sowie intermittierenden Behandlungen mit systemischen Kortikosteroiden ausgeschöpft. Falls hierdurch keine dauerhaften Erfolge erzielt werden können, wird eine chirurgische Sanierung angestrebt. Jedoch auch nach erfolgreicher Operation sind vor allem Patienten mit zusätzlichen Erkrankungen wie Asthma und NERD oft nicht lange beschwerdefrei und Rezidive werden häufig beobachtet.
In den nächsten Jahren werden vermutlich mehrere Antikörper zur Behandlung der CRSwNP zur Verfügung stehen, was zu einem Umdenken und eventuell grundlegender Änderung in den Behandlungsalgorithmen führen kann. Zur Behandlung von Erkrankungen wie Asthma und atopischer Dermatitis, die – ähnlich wie bei CRSwNP – mit Typ-2-Entzündungsreaktionen einhergehen, wurden diese Medikamente bereits entwickelt.
Therapeutische Angriffspunkte und Antikörper zur Behandlung der CRSwNP
Anti-IgE
Häufig sind die totalen IgE-Werte in nasalen Polypen sowie in nasaler Mukosa bei Patienten mit CRSwNP erhöht.13 Der humanisierte, monoklonale Antikörper Omalizumab, der unter anderem für die Therapie von schweremallergischem Asthma zugelassen ist, bindet freies IgE und hemmt so die Aktivierung von Mastzellen und basophilen Granulozyten.14 Weiters können teilweise auch die Aktivierung und Proliferation von T-Helferzellen vom Typ 2 gebremst werden.15 Erfolge in der Behandlung von CRSwNP-Patienten mit zusätzlichem Asthma wurden bereits 2013 beschrieben.16 Neben einer Verbesserung der Lebensqualität konnte eine signifikante Reduktion der Ausdehnung der nasalen Polyposis festgestellt werden.16 Die Ergebnisse der rezent abgeschlossenen Phase-III-Studien POLYP 1 und POLYP 2 zu Omalizumab bei ausgeprägter CRSwNP zeigten in beiden Studien eine signifikante Verbesserung der Lebensqualität, des Riechvermögens sowie Reduktion der nasalen Sekretion und signifikante Verkleinerung der Nasenpolypen.17 Omalizumab wurde meist sehr gut vertragen. Das Nebenwirkungsprofil entsprach dem der Patienten in Asthma- und Urtikariastudien, wobei als häufigste Nebenwirkungen Cephalea, Reaktionen im Bereich der Injektionsstelle, Gelenksschmerzen, Schwindelgefühl und Oberbauchschmerzen berichtet wurden.17
Anti-IL-5 und Anti-IL-5Rα
CRSwNP ist durch eine erhöhte IL-5- Produktion und die dadurch bedingte eosinophile Entzündungsreaktion charakterisiert.18 Die Stimulation mit IL-5 führt zu einer Aktivierung und Rekrutierung von eosinophilen Granulozyten. Erhöhte IL-5-Werte korrelieren mit häufigeren Rezidiven und Auftreten von Asthma. Mepolizumab ist ein monoklonaler Antikörper gegen IL-5 und für die Behandlung von eosinophilem Asthma zugelassen. Eine randomisierte, placebokontrollierte Studie konnte zeigen, dass dieser Antikörper signifikante Verbesserungen bei Patienten mit CRSwNP bewirken kann. So konnten die Ausprägung der nasalen Polyposis und die Notwendigkeit einer Operation verringert werden, wobei die krankheitsbezogene Lebensqualität stieg.19 Die Ergebnisse einer Phase-III-Studie zur Wirksamkeit von Mepolizumab bei ausgeprägter CRSwNP werden in naher Zukunft erwartet (clinicaltrials.gov; NCT03085797).
Benralizumab ist ein monoklonaler, gegen den IL-5α-Rezeptor gerichteter Antikörper. Die Blockade des Rezeptors führt zu einer fast vollständigen Depletion der eosinophilen und basophilen Granulozyten. Der Antikörper wurde bereits für die Behandlung von schweremeosinophilem Asthma zugelassen und zeigt ein Nebenwirkungsprofil, das mit dem eines Placebos vergleichbar ist. Derzeit werden zwei klinische Phase-III-Studien durchgeführt, um den Effekt auf Patienten mit CRSwNP mit ausgeprägter und rezidivierender Polyposis nasi zu untersuchen (clinicaltrials.gov; NCT03401229, NCT04157335).
Anti-IL-4Rα
Dupilumab ist ein humaner, monoklonaler Anti-IL-4Rα-Antikörper, der die gemeinsame Untereinheit von IL-4- und IL-13-Rezeptoren blockiert. Als erstes Biologikum zur Behandlung von CRSwNP wurde Dupilumab bereits sowohl von der Food and Drug Administration (FDA) als auch von der European Medicines Agency (EMA) zugelassen. Neben mittelschwerer bis schwerer atopischer Dermatitis und schwerem Asthma besteht nun auch die Zulassung für ausgeprägte Polyposis nasi als Add-on-Therapie zu intranasalen Kortikosteroiden, wenn die Polyposis nasi mit systemischen Kortikosteroiden und chirurgischen Maßnahmen nicht ausreichend therapiert werden kann.
Diese Zulassungserweiterung basiert auf den Studien LIBERTY NP Sinus-24 und LIBERTY NP Sinus-52.20 Die Ergebnisse dieser Studien zeigen nicht nur eine signifikante und klinisch relevante Reduktion der Größe der Nasenpolypen und Verbesserung der Nasenatmung, sondern auch eine signifikante Verbesserung der Lebensqualität sowie des Riechvermögens (Abb.2). Der Bedarf an systemischen Kortisontherapien und chirurgischen Eingriffen war verglichen mit dem Placebo deutlich geringer.20 Die Sicherheitsanalyse der Studien zeigte ein äußerst günstiges Nebenwirkungsprofil. Am häufigsten traten Epipharyngitis, Cephalea, Epistaxis und Rötungen an der Einstichstelle auf, wobei alle häufigen unerwünschten Nebenwirkungen in der Placebogruppe öfter beobachtet wurden.
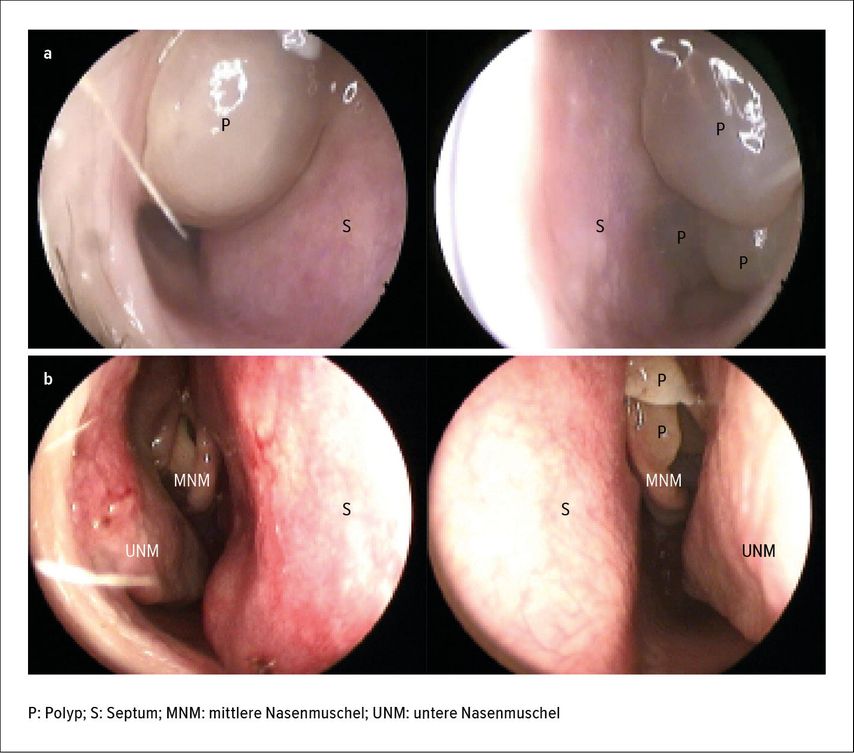
Abb. 2: a: Rechte und linke Nasenhaupthöhle mit ausgeprägter Polyposis nasi bei NERD vor Therapie. b: Rechte und linke Nasenhaupthöhle unter Therapie mit Dupilumab
Anti-IL-33 und Anti-TSLP
Nasale Epithelzellen können als Reaktion auf Allergene oder andere Pathogene Typ-2-Entzündungkaskaden in Gang setzen. In nasalen Polypen produzieren die Epithelzellen unter anderem die Zytokine IL-33 und TSLP, wodurch es zu einer weiteren Ausschüttung von Zytokinen wie IL-5 und IL-13 aufgrund der Aktivierung von innaten lymphoiden Zellen kommt. Antikörper gegen IL-33 wie Etokimab und gegen TSLP wie Tezepelumab setzen am Beginn der Typ-2-Entzündungskaskade an und werden bereits auf ihre Wirksamkeit bei Asthma und CRSwNP untersucht.
Ausblick
Biologika werden vermutlich in den nächsten Jahren ein fester Bestandteil der Therapie der ausgeprägten CRSwNP werden. Da ein breites Spektrum an Antikörpern zur Verfügung stehen wird, ist die Erforschung von prädiktiven Markern von großer Bedeutung. Für personalisierte Therapien werden Biomarker benötigt, die auch eine Optimierung bezüglich Asthmatherapie und CRSwNP-Behandlung ermöglichen. Auch der Zeitpunkt für Beginn und Ende einer Biologikatherapie und die Definition eines Therapieerfolges müssen erst in Behandlungsalgorithmen integriert werden. Um dieses Feld weiter zu erforschen, ist eineZusammenarbeit zwischen Pulmologen und HNO-Ärzten dringend erforderlich.
Obwohl viele Fragen noch unbeantwortet sind, gibt es durch den Einsatz von Biologika in der Behandlung der CRSwNP nun die Möglichkeit, auch vielen bisher unkontrollierten Patienten bessere Symptomkontrolle und Lebensqualität zu bieten.
Autor:
DDr. Sven Schneider
Klinische Abteilung für allgemeine HNO
Universitätsklinik für Hals-, Nasen- und Ohrenkrankheiten
Medizinische Universität Wien
E-Mail: sven.schneider@meduniwien.ac.at
Literatur:
1 Dietz de Loos D et al.: J Allergy Clin Immunol 2019; 143(3): 1207-14 2 Hastan D et al.: Allergy 2011; 66: 1216-23 3 Rajan JP et al.: J Allergy Clin Immunol 2015; 135, 676-81 4 Khan A et al.: Rhinology 2019; 57(1): 32-42 5 Philpott CM et al.: Respir Res 2018; 19(1): 129 6 Langdon C et al.: J Asthma Allergy 2016; 9: 45-53 7 Sella GCP et al.: J Allergy Clin Immunol Pract 2020; 8(1): 302-9 8 Stevens WW et
al.: J Allergy Clin Immunol Pract 2017; 5(4): 1061-70 9 DeConde AS et al.: Laryngoscope 2017; 127(3): 550-5 10 Hopkins C et al.: Laryngoscope 2009; 119(12): 2459-65 11 Vlaminck S et al.: Am J Rhinol Allergy 2014; 28(3): 260-4 12 van der Veen J et al.: Allergy 2017; 72(2): 282-90 13 Bachert C et al.:J Allergy Clin Immunol 2001; 107: 607-14 14 Mitchell PD et al.: Handb Exp Pharmacol 2017; 237: 131-52 15 Holgate S et al.: J Allergy Clin Immunol 2005; 115: 459-65 16 Gevaert P et al.: J Allergy Clin Immunol 2013; 131: 110-6 17 Gevaert P et al.: J Allergy Clin Immunol 2020; DOI: 10.1016/j.jaci.2020.05.032 18 Bachert C et al.: J Allergy Clin Immunol 1997; 99: 837-42 19 Bachert C et al.: J Allergy Clin Immunol 2017; 140: 1024-31 20 Bachert C et al.: Lancet 2019; 394(10209): 1638-50
Das könnte Sie auch interessieren:
Vorgehensweise bei Verdacht auf eine auditive Verarbeitungsstörung (AVS)
Auditive Verarbeitungsstörungen (AVS) sind ein seit Jahren sehr kontrovers diskutiertes Thema, welches sowohl in der Diagnostik als auch in der Therapie mit uneinheitlichem Vorgehen ...
„Die HNO hat glücklicherweise keine Nachwuchsprobleme“
Prim. Prof. Dr. Fabian Sommer hat am 1. November 2024 die Leitung der Abteilung für Hals-, Nasen-, Ohrenheilkunde in Feldkirch, Vorarlbergs einziger HNO-Abteilung, übernommen. Im ...
Komplementäre & integrative Medizin bei Antibiotikaresistenzen und Pandemien
Komplementäre Behandlungsmethoden können zum Beispiel bei Atemwegsinfekten und Otitis media evidenzbasiert in multimodale Therapiekonzepte der HNO eingebunden werden – vor allem dann, ...