Therapie im Wandel: zeitlich begrenzt und Sequenzierung
Autor:
OA Dr. Manuel Orlinger, MBA
Interne I: Internistische Onkologie und Hämatologie
Ordensklinikum Linz GmbH
Barmherzige Schwestern, Linz
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die therapeutische Landschaft der chronischen lymphatischen Leukämie (CLL) hat sich in den vergangenen Jahren fundamental gewandelt. Die klassische Chemoimmun-therapie ist weitgehend historischen Betrachtungen gewichen und wurde durch zielgerichtete Ansätze ersetzt. Im Fokus der aktuellen wissenschaftlichen Auseinandersetzung steht nun die Optimierung dieser chemofreien Strategien.
Die zentrale Dichotomie der Erstlinientherapie – kontinuierliche BTK-Inhibition versus zeitlich begrenzte BCL2-Inhibition – wurde durch aktuelle Daten des ASH-Kongresses 2025, besonders der CLL17-Studie, neu beleuchtet. Gleichzeitig rückt mit den unterschiedlichen zur Verfügung stehenden Therapien die Therapiesequenzierung in den Vordergrund, sodass Therapiealgorithmen durch eine zunehmende Komplexität gekennzeichnet sind.
Vom Standard zur Individualisierung
Lange Zeit dominierte die Frage „Chemotherapie – ja oder nein?“ den klinischen Entscheidungsprozess. Mit der Etablierung hochwirksamer Inhibitoren des B-Zell-Rezeptor-Signalwegs (BTK-Inhibitoren) und des antiapoptotischen Proteins BCL2 hat sich dieser Diskurs verschoben. Die aktuellen Leitlinien präsentieren sowohl die kontinuierliche Gabe von BTK-Inhibitoren (BTKi) als auch die zeitlich begrenzte („fixed duration“) Kombination aus Venetoclax und Obinutuzumab sowie die Kombination aus BTKi und Venetoclax als gleichwertige Erstlinienoptionen.
Diese Äquivalenz in den Leitlinien stellt die behandelnden Hämatoonkolog:innen jedoch vor die Herausforderung der individuellen Selektion. Ist das Ziel eine möglichst tiefe Remission mit therapiefreiem Intervall, oder steht die kontinuierliche Kontrolle des malignen Klons bei einfacher oraler Applikation im Vordergrund? Die auf dem ASH-Kongress 2025 präsentierten Daten, allen voran die Ergebnisse der Phase-III-Studie CLL17 der Deutschen CLL-Studiengruppe (DCLLSG), liefern nun die notwendige Evidenz für eine differenzierte Entscheidungsfindung.
Erstlinientherapie: Erkenntnisse aus der CLL17-Studie
Die CLL17-Studie wurde mit Spannung erwartet, da sie als erster großer Head-to-Head-Vergleich drei relevante Konzepte prospektiv untersuchte: die kontinuierliche Ibrutinib-Monotherapie, die zeitlich begrenzte Kombination aus Venetoclax und Obinutuzumab (VO) sowie die rein orale, zeitlich begrenzte Kombination aus Ibrutinib und Venetoclax (IV).1
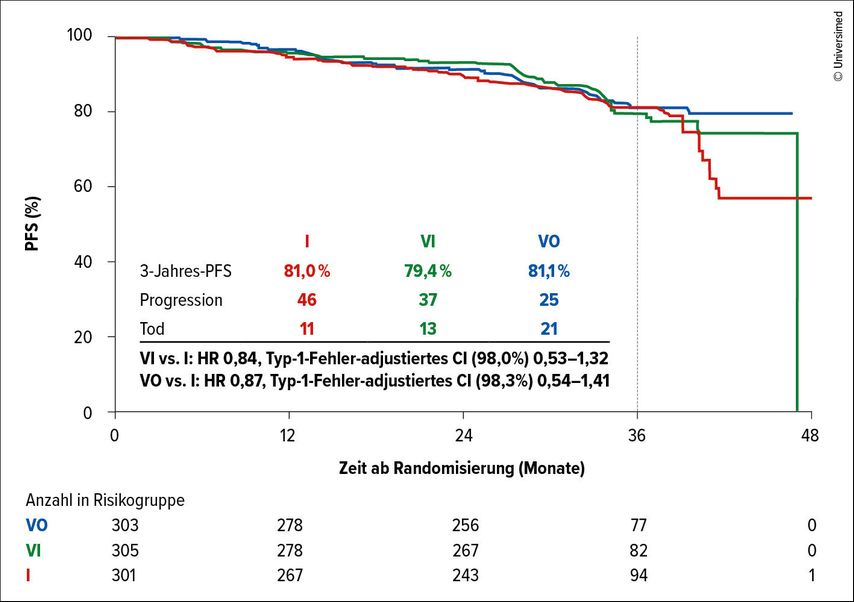
Die primäre Endpunktanalyse bestätigte die Nichtunterlegenheit der zeitlich begrenzten Konzepte gegenüber der Ibrutinib-Dauertherapie beim progressionsfreien Überleben (PFS) (Abb.1). Damit ist die Strategie der „fixed duration“ endgültig als mindestens gleichwertiger Standard validiert. Interessant ist hierbei der Blick auf die Tiefe der Remission: Die Kombination Venetoclax/Obinutuzumab erreichte mit 73,3% uMRD („undetectable minimal residual disease“) im peripheren Blut signifikant tiefere Ansprechraten im Vergleich zur rein oralen Kombination IV (47,2%) und, wenig überraschend, der Ibrutinib-Monotherapie (0%).1 Dies unterstreicht die hohe synergistische Potenz des CD20-Antikörpers im Kontext der BCL2-Inhibition.
Differenzierte Betrachtung der Hochrisikogruppe
Eine pauschale Ablösung der Dauertherapie lässt sich aus den Daten jedoch nicht ableiten, vor allem wenn man die genetischen Subgruppen betrachtet. In die CLL17-Studie waren auch Patient:innen mit Deletion 17p (del17p) und/oder TP53-Mutation eingeschlossen. Aufgrund des tendenziell besseren 3-Jahres-PFS (VO 62,0%, I: 79,4%, VI: 69%) bleibt die kontinuierliche BTK-Inhibition für diese Hochrisikoklientel eine auch pathophysiologisch gut begründete und klinisch bewährte Strategie. Das Risiko für ein rasches Rezidiv nach Beendigung einer zeitlich begrenzten Therapie ist bei TP53-alterierten Patient:innen erhöht, weshalb die dauerhafte Suppression des Klons mittels BTKi (oder in Zukunft einer Kombination) weiterhin eine exzellente Option ist.
Entscheidungsfaktoren Patient:innenpräferenz und Komorbiditäten
Jenseits der reinen Effizienzdaten rückt das „shared decision making“ in den Mittelpunkt. Die Wahl zwischen Venetoclax-basierten Regimen und BTK-Inhibitoren ist maßgeblich von patient:innenindividuellen Faktoren abhängig.
Eine Therapie mit Venetoclax und Obinutuzumab erfordert initial eine relativ hohe logistische Bindung. Das notwendige stationäre oder streng ambulante Monitoring zur Vermeidung eines Tumorlysesyndroms (TLS) während der Aufdosierungsphase („ramp-up“) sowie die intravenösen Gaben des Antikörpers sind für ältere, gebrechliche Patient:innen und solche mit weiten Anfahrtswegen relevante Hürden.
Im Gegensatz dazu bietet die kontinuierliche BTK-Inhibition (mit Acalabrutinib, Zanubrutinib oder Ibrutinib) den Vorteil einer rein oralen Therapie, die im Alltag oft einfacher zu integrieren ist („Tablette statt Tagesklinik“).
Zudem diktieren Komorbiditäten oft die Substanzwahl: Bei Patient:innen mit signifikanter Niereninsuffizienz kann das TLS-Risiko gegen Venetoclax sprechen, während kardiovaskuläre Vorerkrankungen oder eine Blutungsneigung den Einsatz von BTK-Inhibitoren limitieren können. Die Therapieentscheidung ist somit immer eine Abwägung zwischen dem Wunsch nach therapiefreier Zeit und der Machbarkeit bzw. Verträglichkeit im Alltag.
Neue Daten zu Pirtobrutinib in der Erstlinientherapie
Neben den etablierten Substanzen drängen neue Wirkmechanismen in die Erstlinie. Auf dem ASH 2025 wurden Daten der BRUIN-CLL313-Studie vorgestellt, die den nichtkovalenten BTK-Inhibitor Pirtobrutinib im Vergleich zu Bendamustin/Rituximab (BR) in der Erstlinie untersuchte.2 Pirtobrutinib zeigte hierbei eine signifikante Verbesserung des PFS (24-Monate-PFS 93,4% vs. 70,7%; Hazard-Ratio [HR]: 0,20) sowie einen Trend zu einem längeren Gesamtüberleben (OS).
Ergänzend hierzu lieferte die Phase-III-Studie BRUIN CLL314 wichtige Head-to-Head-Daten im Vergleich zu Ibrutinib, die auch eine Kohorte von 225 therapienaiven Patient:innen einschloss. Pirtobrutinib demonstrierte hierbei eine Nichtunterlegenheit im Ansprechen (ORR) und zeigte in der Subgruppe der Erstlinienpatient:innen einen deutlichen Trend zu einem verlängerten PFS (HR: 0,24; 95% CI: 0,10–0,59). Besonders hervorzuheben ist das überlegene Sicherheitsprofil, besonders bezüglich kardialer Ereignisse wie Vorhofflimmern/-flattern: 2,4% unter Pirtobrutinib vs. 13,5% unter Ibrutinib.3
Auch wenn Pirtobrutinib aktuell primär in der Rezidivsituation verortet ist, unterstreichen diese Daten das endgültige Ende der Chemoimmuntherapie und das Potenzial reversibler BTK-Inhibitoren in frühen Linien. Selbst in Szenarien, in denen man früher noch erwogen hätte, BR einzusetzen (z.B. ältere, fitte Patient:innen ohne Hochrisikogenetik), zeigen sich zielgerichtete Substanzen mittlerweile als weit überlegen.
Der Stellenwert der MRD-Diagnostik: Potenzial und Limitationen
Mit der Verbreitung zeitlich begrenzter Therapien gewinnt die Messung der minimalen Resterkrankung (MRD) an Bedeutung. Für die britische FLAIR-Studie wurde auf dem ASH 2025 ein Update zur MRD-gesteuerten Therapie mit Ibrutinib und Venetoclax präsentiert.4 Das Konzept, die Therapiedauer an das Erreichen einer uMRD anzupassen (doppelte Zeit bis uMRD4), führte selbst bei genetischen Hochrisikogruppen zu exzellenten Langzeitergebnissen, die der FCR-Chemotherapie weit überlegen waren.
Es ist jedoch essenziell, diese Daten korrekt in den aktuellen klinischen Kontext einzuordnen. Aktuell existiert keine behördliche Zulassung für eine solche MRD-gesteuerte Verlängerung der Therapie. Zudem fehlt bislang der methodisch saubere Vergleich zwischen einer „MRD-gesteuerten Dauertherapie“ und dem derzeitigen Standard konsekutiver, zeitlich begrenzter Therapien (Retreatment bei Rezidiv). Solange nicht geklärt ist, ob das Hinauszögern des Rezidivs durch eine verlängerte Erstlinientherapie einen echten Überlebensvorteil gegenüber der Wiederbehandlung im Rezidiv bietet, bleibt die MRD-Steuerung ein wertvolles Instrument in klinischen Studien, ist aber noch kein allgemeiner klinischer Standard für die routinemäßige Therapiesteuerung. Prognostisch ist das Erreichen einer uMRD jedoch unbestritten der stärkste Prädiktor für ein langes PFS im Hinblick auf zeitlich begrenzte Therapien.
Therapiesequenzierung im rezidivierten/refraktären Setting
Die Sequenzierung der Therapien im Rezidiv folgt zunehmend logischen biologischen Prinzipien, wobei strikt zwischen „double exposed“ (Therapieabbruch, z.B. wegen Unverträglichkeit oder fixierter Dauer) und „double refractory“ (echte Progression unter Therapie) unterschieden werden muss.
Progression nach Venetoclax-basierter Erstlinie
Daten der GAIA/CLL13-Studie und Registerdaten bestätigen, dass Patient:innen nach einer zeitlich begrenzten Venetoclax-Therapie sensitiv für Folgetherapien bleiben.5,6 Bei einem Spätrezidiv (definiert als Rezidiv mehrere Jahre nach Therapieende) ist eine Wiederholung der Venetoclax-basierten Therapie (Retreatment) eine evidenzbasierte Option.7 Bei frühen Rezidiven oder einer Refraktärität ist der Wechsel auf einen BTK-Inhibitor (bevorzugt Zweitgenerations-Inhibitoren wie Acalabrutinib oder Zanubrutinib) der Standard, da hier keine Kreuzresistenz vorliegt.
Progression nach kovalentem BTK-Inhibitor
Für Patient:innen, die unter einer dauerhaften BTK-Inhibition progredient sind, ist der Klassenwechsel auf Venetoclax (in Kombination mit Rituximab, gemäß MURANO-Daten) der etablierte Standard.8
Hier ergibt sich jedoch durch die Zulassungssituation von Pirtobrutinib eine wesentliche Erweiterung der Optionen. Pirtobrutinib ist nicht mehr ausschließlich Patient:innen vorbehalten, die bereits beide Wirkstoffklassen (cBTKi und BCL2i) erhalten haben. Es besteht die Möglichkeit, Pirtobrutinib auch direkt nach Versagen eines kovalenten BTK-Inhibitors einzusetzen. Da Pirtobrutinib reversibel an BTK bindet, ist es auch bei Vorliegen der klassischen C481-Resistenzmutationen wirksam.9 Dies ist eine valide Option für Patient:innen mit Hochrisikokonstellation (TP53-Mutation, del17p), für Patient:innen, die für Venetoclax (noch) nicht infrage kommen, ein hohes Tumorlyserisiko haben oder eine orale Therapie fortsetzen möchten.
Herausforderung „double refractory“ und neue Horizonte
Die größte therapeutische Herausforderung besteht bei Patient:innen, die sowohl auf kovalente BTK-Inhibitoren als auch auf BCL2-Inhibitoren refraktär sind. Für diese „Double refractory“-Situation ist Pirtobrutinib aktuell die wichtigste verfügbare Substanz, wenngleich das mediane PFS mit 19,6 Monaten10 nicht exorbitant lang ist.
Der Blick in die Zukunft zeigt jedoch bereits die nächste Generation von Wirkstoffen: BTK-Degrader (z.B. BGB-16673, NX-5948). Diese sogenannten PROTACs („proteolysis-targeting chimeras“) führen zum vollständigen Abbau des BTK-Proteins, anstatt es nur zu hemmen. In frühen Studiendaten zeigen sie hohe Ansprechraten auch bei komplexen Resistenzprofilen und könnten mittelfristig die Lücke für mehrfach vorbehandelte Patient:innen schließen.11,12
Ein Sonderfall bleibt die Richter-Transformation, deren Prognose weiterhin als ungünstig einzustufen ist. Hier zeigen Kombinationen aus Checkpoint-Inhibitoren und zielgerichteten Substanzen erste vielversprechende Signale,13 der Einschluss in klinische Studien sollte jedoch weiterhin angestrebt werden.
Fazit für die Praxis
Die CLL-Therapie ist gegenwärtig durch eine Pluralität hocheffektiver Optionen gekennzeichnet. Die Ergebnisse der CLL17-Studie etablieren zeitlich begrenzte Therapien als robusten Standard, machen die Dauertherapie jedoch nicht obsolet – vor allem nicht für Hochrisikopatient:innen oder jene, die eine einfache orale Therapie bevorzugen.
Für die Sequenzierung gilt: Die biologische Empfindlichkeit des Klons entscheidet. Nach Venetoclax ist BTK-Inhibition effektiv, nach BTK-Inhibition ist der Wechsel auf Venetoclax oder – als nun verfügbare Alternative – auf den nichtkovalenten Inhibitor Pirtobrutinib möglich. Ebenso sollte eine Evaluierung hinsichtlich Wiederbehandlung im Kontext zeitlich begrenzter Therapien erfolgen. Entscheidend bleibt, bei jedem Rezidiv den genetischen Status (insbesondere TP53, del17p) neu zu evaluieren, um eine informierte, personalisierte Therapieentscheidung zu treffen.
Literatur:
1 Al-Sawaf O et al.: Fixed-duration versus continuous targeted treatment for previously untreated chronic lymphocytic leukemia: results from the randomized CLL17 trial. Blood 2025; 146: 1 2 Jurczak W et al.: BRUIN CLL-313: randomized phase III trial of pirtobrutinib versus bendamustine plus rituximab in untreated patients with chronic lymphocytic leukemia/small lymphocytic lymphoma. J Clin Oncol 2025; JCO2502380 (doi: 10.1200/JCO-25-02380. Online ahead of print) 3 Woyach JA et al.: Pirtobrutinib versus ibrutinib in treatment-naïve and relapsed/refractory chronic lymphocytic leukemia/small lymphocytic lymphoma. J Clin Oncol 2025; JCO2502477 (doi: 10.1200/JCO-25-02477. Online ahead of print) 4 Dalal S et al.: MRD-guided ibrutinib plus venetoclax improves outcomes in CLL patients with TP53, ATM, or NOTCH1 aberrations compared to ibrutinib and FCR: results from the phase III NCRI FLAIR trial. Blood 2025; 146: 679 5 Niemann C et al.: Efficacy of 2nd-line treatment in CLL after venetoclax-based 1st-line treatment: results from the GAIA/CLL13 trial. Blood 2025; 146: 795 6 Mato AR et al.: Assessment of the efficacy of therapies following venetoclax discontinuation in CLL reveals BTK inhibition as an effective strategy. Clin Cancer Res 2020; 26(14): 3589-96 7 Davids MS et al.: Preliminary results of the ongoing multicenter, phase 2 study of retreatment with venetoclax plus obinutuzumab (ReVenG) in patients with recurrent CLL. Hematological Oncology 2025; 43(S3): e211_70094 8 Kater AP et al.: The MURANO study: final analysis and retreatment/crossover substudy results of VenR for patients with relapsed/refractory CLL. Blood 2025; 145(23): 2733-45 9 Sharman JP et al.: BRUIN CLL-321: randomized phase III trial of pirtobrutinib versus idelalisib plus rituximab (IdelaR) or bendamustine plus rituximab (BR) in BTK inhibitor pretreated chronic lymphocytic leukemia/small lymphocytic lymphoma. Blood 2024; 144: 886 10 Woyach JA et al.: Pirtobrutinib in post-cBTKi CLL/SLL: ∼30 months follow-up and subgroup analysis with/without prior BCL2i from the phase 1/2 BRUIN study. Blood 2023; 142: 325 11Shah N et al.: Bexobrutideg (NX-5948), a novel Bruton’s tyrosine kinase (BTK) degrader, shows high clinical activity and tolerable safety in patients with Waldenström macroglobulinemia: updated results from an ongoing phase 1a/b study. Blood 2025; 146: 5359 12 Ahn I et al.: Updated efficacy and safety results of the bruton tyrosine kinase (BTK) degrader BGB-16673 in patients with relapsed/refractory chronic lymphocytic leukemia/small lymphocytic lymphoma (CLL/SLL) from the ongoing phase 1 CaDAnCe-101 study. Blood 2025; 146: 85 13 Al-Sawaf O et al.: Correlates of response to combined checkpoint and BTK inhibition for treatment of richter transformation: extended follow-up from the prospective RT1 trial. Blood 2025; 146: 90
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
CAR-T-Zellen: Stellenwert – klinische Evidenz – Herausforderungen
„Chimeric antigen receptor“(CAR)-T-Zellen sind eine der bedeutendsten Innovationen der modernen Hämatologie. Es handelt sich dabei um autologe, genetisch modifizierte T-Zellen, die ex ...
Chronische myeloische Leukämie (CML)
Die Prognose der CML-Patient:innen unterscheidet sich durch die Entwicklung der Tyrosinkinaseinhibitoren (TKI) kaum mehr von der Normalbevölkerung. Dennoch gibt es neue Erkenntnisse, die ...