Chronische myeloische Leukämie (CML)
Autorin:
Prim. Priv.-Doz. Dr. Sonja Heibl
Vorständin, stellvertretende Leiterin Tumorzentrum OÖ
Abteilung für Innere Medizin IV
Hämatologie, internistische Onkologie und Palliativmedizin, Nephrologie und Dialyse
Klinikum Wels-Grieskirchen
E-Mail: Sonja.Heibl@klinikum-wegr.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Prognose der CML-Patient:innen unterscheidet sich durch die Entwicklung der Tyrosinkinaseinhibitoren (TKI) kaum mehr von der Normalbevölkerung. Dennoch gibt es neue Erkenntnisse, die das Management beeinflussen und in die neuen Onkopedia-Leitlinien aufgenommen wurden.
Keypoints
-
In der TKI-Ära gibt es in der Stadieneinteilung der CML nur mehr die chronische Phase und die Blastenphase.
-
In der Erstlinientherapie ist nun zusätzlich zu Imatinib, Nilotinib, Dasatinib und Bosutinib Asciminib zugelassen.
-
Bei Versagen auf die Erstlinientherapie erfolgt die Therapiewahl linienagnostisch.
-
Hochrisikofaktoren in der chronischen Phase erfordern gezieltes Vorgehen in der Therapie.
-
Lockerung der Reproduktionsempfehlungen für männliche Patienten
Die CML ist eine klassische myeloproliferative Erkrankung, die definitionsgemäß immer durch die BCR::ABL-Genfusion gekennzeichnet ist. Grundsätzlich ist die CML mit einer Inzidenz von 1,2 bis 1,5/ 100000 Einwohner:innen/Jahr eine seltene Krankheit. Aufgrund der geringen Mortalität (1% jährlich) seit Einführung der TKI steigt die Prävalenz der Erkrankung bei konstanter Inzidenz.1
Stadieneinteilung
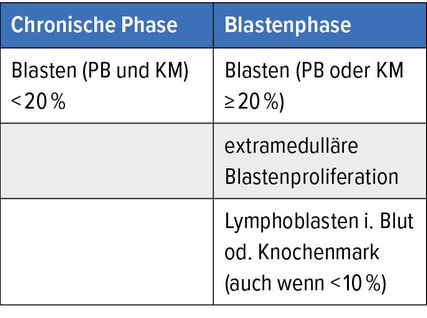
Vor der Verfügbarkeit der TKI verlief die Erkrankung klassisch in drei Phasen – der chronischen Phase, der akzelerierten Phase und der Blastenphase. Bereits in der Klassifikation von 2022 wurde von der WHO die akzelerierte Phase gestrichen und die Unterscheidung zwischen chronischer Phase und Blastenphase durch die Blastenzahl (<20% bzw. >20%) definiert, wenngleich diese arbiträren Grenzen nicht ganz optimal sind.2 Auch in den aktuellen Onkopedia-Leitlinien (November 2025)wird die WHO-Klassifikation als die aktuell empfohlene angeführt (Tab.1).
Erstlinientherapie
In der ersten Linie sind fünf TKI zugelassen – Imatinib, Nilotinib, Dasatinib, Bosutinib und seit Ende 2025 Asciminib. Die Entscheidung, welchen TKI man wählt, hängt von Patient:innen- und Krankheitsfaktoren ab. Es fließen hier Faktoren wie Patient:innenalter, Komorbiditäten, kardiovaskuläres Risikoprofil, aber auch Lebensstil und Arbeitssituation ein. Außerdem spielt das Therapieziel eine wesentliche Rolle – ist dies das Erreichen einer TFR („treatment-free remission“) oder nicht. Die Charakteristika der CML an sich haben auch einen Einfluss auf die Therapiewahl – ELTS-Score, Vorhandensein von chromosomalen Anomalien (ACAs) oder zusätzlichen genetischen Abnormalitäten.
Nilotinib, Dasatinib, Bosutinib und Asciminib zeigen gegenüber Imatinib in der Erstlinienbehandlung eine bessere Effektivität mit höheren Raten an zytogenetischen und molekularen Remissionen. Ob Asciminib in der Erstlinie auch den Zweitgenerations-TKI überlegen ist, konnte in der ASC4First-Studie nicht definitiv gezeigt werden, da die Studie dafür nicht gepowert war.3 Ein Überlebensvorteil konnte für keine der Substanzen beobachtet werden, das Follow-up in der ASC4First-Studie ist allerdings auch noch zu kurz. Die Verträglichkeit (Grad ≥3 AEs und therapiebedingte Abbrüche) war unter Asciminib sowohl im Vergleich zu Imatinib als auch zu den Zweitgenerations-TKI besser.
Versagen auf die Erstlinientherapie
Die häufigste Ursache für Versagen der Erstlinientherapie ist entweder Unverträglichkeit oder primäre/sekundäre Resistenz. Etwa 30–40% der Patient:innen müssen aus den genannten Gründen auf eine andere Erstlinientherapie umgestellt werden. In den aktuellen Onkopedia-Leitlinien wird neu ein „linienagnostisches“ Vorgehen empfohlen, da die Ursache des Therapieversagens bedeutender ist als die Anzahl der Vortherapien.
Bei Intoleranz kann nach Prüfung der Kreuzintoleranz jeder alternative TKI eingesetzt werden, auch Imatinib ist in der Situation der Unverträglichkeit möglich. Im Falle einer Resistenz auf die Erstlinientherapie scheidet Imatinib als Folgesubstanz aus. In jedem Fall soll ein Mutationsprofil erstellt werden und dann entsprechend die Wahl des TKI erfolgen. Liegt eine T315I-Mutation vor, ergibt sich die Indikation für den Einsatz von Ponatinib. Asciminib in der höheren Dosierung (2x200mg) ist aktuell nur in der Schweiz und in den USA zugelassen.
Hochrisikomerkmale und Therapieimplikationen
In der aktuellen Situation ist die Einschätzung der Prognose der Krankheit anhand von Scores eher schwierig. Prognose-Scores nach Sokal und Hasford (Euro-Score) wurden in der Prä-TKI-Ära entwickelt und spiegeln die aktuelle therapeutische Situation nicht eindeutig wider. Der heute bevorzugte Score ist der EUTOS-„Long Term Survival“(ELTS)-Score, mit dem sehr gut die CML-bedingte Mortalität eingeschätzt werden kann.4 Bezüglich Behandlungsresistenz, Progression und Therapieauswahl ist die Aussagekraft allerdings eingeschränkt.
Das Auftreten von bestimmten zusätzlichen ACAs wird häufiger in der Blastenphase gesehen, in der chronischen Phase wird es als Risikosignal interpretiert.2,5–7
Als Hochrisikoindikatoren in der chronischen Phase gelten die seltenen ACAs, i(17q) sowie ein komplexer Karyotyp oder das Vorhandensein von 3q26.2-Rearrangierungen (Tab.2).
Werden in der chronischen Phase zytogenetisch zusätzliche Hochrisikoaberrationen nachgewiesen, dann sollte die Möglichkeit einer allogenen Stammzelltransplantation früh evaluiert werden. Primär sollten in dieser Situation bevorzugt potente Multikinaseinhibitoren wie Bosutinib oder Dasatinib eingesetzt werden.
Therapiefreie Remission (TFR)
Nach Erreichen einer stabilen tiefen molekularen Remission (DMR) über einen bestimmten möglichst langen Zeitraum kann unter bestimmten Voraussetzungen die TKI-Therapie abgesetzt werden.8,9 Als obligatorische Voraussetzungen wurden in der aktuellen Onkopedia-Leitlinie eine chronische Erkrankungsphase der CML, eine adäquate qualitätsgesicherte PCR-Methodik sowie ein:e entsprechend motivierte:r Patient:in gefordert.
Ein Absetzversuch sollte mit den Patient:innen nur dann diskutiert werden, wenn eine Imatinib-Therapie mindestens fünf Jahre und eine Zweitgenerations-TKI-Therapie mindestens vier Jahre mit einer Dauer der DMR von zumindest zwei Jahren dokumentiert werden kann. Außerdem muss ein engmaschiges Monitoring nach dem Absetzen des TKI möglich sein.
Familienplanung
Die Empfehlungen hinsichtlich der Reproduktion haben sich für männliche Patienten dahingehend verändert, dass nun klar festgehalten wird, dass unter Imatinib, Bosutinib, Dasatinib, Nilotinib und Asciminib keine Einschränkung der Fertilität und kein Anhaltspunkt für eine Mutagenese mit angeborenen Fehlbildungen der Kinder besteht, sodass aus diesem Grund eine Vaterschaft unter der Therapie mit den genannten TKI möglich ist.10
Literatur:
1 Huang X et al.: Estimations of the increasing prevalence and plateau prevalence of chronic myeloid leukemia in the era of tyrosine kinase inhibitor therapy. Cancer 2012; 118(12): 3123-7 2 Khoury JD et al.: The 5th edition of the World Health Organization classification of haematolymphoid tumours: myeloid and histiocytic/dendritic neoplasms. Leukemia 2022; 36(7): 1703-19 3 Hochhaus A et al.: Asciminib in newly diagnosed chronic myeloid leukemia. N Engl J Med 2024; 391(10): 885-98 4 Pfirrmann M et al.: The EUTOS long-term survival (ELTS) score is superior to the Sokal score for predicting survival in chronic myeloid leukemia. Leukemia 2020; 34(8): 2138-49 5 Hehlmann R et al.: Impact of emerging ACA on survival in chronic myeloid leukemia (CML). Leukemia 2022; 36(10): 2544-7 6 Hehlmann R et al.: High-risk additional chromosomal abnormalities at low blast counts herald death by CML. Leukemia 2020; 34(8): 2074-86 7 Alhuraiji A et al.: Prognostic significance of additional chromosomal abnormalities at the time of diagnosis in patients with chronic myeloid leukemia treated with frontline tyrosine kinase inhibitors. Am J Hematol 2018; 93(1): 84-90 8 Campiotti L et al.: Imatinib discontinuation in chronic myeloid leukaemia patients with undetectable BCR-ABL transcript level: a systematic review and a meta-analysis. Eur J Cancer 2017; 77:48-56 9 Mahon FX et al.: European Stop Tyrosine Kinase Inhibitor trial (EURO-SKI) in chronic myeloid leukemia: final analysis and novel prognostic factors for treatment-free remission. J Clin Oncol 2024; 42(16): 1875-80 10 Nesr G et al.: Effect of tyrosine kinase inhibitors on male fertility in patients with chronic phase chronic myeloid leukemia. Leuk Lymphoma 2024; 65(8): 1161-6
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
CAR-T-Zellen: Stellenwert – klinische Evidenz – Herausforderungen
„Chimeric antigen receptor“(CAR)-T-Zellen sind eine der bedeutendsten Innovationen der modernen Hämatologie. Es handelt sich dabei um autologe, genetisch modifizierte T-Zellen, die ex ...
Therapie im Wandel: zeitlich begrenzt und Sequenzierung
Die therapeutische Landschaft der chronischen lymphatischen Leukämie (CLL) hat sich in den vergangenen Jahren fundamental gewandelt. Die klassische Chemoimmun-therapie ist weitgehend ...