CAR-T-Zellen und BiTE: neue Immuntherapien in der Rheumatologie
Bericht:
Reno Barth
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Das ideale Ziel einer Therapie einer rheumatischen Erkrankung ist die medikamentenfreie Remission. Dieses Ziel wird mit den gängigen Therapien, also mit therapeutischen Antikörpern und Januskinase-Inhibitoren, regelhaft nicht erreicht. Strategien, die auf radikale Depletion von B-Zellen und einen folgenden Reset des Immunsystems setzen, könnten dieses Ziel erreichbar machen.
In der Rheumatologie würden seit vielen Jahren weitgehend die gleichen Strategien weiterentwickelt, so Univ.-Prof. Dr. Ricardo Grieshaber-Bouyer von der 3. Internen Abteilung am Uni-Klinikum Erlangen. Auch mit den aktuell in Phase-II- und -III-Studien untersuchten Small Molecules und Antikörpern werden lange bekannte Wege begangen. Sie richten sich gegen die bekannten Zytokine, gegen Januskinasen und nur in wenigen Fällen gegen neue Ziele.1 Umso erfreulicher sei es, so Grieshaber-Bouyer, dass nun auch B-Zellen in den Mittelpunkt des Interesses rücken. Das betreffe zum einen die Depletion von B-Zellen mittels monoklonaler Antikörper und zum anderen die Inhibition von B-Zell-Wachstumsfaktoren. Ziele an der B-Zelle sind CD20 (Ocrelizumab, Rituximab), CD22 (Epratuzumab), BAFF-R (Belimumab), CD80 und CD86 (Abatacept), TACI und BCMA (Atacicept).2
Einen effektiveren Weg, B-Zellen zu depletieren, und damit auch eine Option, Autoimmunerkrankungen „auf einer anderen Ebene“ zu beeinflussen, stellen gegen CD19 gerichtete CAR-T-Zellen dar, erläutert Grieshaber-Bouyer. Man habe in den vergangenen vier Jahren seit der Behandlung der ersten Patientin mit dieser neuen Therapie gesehen, dass CD19-CAR-T-Zell-Therapie bei einer breiten Auswahl an immunvermittelten Erkrankungen transformative Ergebnisse liefert. CAR-T-Zellen – CAR bedeutet „chimeric antigen receptor“ – sind gentechnisch veränderte T-Zellen mit synthetischen antigenspezifischen Rezeptoren, die sich bei den in der Rheumatologie eingesetzten Therapien zumeist gegen CD19 auf B-Zellen richten. Mit CAR-T-Zellen wird eine vollständige Depletion der CD19-positiven B-Zellen erreicht. Man habe gesehen, dass Lupuspatient:innen mit starker Hautbeteiligung „nach der Behandlung kaum mehr wiederzuerkennen“ waren, und man habe sogar Besserungen bei interstitiellen Lungenerkrankungen beobachtet. So stellte sich bei vielen mit CAR-T-Zellen behandelten Patient:innen langfristige Remission ein. Dabei lerne man auch viel über die Biologie und die Pathophysiologie des Immunsystems. Zum Beispiel zeigten longitudinale Studien mit Lymphknotenbiopsien, dass mit CAR-T-Zellen eine komplette Depletion der CD19- und CD20-positiven B-Zellen möglich sei, was beispielweise mit Rituximab nicht gelinge.
Grieshaber-Bouyer: „Das zeigt, dass die T-Zell-vermittelte Lyse der B-Zellen im Gewebe effektiver ist. Die Frage ist nun, wie sich das Immunsystem nach einer vollständigen Depletion der B-Zellen weiterentwickelt.“3
Immun-Reset durch vollständige Depletion der B-Zellen
Die ausgezeichnete klinische Wirksamkeit dieser kompletten B-Zell-Depletion bildete die Basis für das Konzept eines „Immun-Resets“, für das mittlerweile auch molekularbiologische Daten sprechen. So kommt es nach der CAR-T-Behandlung zum Verschwinden von Plasmablasten und zu einer deutlichen Zunahme naiver und transitionaler B-Zellen. Die vor einer CAR-T-Zell-Therapie reichlich vorhandenen klassengewechselten IgG+ und IgA+ B-Gedächtniszellen verschwinden, nach der Behandlung dominieren naive Zellen mit IgM oder IgD.
Bemerkenswerterweise betrifft der Reset nicht nur die B-Zellen. Vielmehr zeigen regulatorische T-Zellen (Treg) post CAR-T-Behandlung vermehrte Expression von Proteinen, die mit Immunsuppression assoziiert sind. Grieshaber-Bouyer weist darauf hin, dass diese Proteine bei Patient:innen mit Autoimmunerkrankungen in geringerem Maß exprimiert werden als bei Gesunden. Nach einer CAR-T-Zell-Behandlung erreichen die inhibitorischen Proteine der Treg annähernd das Niveau, das bei gesunden Probanden beobachtet wird. Man bekomme also wieder eine stärkere Regulation des Immunsystems durch die Treg. Diese Effekte weiten sich auf das myeloide Kompartiment aus. Beispielsweise nimmt die Aktivierung der Neutrophilen durch CAR-T-Zell-Therapie ab, es kommt zu einer Reprogrammierung der Neutrophilen mit einer Abnahme der proinflammatorischen Effektormoleküle. Unter anderem nimmt die Antwort auf Zytokine und Typ-1-Interferon ab.
Grieshaber-Bouyer: „Wir können also von einem Immun-Reset auf mehreren Ebenen sprechen, der höchstwahrscheinlich mit dem klinischen Ansprechen korreliert. Wir haben gelernt, dass T-Zellen sehr viel effektivere Mediatoren zur Depletion von B-Zellen sind als Antikörper.“ Diese Einsichten haben auch neue Ziele für innovative Therapien definiert und weisen potenziell auch in Richtung einer erweiterten Zahl von Erkrankungen, die auf diesem Weg behandelt werden könnten. Grieshaber-Bouyer nennt in diesem Zusammenhang die Myasthenia gravis und interstitielle Lungenerkrankungen.4 Aktuell befinden sich unterschiedliche Strategien der B-Zell-Depletion in Entwicklung.
Das sind einerseits autologe und allogene Zelltherapien sowie andererseits peptidbasierte Therapien wie therapeutische Antikörper, darüber hinaus aber auch neue Strategien wie die T-Zell-Engager, die die Zytotoxizität von T-Zellen nützen. Als Target für diese Therapien kommt nicht nur CD19 infrage, das von allen B-Zell-Populationen exprimiert wird, sondern mögliche Ziele sind auch CD20, CD38, BAFF-R oder BCMA.
Bei Wirkungsverlust alternatives Target angreifen
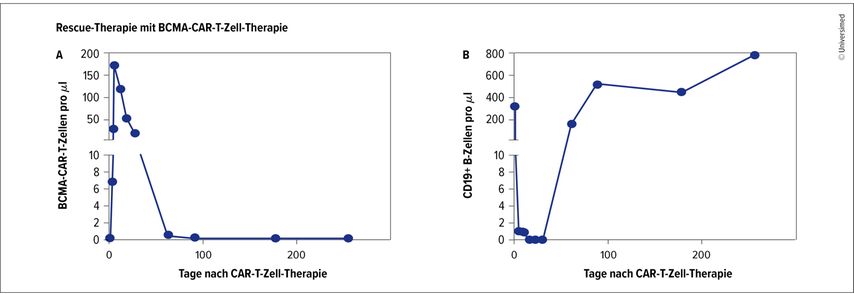
Diese alternativen Ziele werden relevant, wenn CD19-gerichtete CAR-T-Zellen nicht den gewünschten Erfolg erzielen oder es nach initialem Ansprechen zu einem Rezidiv kommt. Grieshaber-Bouyer illustriert dies anhand einer 45-jährigen Patientin mit Jo-1-positiver inflammatorischer Myositis: Nach rascher Remission unter CD19-CAR-T-Therapie trat nach neun Monaten ein Rezidiv mit Anstieg der Kreatinkinase (CK) auf.5 Eine erneute Behandlung mit dem gleichen T-Zell-Produkt blieb wirkungslos – es kam weder zur Expansion der CAR-T-Zellen noch zu einem klinischen Ansprechen, obwohl CD19-gerichtete CAR-T-Zellen im Blut nachweisbar waren.Daraufhin wurde eine Therapie mit dem Anti-CD38-Antikörper Daratumumab eingeleitet, die vorübergehend wirksam war. Im Anschluss erhielt die Patientin BCMA-gerichtete CAR-T-Zellen. BCMA („B-cell maturation antigen“) ist ein transmembranäres Glykoprotein der TNF-Rezeptorfamilie, das vor allem auf reifen B-Lymphozyten und Plasmazellen exprimiert wird.Diese Behandlung erwies sich als erfolgreich: Die CAR-T-Zellen expandierten, eliminierten Plasmazellen im lymphatischen Gewebe, senkten die Autoantikörperspiegel und führten zu einer stabilen, medikamentenfreien Remission. Vermutlich trug insbesondere die Depletion von Plasmazellen – mit geringerer CD19-, aber höherer BCMA-Expression – zu diesem Erfolg bei.5Über klassische zytotoxische Ansätze hinaus zeigen CAR-T-Zellen weiteres Potenzial: So wurde auf dem EULAR 2025 eine Phase-I-Studie mit einem regulatorischen Treg-basierten CAR-T-Produkt vorgestellt, das gegen citrullinierte Proteine (CitP) gerichtet ist. Diese spielen eine zentrale Rolle in der Pathophysiologie der rheumatoiden Arthritis und sind in entzündeter Synovia nachweisbar. Das autologe Produkt SBT-77-7101 zielt spezifisch auf CitP ab, ohne Zelldepletion zu verursachen, und soll stattdessen Immuntoleranz induzieren. Erste Daten aus drei Patient:innen zeigen ein günstiges Sicherheitsprofil.6
Abb. 1: Kinetik der Zellpopulationen nach Rescue-Therapie mit BCMA-CAR-T-Zellen. (A) BCMA-CAR-T-Zellen/µl sowie (B) CD19+ B-Zellen/µl in Abhängigkeit von der Zahl der Tage nach CAR-T-Zell-Therapie (modifiziert nach Müller F et al. 2025)5
Bispezifische Antikörper statt ge-netisch manipulierter Lymphozyten
Ein Problem der CAR-T-Zell-Therapie liegt in der langen Herstellungsdauer des Zellprodukts sowie im generell (auch finanziell) hohen Aufwand, den diese Methode erfordert. Eine Alternative könnten T-Zell-Engager darstellen. Diese führen ebenso wie CAR zu einer Aktivierung von T-Zellen gegen B-Zellen, benötigen jedoch keine gentechnische Manipulation von Zellen ex corpore. T-Zell-Engager sind künstliche Antikörperkonstrukte, die die T-Zellen des Patienten in Kontakt mit den gewünschten Zielzellen bringen. Antikörper, die gleichzeitig an eine T-Zelle und an eine Zielzelle andocken, werden als bispezifische T-Zell-Engager (BiTE) bezeichnet. Nach dem Kontakt werden die Zielzellen durch die T-Zellen abgetötet. Zielzellen können beispielsweise Krebszellen, aber auch B-Zellen sein, womit deren Depletion erreicht wird. Die Wirksamkeit dieser Technologie konnte bereits in mehreren onkologischen Indikationen nachgewiesen werden, was zu entsprechenden Zulassungen führte.
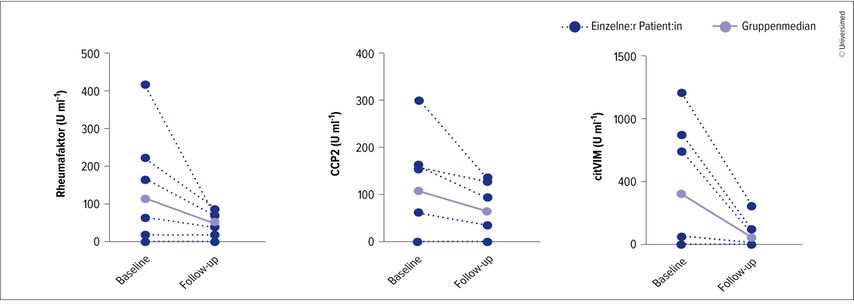
In der Indikation therapierefraktäre rheumatoide Arthritis befindet sich der gegen CD19 gerichtete T-Zell-Engager Blinatumomab (CD19xCD3-BiTE) in klinischen Studien. Nach zweimaliger Infusion des extrem niedrig dosierten BiTE kam es zu Depletion von B-Zellen, Immun-Reset und klinischem Ansprechen mit deutlicher Abnahme der druckschmerzhaften und geschwollenen Gelenke sowie Remission nach DAS28-CRP (Disease Activity Score 28 for Rheumatoid Arthritis with CRP). Die Antikörperspiegel (Rheumafaktor, Anti-CCP etc.) fielen rasch ab (Abb. 2).7 Als Nebenwirkung trat während der ersten Infusion ein kurzer Anstieg der Körpertemperatur sowie der Akutphasen-Proteine auf, es gab jedoch keine Anzeichen eines klinisch relevanten Zytokinfreisetzungssyndroms. Dennoch erfolgen die Infusionen jeweils im Rahmen eines fünftägigen Krankenhausaufenthalts. Nach 16 Wochen wurde als kostimulatorische Blockade eine Erhaltungstherapie mit Abatacept begonnen.7
Abb. 2: Therapierefraktäre RA: Reduktion der Autoantikörper nach zweimaliger Infusion eines CD19xCD3-BiTE (modifiziert nach Bucci L et al. 2024)7
Depletion von Plasmazellen bei verschiedenen Autoimmunerkrankungen
Ein Wechsel des Targets im Falle eines Rezidivs ist auch mit T-Zell-Engagern möglich, die sich auch zur Depletion von Plasmazellen eignen. Teclistamab ist ein bispezifischer Antikörper, der mit einem Arm an BCMA auf Plasmazellen bindet und mit dem anderen Arm an CD3 auf T-Lymphozyten. Teclistamab aktiviert die T-Zellen damit gegen BCMA und ist bereits zur Behandlung des multiplen Myeloms zugelassen. Bei Patient:innen mit unterschiedlichen Autoimmunerkrankungen wurde mit Teclistamab sowohl eine Reduktion der Autoantikörper als auch klinisches Ansprechen erreicht.
In die an deutschen Zentren durchgeführte Pilotstudie waren jeweils eine Patientin mit systemischer Sklerose, mit Sjögren-Syndrom, mit idiopathischer inflammatorischer Myositis und mit schwerer rheumatoider Arthritis (RA) eingeschlossen. In allen Fällen lag ein therapierefraktärer Status der Immunerkrankung nach mindestens fünf gescheiterten Immunvortherapien inklusive Rituximab vor. Die Behandlung mit Teclistamab erfolgte in aufsteigenden Dosierungen an den Tagen 1 (0,06mg/kg), 3 (0,3mg/kg) und 5 (1,5mg/kg) plus einer Erhaltungsdosis 4 bis 12 Wochen später und führte zu einer raschen Depletion sowohl der Plasma- als auch der B-Zellen.
Factbox
CAR-T-Zellen – CAR bedeutet „chimeric antigen receptor“ – sind gentechnisch veränderte T-Zellen mit synthetischen antigenspezifischen Rezeptoren, die sich bei den in der Rheumatologie eingesetzten Therapien zumeist gegen CD19 auf B-Zellen richten.Teclistamab verminderte die Krankheitsaktivität bei allen vier Patientinnen, es kam zu Symptomverbesserungen und Reduktionen der Immunglobuline bereits nach einer Woche. Bei allen Teilnehmerinnen waren mit Beginn der Studientherapie die bisherigen Immunsuppressiva abgesetzt worden. Bei der RA-Patientin sank der DAS28-CRP von 5,9 vor Beginn der experimentellen Behandlung auf 1,9 nach 12 Wochen. Bei der Patientin mit systemischer Sklerose besserte sich die Hautsymptomatik von 39 im modifizierten Rodnan Skin Score auf 24 zu Woche 22. Die antinukleären Antikörpertiter (ANA) sanken von 1:3200 auf 1:100. Auch bei der Patientin mit primärem Sjögren-Syndrom und derjenigen mit idiopathischer inflammatorischer Myositis kam es zu substanziellen Verringerungen der Krankheitsaktivität in Verbindung mit abnehmenden Autoantikörpern.8 Mittlerweile liegen zu dieser ersten Fallserie Daten aus der Nachbeobachtung über mehr als 400 Tage vor. Sechs weitere Patient:innen wurden mit Teclistamab behandelt. Bei mehreren Patient:innen – insbesondere bei drei Patient:innen mit systemischer Sklerose – führte die Behandlung mit Teclistamab zu kontinuierlicher Remission ohne zusätzliche Therapie. Bei anderen wurde das Ansprechen durch Flares unterbrochen, die mit einer neuerlichen Anwendung von Teclistamab wieder unter Kontrolle gebracht werden konnten. Lediglich in einem Fall von idiopathischer inflammatorischer Myositis wurde kein Ansprechen erreicht.9
Alles in allem stellen die T-Zell-Engager einen wichtigen Schritt in Richtung einer optimalen Immuntherapie für Autoimmunerkrankungen dar, erläutert Grieshaber-Bouyer, da sie als „Off the shelf“-Therapie im Gegensatz zu CAR-T-Zellen keine individualisierte Herstellung eines Zellprodukts benötigen, das Potenzial für wiederholten Einsatz haben und im Idealfall ambulant appliziert werden könnten. Darüber hinaus erwartet Grieshaber-Bouyer jedoch auch die Ausweitung dieser Strategie auf neue Indikationen und neue Ziele, insbesondere was die Induktion von Immuntoleranz anbelangt.
Quelle:
Session „Therapeutische Herausforderungen“, Jahreskongress der SGR 2025 am 4. und 5.9. 2025 in Interlaken
Literatur:
1 Fauconnier A et al.: Trends in the drug target landscape for autoimmune diseases. Nat Rev Drug Discov 2025; 24(6): 415-6 2 Gregersen JW, Jayne DRW: B-cell depletion in the treatment of lupus nephritis. Nat Rev Nephrol 2012; 8(9): 505-14 3 Tur C et al.: CD19-CAR T-cell therapy induces deep tissue depletion of B cells. Ann Rheum Dis 2025; 84(1): 106-14 4 Wilhelm A et al.: Selective CAR T cell-mediated B cell depletion suppresses IFN signature in SLE. JCI Insight 2024; 9(12): e179433 5 Müller F et al.: BCMA CAR T cells in a patient with relapsing idiopathic inflammatory myositis after initial and repeat therapy with CD19 CAR T cells. Nat Med 2025; 31(6): 1793-7 6 Baxter SK et al.: REGULATE-RA: A Phase 1 study of CAR-T regulatory cells targeting citrullinated proteins in refractory rheumatoid arthritis: interim safety and tolerability. EULAR 2025, POS0034 7 Bucci L et al.: Bispecific T cell engager therapy for refractory rheumatoid arthritis. Nat Med 2024; 30(6): 1593-601 8 Hagen M et al.: BCMA-targeted T-cell-engager therapy for autoimmune disease. N Engl J Med 2024; 391(9): 867-9 9 Bucci L et al.: BCMA T-Cell engager therapy in patients with refractory autoimmune disease. N Engl J Med 2025; 393(15): 1544-7
Das könnte Sie auch interessieren:
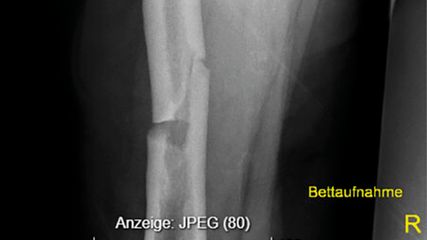
Atypische Frakturen & Bisphosphonate
Bisphosphonate sind Standard in der Osteoporosetherapie und wirksam in der Prävention osteoporotischer Frakturen. Allerdings sind sie in seltenen Fällen mit atypischen Frakturen, vor ...
Selten, aber relevant: Methotrexat kann Knochen schädigen
Bei Schmerzen und Insuffizienzfrakturen der unteren Extremität unter Therapie mit Methotrexat besteht der Verdacht auf eine seltene, aber relevante MTX-Osteopathie. Rheumatolog:innen ...
Osteologische Mythen im Faktencheck
Rund um die Osteoporose und ihre Behandlung kursieren nicht nur unter Betroffenen, sondern selbst in Fachkreisen einige falsche Annahmen. Diese halten sich hartnäckig, obwohl solide ...