Exkurs: Verschreibung cannabisbasierter Medikamente in Deutschland
Autorin:
Prof. Dr. med. Kirsten Müller-Vahl
Klinik für Psychiatrie, Sozialpsychiatrie und Psychotherapie
Medizinische Hochschule Hannover
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Zahl der verschreibungsfähigen cannabisbasierten Medikamente hat in den vergangenen Jahren kontinuierlich zugenommen. Seit einem Urteil des Bundessozialgerichts im Jahr 2022 ist präziser geregelt, wann die gesetzlichen Krankenkassen (GKV) die Kosten für eine cannabisbasierte Behandlung übernehmen müssen. Durch einen Beschluss des Gemeinsamen Bundesausschusses (G-BA) im Oktober 2024 können zahlreiche Fachärzt:innen cannabisbasierte Medikamente nun ohne vorherige Genehmigung verordnen.
Keypoints
-
Die Verordnung und insbesondere die Kostenübernahme für eine THC-haltige cannabisbasierte Therapie sind durch zahlreiche Gesetze, Gerichtsurteile und Beschlüsse des G-BA geregelt.
-
Nach wie vor gelten die 2017 vom Gesetzgeber im SGB festgelegten Kriterien für eine Kostenübernahme durch die GKV, die grundsätzlich erfüllt sein müssen: Vorliegen einer schwerwiegenden Erkrankung, Fehlen von Behandlungsalternativen und Aussicht auf einen Therapieerfolg.
-
Seit 2024 entfällt für bestimmte Fachärzt:innengruppen der Genehmigungsvorbehalt, sodass auch ohne vorherige Kostenübernahmezusage eine cannabisbasierte Therapie zulasten der GKV verordnet werden kann.
Seit Inkrafttreten des «Cannabis-als-Medizin-Gesetzes» im März 2017 können verschiedene cannabisbasierte Medikamente inklusive Medizinalcannabisblüten und daraus hergestellte Cannabisextrakte in pharmazeutischer Qualität ärztlich verordnet werden. Zum 1. April 2024 wurde Cannabis zudem in Deutschland (teil-)legalisiert bzw. der Konsum entkriminalisiert. Die genauen gesetzlichen Bestimmungen sind im Cannabisgesetz (CanG) geregelt.1 Das Medizinal-Cannabis-Gesetz, kurz MedCanG, ist nun Teil des CanG. Einzige Änderung im Hinblick auf die medizinische Verordnung von Cannabis war die Herausnahme der cannabisbasierten Medikamente aus der Betäubungsmittelverschreibungsverordnung (BtMVV). Somit sind cannabisbasierte Medikamente – mit Ausnahme von Nabilon (Canemes®) – nun keine Betäubungsmittel mehr und können auf einem rosa Rezept verordnet werden. Cannabidiol (CBD) unterlag auch zuvor nicht der BtMVV.
Verschreibungsfähige cannabisbasierte Medikamente
Gegenwärtig (Stand 06/2025) sind in Deutschland lediglich drei Fertigarzneimittel auf Cannabisbasis zugelassen: der Cannabisextrakt Nabiximols (Sativex®) für die Behandlung der mittelschweren bis schweren, therapieresistenten Spastik bei Multipler Sklerose (MS), der synthetische Tetrahydrocannabinol(THC)-Abkömmling Nabilon (Canemes®) für die Behandlung von Übelkeit und Erbrechen bei Chemotherapie und der CBD-Extrakt Epidyolex® als Zusatztherapie von Krampfanfällen bei Lennox-Gastaut-Syndrom (LGS) und Dravet-Syndrom (DS) in Verbindung mit Clobazam sowie als Zusatztherapie von Krampfanfällen bei tuberöser Sklerose (TSC).
Nabiximols (Sativex®)
Nabiximols wurde in Deutschland bereits 2011 arzneimittelrechtlich zugelassen und ist mittlerweile in 29 Ländern für die Therapie der Spastik bei MS auf dem Markt. Es ist ein auf THC und CBD im Verhältnis von etwa 1:1 standardisierter Cannabisextrakt, der zur Anwendung als Mundspray zur Verfügung steht. Ein Sprühstoss (entsprechend 100μl) enthält 2,7mg THC und 2,5mg CBD. Die zulässige Höchstdosis beträgt 12 Hübe/Tag, entsprechend 32,4mg THC. Da die Cannabinoide in einer ethanolischen Lösung gelöst sind, kann es bei der Anwendung zu Brennen oder gar Entzündungen im Mund kommen. Trotz der oromukosalen Applikation erfolgt die Aufnahme praktisch ausschließlich über den Gastrointestinaltrakt.
Nabilon (Canemes®)
Das THC-Analogon Nabilon (Canemes®) ist in Deutschland seit 2017 zugelassen. Nabilon ist ein vollsynthetisch hergestelltes Cannabinoid mit THC-ähnlicher Struktur. Es bestehen keine bedeutsamen Wirkunterschiede zwischen Nabilon und Dronabinol (THC). Eine Kapsel Nabilon enthält 1mg, was hinsichtlich der Wirkstärke etwa 7–8mg Dronabinol (THC) entspricht. Daher sind eine langsame Eindosierung und Dosissteigerung kaum möglich. Vom Hersteller wird empfohlen, eine Dosis von 6mg/Tag (3x2mg) nicht zu überschreiten.
CBD-Extrakt Epidyolex®
Seit 2019 steht mit dem Cannabidiol-Pflanzenextrakt Epidyolex® ein CBD-Fertigarzneimittel zur Verfügung. Epidyolex® wird aus einer Cannabisblütensorte («Charlottes Web») extrahiert und als ölige Lösung oral angewendet (100mg CBD/ml). In den zugelassenen Indikationen erfolgt zumeist eine Hochdosistherapie mit mehreren Hundert mg/Tag. Die zugelassene Höchstdosis beträgt 25mg pro kg Körpergewicht.
CBD als Rezepturarzneimittel
CBD kann darüber hinaus auch als Rezepturarzneimittel «no-label» verordnet werden. Da CBD – im Gegensatz zu THC-haltigen cannabisbasierten Medikamenten – keine psychedelischen Wirkungen und kein Abhängigkeitspotenzial aufweist, unterlag es zu keiner Zeit dem Betäubungsmittelgesetz (BtMG). Neben CBD-haltigen Arzneimitteln sind auch CBD-Präparate als Nahrungsergänzungsmittel oder Hygiene- und Kosmetikprodukte auf dem Markt, die aber nicht medizinisch genutzt werden sollten, da für diese Produkte nicht die strengen Qualitätsregeln wie für Arzneimittel gelten.
Dronabinol (THC)
Dronabinol (THC) ist in Deutschland bereits seit 1998 verschreibungsfähig, aber weiterhin für keine Indikation zugelassen. Dronabinol ist der internationale Freiname (INN) für das natürlich in der Cannabispflanze vorliegende Isomer des Delta-9-Tetrahydrocannabinol. Es kann vollsynthetisch hergestellt oder aus der Cannabispflanze isoliert werden. Dronabinol kann theoretisch als Fertigarzneimittel aus dem Ausland importiert werden, kommt in Deutschland aber praktisch ausschliesslich als Rezepturarzneimittel zur Anwendung. In der Apotheke kann Dronabinol entsprechend den Rezepturvorschriften in unterschiedlicher Form zubereitet werden: als ölige Dronabinol-Tropfen 25mg/ml (NRF 22.8) oder Dronabinol-Kapseln (NRF 22.7) zur oralen Einnahme oder als ethanolische Dronabinol-Lösung 10mg/ml zur Inhalation (NRF 22.16). Am häufigsten wird Dronabinol als ölige Lösung zur oralen Einnahme verordnet. Dies erlaubt nicht nur eine sehr genaue Dosierung, sondern auch eine niedrige Startdosis und eine langsame Dosissteigerung. Üblich ist eine 2,5%ige Lösung (25mg/ml) entsprechend 250mg Dronabinol in 10ml (NRF 22.8).
Vollspektrumextrakte
Neben dem zugelassenen Cannabisextrakt Nabiximols (Sativex®) ist in Deutschland eine Vielzahl von sogenannten Vollspektrumextrakten als Rezepturarzneimittel verordnungsfähig, die aus getrockneten Blüten hergestellt werden und neben THC und CBD alle weiteren Phytocannabinoide (sogenannte kleine Cannabinoide), Terpene und Flavonoide der Cannabispflanze enthalten. Extrakte werden – wie auch Medizinalcannabisblüten – auf die Gehalte an THC und CBD standardisiert und unterteilt in THC-dominante (THC>CBD), CBD-dominante (CBD>THC) und balancierte oder ausgeglichene Produkte (THC=CBD). Etwa die Hälfte der derzeit angebotenen Extrakte ist den balancierten Produkten zuzurechnen. Vollspektrumextrakte stehen mehrheitlich in Form öliger Lösungen zur oralen Einnahme zur Verfügung. Einige wenige Firmen bieten mittlerweile auch Extrakte in Kapselform, als oromukosales Spray oder zur Inhalation an. Damit soll einerseits die Handhabung vereinfacht werden. Anderseits wird mit der oromukosalen und inhalativen Applikation das Ziel verfolgt, den Wirkeintritt zu beschleunigen – ähnlich jenem bei der Inhalation von Medizinalcannabisblüten.
Medizinalcannabisblüten
Medizinalcannabisblüten können seit 2017 «no-label» als Rezepturarzneimittel verordnet werden. Bei der Bundesopiumstelle des Bundesinstituts für Arzneimittel und Medizinprodukte (BfArM) sind formal mehr als 800 verschiedene Blütensorten registriert, die theoretisch verordnet werden können. Lieferbar sind derzeit meist zwischen 150 und 200 Blütensorten, die jeweils auf die Gehalte an THC (maximal 30%) und CBD standardisiert sind. Die überwiegende Zahl der Cannabisblüten ist THC-dominant, mit einem THC-Gehalt um 20%. Bei der Verschreibung von Cannabisblüten ist die Angabe «Cannabisblüten» auf dem Rezept nicht ausreichend. Es muss stets der genaue Name der Blütensorte angegeben werden. Ferner muss das Rezept einen Vermerk zur Verarbeitung enthalten. Dies kann entweder durch die Angabe einer entsprechenden NRF-Vorschrift erfolgen (z.B. Cannabisblüten [Sorte XY], NRF 22.13.) oder aber den Vermerk «unzerkleinert». Theoretisch ist nach NRF-Vorschrift auch eine Teezubereitung möglich.
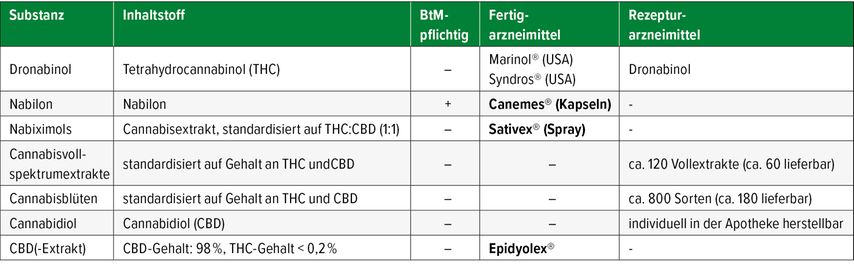
Medizinalcannabisblüten werden nach unterschiedlichen Kriterien eingeteilt. Am häufigsten erfolgt eine Einteilung in sogenannte Chemotypen in Abhängigkeit vom THC-Gehalt in THC-dominante, CBD-dominante und balancierte oder ausgeglichene Sorten. Auch wenn aus wissenschaftlicher Sicht heute von lediglich einer einzigen Cannabisspezies ausgegangen wird, nämlich Cannabis sativa L., die in drei Varietäten unterteilt wird (C. sativa L. var. sativa, C. sativa L. var. indica und C. sativa L. var. ruderalis), so hat sich im allgemeinen Sprachgebrauch auch für Medizinalcannabisblüten eine Unterscheidung in Sativa- und Indica-Sorten etabliert. Ob die den Sorten zugeschriebene Wirkweise (Sativa=anregend, Indica=entspannend) zutreffend ist, ist wissenschaftlich umstritten. Durch Kreuzungen der Varietäten (meist Sativa und Indica) entstehen sogenannte Hybride. Mittlerweile ist die Mehrzahl der verschreibungsfähigen Medizinalcannabisblüten genetisch als Hybrid zu klassifizieren. Diese können wiederum in Sativa- und Indica-dominante Sorten unterteilt werden.2 Tabelle 1 zeigt eine Übersicht über alle derzeit in Deutschland verschreibungsfähigen cannabisbasierten Medikamente.
Kostenerstattung und Genehmigungsvorbehalt
SGB V § 31 Abs. 6
Der rechtliche Rahmen im Hinblick auf die Kostenübernahme für eine Therapie mit THC-haltigen cannabisbasierten Medikamenten durch die gesetzliche Krankenversicherung (GKV) ist im Sozialgesetzbuch (SGB) V § 31 Abs. 6 geregelt.3 Diese Regelung wurde bei Inkrafttreten im Jahr 2017 als «sozialrechtliche Minirevolution» bezeichnet, da erstmals überhaupt in Deutschland die Möglichkeit geschaffen wurde, dass ein:e Patient:in Anspruch auf Übernahme der Kosten für ein nicht zugelassenes Arzneimittel im Rahmen eines «off-label-» oder «no-label use» erhält. Im Gesetz wurden als Voraussetzung für eine Kostenerstattung durch die GKV folgende Punkte festgelegt, die bis heute Gültigkeit haben:
-
Es liegt eine «schwerwiegende Erkrankung» vor.
-
Eine «allgemein anerkannte, dem medizinischen Standard entsprechende Leistung steht im Einzelfall nicht zur Verfügung» oder diese Leistung kann «im Einzelfall nach der begründeten Einschätzung der behandelnden Vertragsärztin oder des behandelnden Vertragsarztes unter Abwägung der zu erwartenden Nebenwirkungen und unter Berücksichtigung des Krankheitszustandes der oder des Versicherten nicht zur Anwendung kommen».
-
Es besteht «eine nicht ganz entfernt liegende Aussicht auf eine spürbare positive Einwirkung auf den Krankheitsverlauf oder auf die schwerwiegende Symptome».
Urteil des Bundessozialgerichts 2022
Bis Oktober 2024 musste in jedem Einzelfall vor der Verordnung eines THC-haltigen Cannabisarzneimittels zulasten der GKV ein Kostenübernahmeantrag bei der Krankenkasse gestellt werden, für den zwingend ein Arztfragebogen zu Cannabinoiden nach § 31 Abs. 6 SGB V genutzt werden musste. Infolge eines Urteils des 1. Senats des Bundessozialgerichts vom 10.11.2022 wurden die Anforderungen an die ärztlichen Ausführungen für einen solchen Kostenübernahmeantrag nochmals erhöht.4 So wurde entschieden, dass die Krankenkassen bei Vorliegen schwerer Erkrankungen die Verordnung von Cannabis zur Krankenbehandlung nur dann genehmigen dürfen, «wenn der behandelnde Arzt hierfür eine besonders sorgfältige und umfassende Einschätzung abgegeben hat». Allerdings wurde den Krankenkassen gleichzeitig lediglich noch eine Prüfmöglichkeit eingeräumt. Dazu heisst es in dem Urteil weiter: «Sind die hohen Anforderungen an diese Einschätzung erfüllt, darf die Krankenkasse das Ergebnis der ärztlichen Abwägung nur darauf hin überprüfen, ob dieses völlig unplausibel ist.» Explizit wird darüber hinaus im Rahmen des Kostenübernahmeantrags zusätzlich eine Einschätzung zum Abhängigkeitsrisiko gefordert: «Ob eine Suchtmittelabhängigkeit der Verordnung von Cannabis entgegensteht, hat der Arzt im Einzelfall ebenfalls sorgfältig abzuwägen.»
Beschluss des G-BA 2024
Im Oktober 2024 trat ein Beschluss des Gemeinsamen Bundesausschusses (G-BA) in Kraft, wonach nun auch eine Cannabisverordnung zulasten der GKV ohne vorherige Genehmigung durch die Krankenkasse möglich ist.5 Dies ist allerdings beschränkt auf Ärztinnen und Ärzte, die bestimmte Facharzt-, Schwerpunkt- oder Zusatzbezeichnungen haben, darunter Fachärzt:innen für Allgemeinmedizin, Anästhesiologie, Frauenheilkunde und Geburtshilfe mit Schwerpunkt gynäkologische Onkologie, innere Medizin, Neurologie, physikalische und rehabilitative Medizin sowie Psychiatrie und Psychotherapie. In dem Beschluss heisst es aber, dass diese Fachärzt:innen bei «Unsicherheiten, ob bei einer Patientin oder einem Patienten die Voraussetzungen für eine Cannabisverordnung gegeben sind», auch weiterhin eine Genehmigung der Cannabisverordnung bei der Krankenkasse beantragen können.
Regress
Unklar ist momentan, wie hoch das Regressrisiko für Ärzt:innen ist, wenn THC-haltige cannabisbasierte Medikamente ohne vorherige Kostenübernahmezusage verordnet werden. Der G-BA führte dazu aus: «Deshalb können auch fachlich ausreichend qualifizierte Ärztinnen und Ärzte eine Genehmigung der Verordnung bei der Krankenkasse beantragen, auch um finanziellen Rückforderungen der Krankenkasse (Regress) vorzubeugen. Eine abschliessende Prüfung, ob auch eine wirtschaftlichere Auswahl des Cannabisprodukts möglich gewesen wäre, ist mit einer Genehmigung aber nicht verbunden.»5 Auch wenn der Wegfall des Genehmigungsvorbehalts eine langjährige Forderung zahlreicher Verbände und Ärzt:innen war, so ist nun eine gewisse Verunsicherung eingetreten, wie hoch tatsächlich das Regressrisiko ist. Seit Inkrafttreten des Medizincannabisgesetzes im Jahr 2017 ist die Zahl der Regressforderungen insgesamt aber sehr gering und betrifft überwiegend Verordnungen von Medizinalcannabisblüten in extrem hohen Dosierungen.
Wirtschaftlichkeitsgebot
Ungeachtet dieser Regelungen gelten auch für die Verordnung von Arzneimitteln auf Cannabisbasis die Regelungen der Wirtschaftlichkeitsprüfung nach §§ 106 ff. SGB V. Im Urteil des Bundessozialgerichts vom 10.11.2022 heisst es dazu: «Bei der Auswahl der Darreichungsform und der Verordnungsmenge hat der Vertragsarzt das allgemeine Wirtschaftlichkeitsgebot zu beachten. Insoweit steht ihm keine Einschätzungsprärogative zu. Bei voraussichtlich gleicher Geeignetheit von Cannabisblüten, Cannabisextrakten und Arzneimitteln mit den Wirkstoffen Dronabinol oder Nabilon besteht nur ein Anspruch auf Versorgung mit dem kostengünstigsten Mittel. Die Krankenkasse ist berechtigt, trotz Erfüllung der Anspruchsvoraussetzungen die Genehmigung der vom Vertragsarzt beabsichtigten Verordnung zu verweigern und auf eine günstigere, voraussichtlich gleich geeignete Darreichungsform zu verweisen.»4
Weitere Regelungen
Bereits im März 2023 beschloss der G-BA, dass nur die Erstverordnung von Cannabis sowie ein grundlegender Therapiewechsel der Genehmigung durch die Krankenkassen bedürfen.6 Folgeverordnungen, Dosisanpassungen oder der Wechsel zu anderen getrockneten Blüten oder zu anderen Extrakten in standardisierter Form bedürfen grundsätzlich keiner erneuten Genehmigung. Sofern eine Genehmigung für eine Therapie mit Cannabis früher bereits einmal erteilt wurde, gilt diese dauerhaft. Auch Cannabisverordnungen im Rahmen der spezialisierten ambulanten Palliativversorgung bedürfen grundsätzlich keiner Genehmigung. Für Verordnungen im Rahmen der allgemeinen ambulanten Palliativversorgung oder bei Beginn einer Cannabistherapie bereits während einer stationären Behandlung besteht eine verkürzte Prüffrist der Krankenkassen von lediglich drei Tagen. Ansonsten beträgt diese Frist zwei Wochen und bei Einbeziehung des Medizinischen Dienstes vier Wochen. Zu beachten ist, dass der G-BA bei einer Verordnung zulasten der GKV festgelegt hat, dass vor einer Verordnung von Cannabis in Form von getrockneten Blüten oder Extrakten zu prüfen ist, ob andere cannabishaltige Fertigarzneimittel zur Verfügung stehen, die zur Behandlung geeignet sind. Die Verordnung von Cannabis in Form von getrockneten Blüten ist zu begründen.
Literatur:
1 BMG: Cannabisgesetz (CanG) www.bundesgesundheitsministerium.de/service/gesetze-und-verordnungen/detail/cannabisgesetz.html (zuletzt aufgerufen am 12. Mai 2025) 2 Müller-Vahl KR, Grotenhermen F: Cannabis und Cannabinoide in der Medizin. 2., aktualisierte Auflage. Medizinisch-Wissenschaftliche Verlagsgesellschaft; 2024; 3 § 31 SGB 5 – Einzelnorm. 4 Aktenzeichen B 1 KR 21/21 R, B 1 KR 28/21 R, B 1 KR 9/22 R, B 1 KR 19/22 R, Bundessozialgericht – Entscheidungen (ab 2018) www.bsg.bund.de/SharedDocs/Entscheidungen/DE/2022/2022_11_10_B_01_KR_28_21_R.html (zuletzt aufgerufen am 12. Mai 2025) 5 Meldung G-BA vom 16. Oktober 2024, www.g-ba.de/presse/pressemitteilungen-meldungen/1210/ (zuletzt aufgerufen am 12. Mai 2025) 6 Pressemitteilung G-BA vom 16. März 2023, www.g-ba.de/presse/pressemitteilungen-meldungen/1098/ (zuletzt aufgerufen am 26. Mai 2023)
Das könnte Sie auch interessieren:
Von RED-S bis zu Essstörungen bei Athletinnen und Athleten
In Chur lud im Februar wieder die Schweizerische Gesellschaft für Sportpsychiatrie und -psychotherapie (SGSPP) zur Jahrestagung ein. Ein grosses Thema dabei waren Ernährungsproblematiken ...
Besonderheiten in Symptomatik, Schwangerschaft und Stillzeit bei Frauen mit ADHS: Diagnostik und Therapie
Mädchen und Frauen mit ADHS erhalten seltener eine Diagnose, da sie weniger durch auffälliges oder externalisierendes Verhalten in Erscheinung treten. Unbehandelt kann ADHS jedoch zu ...
Psychopharmaka bei Menschen mit Störungen der intellektuellen Entwicklung – Richtlinien und Evidenzen
Menschen mit Störungen der intellektuellen Entwicklung (SIE) erhalten deutlich häufiger Psychopharmaka als Menschen ohne SIE. Neben einer klaren, diagnosebezogenen Indikation werden ...