
Wie entwickelt sich die Sarkomchirurgie?
Die Chirurgie erzielt von allen Therapiemodalitäten bei Sarkomen die höchste Lokalkontrollrate. Das primäre Ziel der Sarkomchirurgie besteht darin, den Tumor mikroskopisch komplett zu entfernen. Grundsätzlich kann davon ausgegangen werden, dass, je weiter reseziert wird, desto potenziell besser dieses Ziel erreichbar ist bzw. umso höher die lokale Tumorkontrollrate ist, aber umso potenziell schlechter die resultierende Funktion.
Keypoints
-
Transdisziplinäre Sarkomchirurgie-Kompetenzteams bilden, um die R0-Resektionsrate zu verbessern bzw. die Rate der «Whoops»-Resektionen zu senken
-
Sarkombehandlung vom in sich abgeschlossenen Disziplinen-Denken zum offenen Netzwerkverhalten entwickeln
-
«Real world data»-Register führen, welche das Management vom Sarkomboard mit dem Register koppeln
-
Qualitätsindikatoren definieren und analysieren, die Arzt- und Patienten-basiert sind
Im Gegensatz zu Karzinomen, die nur im Verbund wachsen, können peritumorale Sarkom-Satellitenzellen als Einzelzelle wieder zu einem Rezidiv heranwachsen. Eine Nachresektion macht deswegen – im Gegensatz zu Karzinomen – nur Sinn, wenn das komplette Tumorbett miteinbezogen wird. Zudem wird eine adäquate Resektion, nebst der Komponente des individuellen Chirurgen, auch durch das biologische Wachstumsmuster der einzelnen Sarkomentität sowie von der lokalen Anatomie beeinflusst («anatomische Grenzen»). Die R0-Resektion ist deswegen in der Sarkomchirurgie ein zentraler, hochkomplexer Parameter – keine andere Therapiemodalität kann für eine inadäquate Resektion kompensieren. «Worst case scenario» chirurgischerseits ist die ungeplante Operation mit Überraschungsresultat «Sarkom» (sog. «whoops lesion»).
Wo liegen die grössten Herausforderungen?
Die wichtigsten Parameter betreffend lokale Tumorkontrolle sind der erzielte chirurgische Resektionsrand bzw. ungeplante Operationen («whoops»); diese sind wichtiger als Grading, Grösse und Lage des Tumors.1 Obwohl die R0-Resektion einen zentralen Parameter in der Sarkombehandlung darstellt, ist kaum bekannt, wie häufig eine solche erreicht wird. Eine der Erklärungen liegt darin, dass keine einheitliche Definition für «R0» besteht:
-
Rein metrisch, oder in Abhängigkeit von biologischen Strukturen und anatomischen Barrieren?
-
Mitberücksichtigung neoadjuvanter Therapien?
-
Angabe definiert vom Chirurgen, vom Pathologen oder aber aus der Synthese der beiden nach interdisziplinärer Diskussion?
Zudem undefiniert: Wie wird sichergestellt, dass nicht die postoperative Aufarbeitung des Resektates durch den Pathologen selbst zu einem iatrogenen Resektionsrand führt?
Ungeplante Resektionen («Whoops»- Operationen) nach dem Motto «Schneiden wir den Tumor raus, um zu sehen, was es ist», stellen ein internationales Problem dar und führen häufig zu inadäquaten Resektionen mit potenziellem lokalem Kontrollverlust des Tumors.2 Rund 20% aller Sarkome werden auch heute noch auf diese Weise diagnostiziert/operiert, was eine sehr grosse Herausforderung für das allfällig weiterbehandelnde Sarkomteam («best case») darstellt. «Whoops»-Operationen bedeuten für betroffene Patienten eine verzögerte korrekte Behandlung, oft zusätzliche Eingriffe, nicht selten letztlich eine dadurch ab initio schlechtere Prognose. Um diese vielfältigen Herausforderungen meistern zu können, ist ein prätherapeutischer transdisziplinärer Austausch mittels einer gemeinsamen Plattform (Multidisziplinäres Tumorboard, MTB) unabdingbar, zur Definition einerseits des Resektionsrandes und andererseits der weiteren interdisziplinären Abläufe zur Abklärung bzw. Behandlung von Patienten mit Sarkomverdacht.
Was ist Sarkomchirurgie?
Die Sarkomchirurgie stellt keine eigentliche Disziplin dar, sie setzt sich vielmehr aus verschiedenen Disziplinen zusammen, in Abhängigkeit von der anatomischen Lage des Sarkoms. Sarkomchirurgie ist deshalb nicht Disziplin-fokussiert, sondern vielmehr Problem-orientiert. Da die Chirurgie je nach anatomischer Region technisch hochspezialisiert ist, können prinzipiell nicht alle Operationen von einer Person auf technisch höchstem Niveau durchgeführt werden.
Wie wird ein Sarkomchirurg definiert?3 Er hat eine entsprechende vertiefte zusätzliche onkologische Ausbildung auszuweisen, eine >10-jährige Berufserfahrung auf dem Fachgebiet und ist mit den Prinzipien der Sarkomchirurgie vertraut. Darüber hinaus muss er fähig/willig sein, in einer entsprechenden Struktur und Kultur ein Team von technisch versierten Chirurgen-Kollegen einbeziehen zu können, um die anatomischen Erfordernisse ausreichend adressieren zu können (intraprofessionelle Kooperation). Dies gilt sowohl für die Resektion eines Tumors als auch für die anschliessende Rekonstruktion. Dabei geht es immer um die Balance zwischen Tumorkontrolle und resultierender Funktion; diese muss eng abgesprochen werden mit dem Patienten und im Behandlungsteam (Abb. 1). Einen solch engen Austausch hat ein Sarkomchirurg mit dem Pathologen und dem Facharzt für interventionelle Radiologie zu etablieren, um die Abklärung von Patienten mit mesenchymalen Tumoren als Abklärungseinheit möglichst zielgerichtet umzusetzen, damit die Rate der ungeplanten Resektionen gesenkt werden kann; dasselbe gilt für die gemeinsame weitere Therapieplanung im Hinblick auf adjuvante Therapien (interprofessionelle Kooperation).
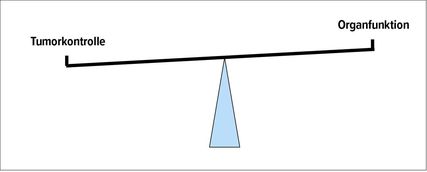
Abb. 1: Das Sarkombehandlungsteam muss zu Beginn mit dem Patienten festlegen, welches Ausmass eine Tumorresektion einnimmt, welche funktionellen Konsequenzen eine solche nach sich zieht und inwieweit dies direkt mit der Tumorkontrolle assoziiert ist
Diese Überlegungen führen als Konsequenz zur Bildung eines Sarkom-Kompetenzteams, in dem alle erforderlichen Ansprüche transdisziplinär auf den Patienten massgeschneidert unter der Koordination des Sarkomchirurgen orchestriert werden. Es wird dabei inskünftig zentral sein, dass die Leistung eines solchen transdisziplinären Sarkom-Kompetenzteams nicht mehr isoliert wie bisher, sondern Outcome-basiert als Einheitsleistung erfasst und ausgewiesen wird, mittels eines Registers, das die Daten und Qualitätsparameter aller Disziplinen miteinschliesst (Abb. 2).
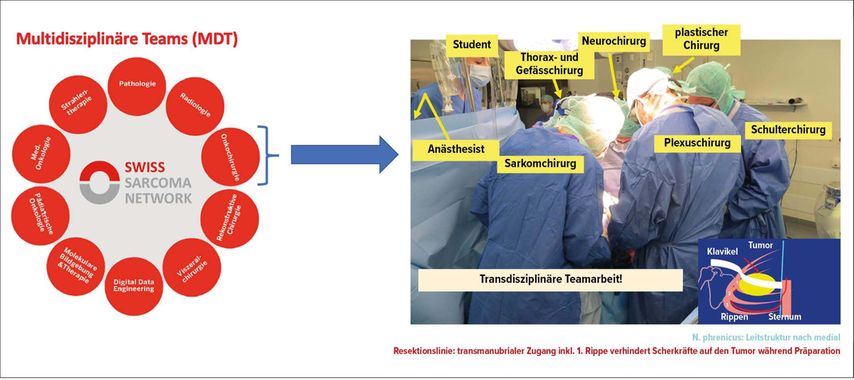
Abb. 2: Die Organisation einer Sarkomeinheit in multidisziplinären Teams – in Analogie zum chirurgischen multidisziplinären Kompetenzteam – ist entscheidend für die optimale Behandlung der Sarkompatienten. Eine solche Einheit verwendet optimalerweise eine gemeinsame digitale Plattform zum nationalen und internationalen Austausch und zur Definition und Erfassung der Qualität
«The power of data bases»
Wieso ist ein transdisziplinäres Register notwendig? Die «French sarcoma group» bildete 2010 ein Sarkomregister; mittlerweile sind bereits mehr als 55000 Patienten eingeschlossen, das Register stellt damit die derzeit grösste existierende Sarkom-Informationsquelle dar.4 Die Franzosen konnten damit zeigen, dass zum Beispiel die Fallbesprechung an einem interdisziplinären Tumorboard assoziiert ist mit besserem rezidivfreiem (sowohl lokal wie systemisch) Überleben, weniger Reoperationen und einem besseren Umsetzen der «clinical practice guidelines».5 Sie zeigten auch die Wichtigkeit eines Zweit-Reviews der Diagnose durch einen weiteren Fachpathologen: In einem Kollektiv von 1017 Patienten musste bei 27% eine Revision der Diagnose vorgenommen werden, die eine relevante Änderung der Therapie nach sich zog.6 Sie zeigten zudem, dass, wenn die Operation innerhalb des Netzwerks stattfand, die R0-Resektionsrate deutlich höher war (R0-Resektionsrate innerhalb des Netzwerkes bei 52%, ausserhalb nur gerade 26%) und dies assoziiert war mit besserem Lokalrezidiv-freiem, ereignisfreiem sowie Gesamtüberleben.7 Diese Daten erlauben grundlegende Rückschlüsse mit sehr grosser Bedeutung für unseren klinischen Alltag, so wie wir sie bisher nicht kannten.
Was sind die Ansprüche an ein Register?
Ein Register ist ein zentraler Pfeiler, um die Qualität der Patientenbehandlung zu erfassen bzw. die Teamkompetenz zu verbessern. Aufgrund obiger Ausführungen ist evident, dass ein Sarkomregister alle Disziplinen gleichzeitig einzuschliessen hat (Endresultat definiert durch schwächstes Glied in der Kette). Mittlerweile ist die Wichtigkeit von «real world data» erkannt und etabliert. Das Sarkomboard ist der einzige Moment in der Prozesskette, in dem sich alle Disziplinen zur Diskussion der Faktenlage und der weiteren Strategien der Behandlung der Sarkompatienten treffen – dieser Schlüsselmoment muss in einem «Real world data»-Register entsprechend abgebildet werden. Es ist deshalb notwendig, das gesamte Sarkomboard-Management mit dem Register zu koppeln. Ein Sarkomregister muss erlauben, alle aktuellen WHO(«World Health Organization»)-Diagnosen und anatomischen Lokalisationen zu erfassen, idealerweise auch alle Arten von chirurgischen Resektionen und Rekonstruktionen.
Das Register erlaubt die Analyse eines jeden einzelnen Parameters und jegliche Kombination derselben sowie Standard- und spezifische Auswertungen (wie zum Beispiel Qualitätsindikatoren) pro gewählte Zeiteinheit. Da die «patient-reported outcome measures» (PROM) auch in Europa zunehmend wichtiger werden, sollte ein solches System ebenfalls erlauben, entsprechende Rückmeldungen seitens der Patienten im Follow-up zu ergänzen.
Ein solches Tool erlaubt nicht nur den erleichterten transdisziplinären Austausch im Alltag, sondern wird auch die Basis darstellen, um die Qualität der Sarkombehandlung zu definieren und zu messen («outcome measurement») – letztlich der einzig rechtfertigende Parameter für die Anerkennung eines solchen MDT bzw. die einzige Möglichkeit für den Vergleich der Analysen mit anderen Zentren.
Definition und Erfassung von Qualitätsindikatoren
In der Schweiz, wie auch in anderen Ländern, wird es ab Januar 2021 eine gesetzliche Grundlage und damit Verpflichtung zur Qualitätserfassung geben. Der Ausweis von Qualität in der Sarkombehandlung bezieht sich aber nicht nur auf die Sarkomchirurgie, sondern auf die gesamte Organisationseinheit (s. oben). Die Analyse diverser Parameter bei Patienten mit Bindegewebstumoren (z.B.: Wie lange dauert das Erstellen einer Diagnose? Wird eine Biopsie vor Behandlungsbeginn durchgeführt? Wartezeiten auf einzelne Aktionsschritte?) ist ein Qualitätsausweis – bislang kaum beachtet und entsprechend kaum erfasst. Ebenso sollte Sarkomchirurgie hinsichtlich deren Komplexität und Qualität analysierbar werden, genauso die Chemotherapie und Radiotherapie. PROM müssen hier ebenfalls als Ergänzung eingebracht werden. Idealerweise soll ein «Real world data»-Register alle diese Herausforderungen abdecken.
Erwartungen und Ausblick
Die Sarkomchirurgie wird sich vom monodisziplinären Denken lösen und sich zunehmend transdisziplinär organisieren müssen. Nur so können wir jeder spezifischen initialen Präsentation eines einzelnen Patienten onkochirurgisch sowie anatomisch-technisch gerecht werden. Durch die Organisation im Sinne eines Sarkom-Kompetenzteams wird erwarteterweise7 die R0-Resektionsrate verbessert und die Rate ungeplanter Resektionen gesenkt. Dieses transdisziplinäre Denken ist seitens aller beteiligten Disziplinen erforderlich.
Es zeichnet sich damit ab, dass eine solche Kompetenzeinheit nicht an einer einzelnen Institution angesiedelt sein kann, sondern überregional/national in einem Netzwerk organisiert sein muss, um das Wissen der Experten und die Behandlung der Patienten unabhängig von der geografischen Lokalisation zu maximieren.
Autoren:
Prof. Dr. med. Dr. sc. nat. Bruno Fuchs1
Prof. Dr. med. Beata Bode2
Prof. Dr. med. Gabriela Studer3
Prof. Dr. med. Stefan Breitenstein4
1 Chair SwissSarcomaNetwork, Chefarzt Orthopädische Onkologie/Sarkomzentrum
Kantonsspitäler Winterthur und Luzern, Universitätsspital Zürich
2 Leitende Ärztin Pathologie
Pathologiezentrum Enge
Universität Zürich
3 Chefärztin Radio-Onkologie
Kantonsspital Luzern
4 Direktor Departement Chirurgie
Chefarzt Viszeral- und Thoraxchirurgie
Kantonsspital Winterthur
E-Mail: fuchs@sarcoma.surgery
Literatur:
1 Biau D et al.: Local recurrence of localized soft tissue sarcoma: a new look at old predictors. Cancer 2012; 118(23): 5867-77 2 Pretell-Mazzini J et al.: Unplanned excision of soft-tissue sarcomas: current concepts for management and prognosis. J Bone Joint Surg Am 2015; 97(7): 597-603 3 Balch C: What is a surgical oncologist? Ann Surg Oncol 2018: 25(1): 7-9 4 Amadeo B et al.: Incidence and time trends of sarcoma (2000-2013): results from the Frenchnetwork of cancer registries (FRANCIM). BMC Cancer 2020; 20(1): 190 5 Blay JY et al.: Improved survival using specialized multidisciplinary board in sarcoma patients. Ann Oncol 2017; 28(11): 2852-9 6 Perrier L et al.: The cost-saving effect of centralized histological reviews with soft tissue and visceral sarcomas, GIST, and desmoid tumors: The experiences of the pathologists of the French Sarcoma Group. PLoS One 2018; 13(4): e0193330 7 Blay JY et al.: NETSARC/REPPS/RESOS and French Sarcoma Group–Groupe d’Etude des Tumeurs Osseuses (GSF-GETO) Networks. Surgery in reference centers improves survival of sarcoma patients: a nationwide study. Ann Oncol 2019; 30(7): 1143-53
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...


