
Virtuell, doch nicht weniger fesselnd
Gynäkologisches Tumorzentrum<br>Universitätsspital Basel<br>E-Mail: viola.heinzelmann@usb.ch
Gynäkologisches Tumorzentrum<br>Universitätsspital Basel
Aufgrund der Covid-19-Pandemie fand der diesjährige Kongress der ASCO(American Society of Clinical Oncology)virtuell statt. Das Programm und die Neuerungen waren jedoch nicht weniger spannend als an den bisherigen Kongressen und boten in jedem Teilgebiet aufregende Neuerungen, insbesondere im operativen Bereich, doch auch im Bereich der Systemtherapie der gynäkologischen Karzinome. Der Artikel gibt Ihnen die wichtigsten Abstracts mit einer kurzen Interpretation der Autoren wieder.
Keypoints
-
Eine erneute chirurgische Behandlung beim rezidivierten Ovarialkarzinom erscheint sinnvoll und lebensverlängernd bei gut selektionierten Patientinnen und operativer Expertise.
-
Die Behandlung mit PARP-Inhibitoren ist mittlerweile ein Standard. Im Rezidiv sind nach 5 Jahren immer noch rund 28% aller Patientinnen unter Therapie ohne weitere Folgetherapie.
-
Carboplatin-basierte Chemotherapie bleibt auch im Rezidiv die wichtigste Therapie. Eine Chemotherapie-freie Kombination mit Olaparib/Cediranib scheint nicht besser zu sein bzgl. Ansprechen und PFS.
-
Im Bereich der Immuntherapie braucht es weitere Forschung, die Therapie erscheint bei Subtypen wie dem klarzelligen Ovarialkarzinom am vielversprechendsten. Es braucht eine gute Tumor-/Patientenselektion mit klaren prädiktiven molekularen Markern.
-
Bei einer seltenen gynäkologischen Tumorerkrankung der GTD scheint die Immuntherapie mit Avelumab gut zu funktionieren.
Operative Therapie des rezidivierten «Platin is an option»- Ovarialkarzinoms
Mit Spannung wurden die Follow-up/Survival-Daten der Desktop-III-Studie erwartet.1 Die Studie randomisierte Patientinnen mit«Platin is an option»-Rezidiv zu sekundärem Debulking und ggf. Chemotherapie oder zu alleiniger Chemotherapie. Die Patientinnen wurden nach dem prospektiv validierten Arbeitsgemeinschaft-für-Gynäkologische-Onkologie(AGO)-Score aus der Desktop-I-Studie selektioniert (Tab. 1).
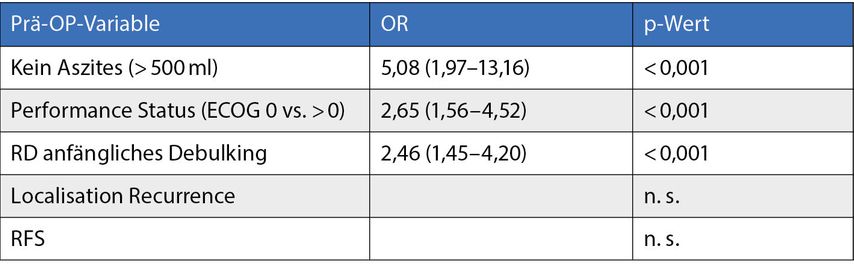
Tab. 1: Prädiktoren einer optimalen sekundären Zytoreduktion nach der DESKTOP-I-Studie (AGO). Retrospektive Analyse, n=267. ECOG, Eastern Cooperative Oncology Group; RD, «residual disease»; RFS, «relapse free survival». Modifiziert nach 9, 10
In die DESKTOP-III-Studie wurden 407 Patientinnen eingeschlossen. Eine komplette Resektion konnte bei 75% erreicht werden. Der primäre Endpunkt der Studie («overall survival», OS) war mit 53,7 vs. 46,2 Monate (HR: 0,76; 95% CI: 0,59–0,97; p=0,03) statistisch signifikant verlängert. Auch das mediane progressionsfreie Überleben (PFS) war mit 18,4 vs. 14 Monate verlängert (HR: 0,66; 95% CI: 0,54–0,82; p<0,001). Die Studie verdeutlicht klar, wie wichtig die richtige Patientinnenselektion und die Expertise des operativen Zentrums für das Outcome sind. Ohne eine komplette Resektion zu erreichen war gleich schlecht als ob kein operativer Versuch unternommen worden wäre.
Zeitgleich wurden auch die Resultate der SOC-I-Studie aus Shanghai vorgestellt, die dieselbe Fragestellung wie DESKTOP III untersuchte.2 Hierbei wurden die Ergebnisse der Interimsanalyse bzgl. OS und PFS gezeigt, die identisch mit den Resultaten der DESKTOP-III-Studie sind und ebenfalls einen klaren Benefit aufzeigen. In dieser Studie wurde der potenzielle Benefit einer R0-Resektion durch den iMODEL- Score und den Einsatz von Positronenemissionstomografie (PET-CT) untersucht. Das mediane PFS lag bei 17,4 Monaten (Chirurgie/Chemotherapie-Arm) vs. 11,9 Monate (Chemotherapie-Arm) (HR: 0,58; 95% CI: 0,45–0,74; p<0,001).
Zur Fragestellung des sekundären Debulkings in der «Platin is an option»-Situation gibt es noch eine dritte vergleichbare Studie, die GOG-213 von Coleman et al.3 Die Coleman-Studie zeigte keinen Benefit hinsichtlich des OS, jedoch war eine grosse Zahl an Patientinnen mit Bevacizumab behandelt worden, und im Gegensatz zu den anderen beiden Studien lag der Patientinnenselektion kein Score zugrunde. Der bestvalidierte Score ist sicher der AGO-Score. Tabelle 2 bietet eine Übersicht über die drei erwähnten Studien.
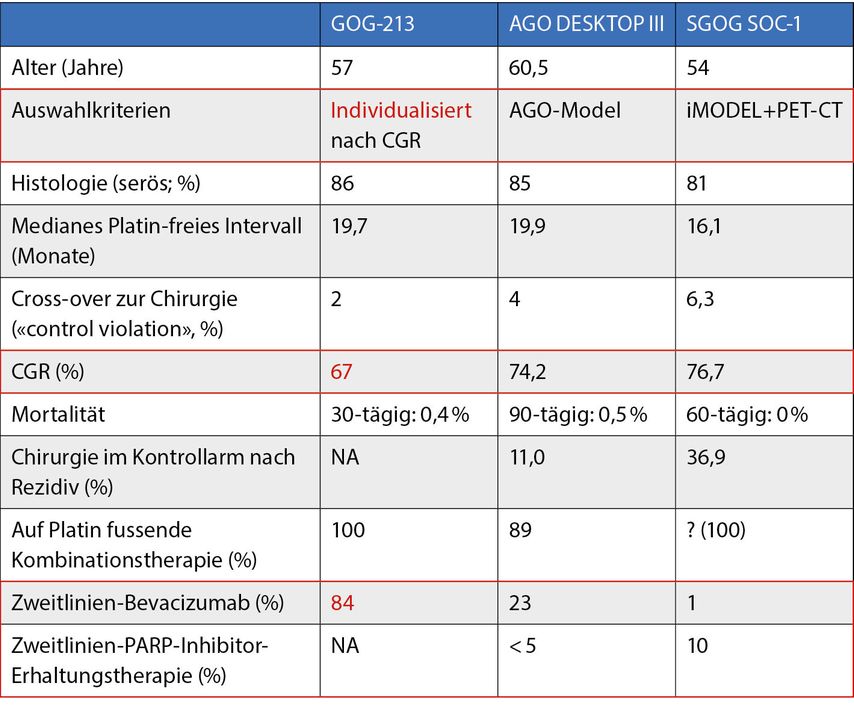
Tab. 2: Vergleich der GOG-213-, DESKTOP-III- und SOC-1-Studie. CGR, «complete gross resection». Modifiziert nach 11
Die Forschung auf dem Gebiet geht sicher weiter, insbesondere besteht auch die Frage des Stellenwerts moderner Systemtherapie wie der Poly-ADP-Ribose-Polymerase(PARP)-Inhibitoren Olaparib, Niraparib, Veliparib und Rucaparib im Rezidiv nach sekundärem Debulking. Wichtig ist zu bedenken, dass die Patientinnenselektion und die Erfahrung des operativen Zentrums ausschlaggebend sind. Eine Operation, in der keine vollständige Resektion erzielt werden kann, sollte abgebrochen werden, da sie zu Morbidität, aber keinem Outcome-Vorteil führt.
PARP-Inhibitoren beim Ovarialkarzinom
PARP-Inhibitoren gehören seit mehreren Jahren zur Standard-Erhaltungstherapie beim high-grade epithelialen Ovarialkarzinom. Mehr als 50% aller serösen high-grade Karzinome weisen eine «BRCAness» auf und sind damit sensibel auf diese Therapieform. Am ASCOMeeting 2020 wurden mehrere interessante Arbeiten zu PARP-Inhibitoren präsentiert. Hervorheben wollen wir die ersten OS-Daten, die jetzt von der SOLO2-Studie4 vorliegen, sowie die Kombinationsdaten von Olaparib und Cediranib.
In der SOLO2-Studie wurden Patientinnen mit «Breast cancer»(BRCA)-Mutation und einem «Platin is an option»-Rezidiv zu einer Therapie mit Olaparib oder Placebo randomisiert. Das mediane OS in der Intention-to-treat(ITT)-Analyse lag in der PARP-Inhibitor-Gruppe bei 51,7 Monaten und in der Placebogruppe bei 38,8 Monaten (HR: 0,74; 95% CI: 0,54–1,00; p=0,0537). Nach 5-jährigem Follow-up waren 28,3% der Patientinnen unter Olaparib am Leben und hatten noch keine weitere Folgetherapie. Zu bedenken ist hierbei, dass in der Placebogruppe viele Patientinnen sukzessive eine Therapie mit PARP-Inhibitoren erhalten hatten. Wenn diese Information mit einberechnet wurde (Placeboarm adjusted), betrug die HR sogar 0,56 (51,7 vs. 35,4 Monate)(Abb. 1).
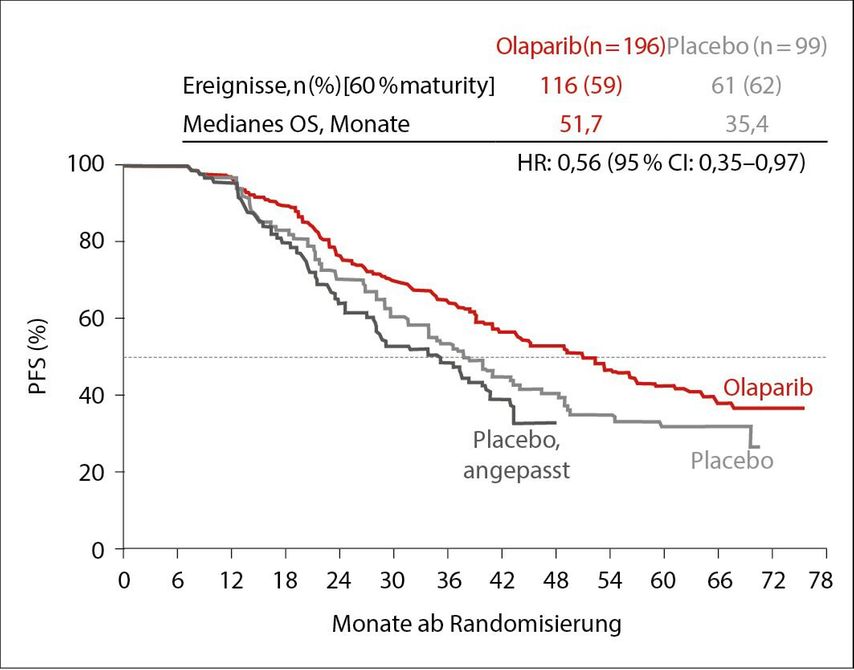
Abb. 1: Finale Analyse des OS, in der Placebogruppe angepasst an die 38% der Patientinnen, die eine darauffolgende PARP-Inhibitor-Therapie erhielten. Das mediane OS verbesserte sich um 16,3 Monate (Olaparib-Erhaltungstherapie vs. Placebo). Modifiziert nach 12
Zur Kombinationstherapie PARP-Inhibitoren und Anti-Angiogenese lagen im Rezidiv bislang Resultate von zwei Phase-II-Studien vor (Tab. 3). Beide Studien zeigten einen klaren Benefit bei der Kombination von PARP-Inhibitoren mit einem Anti-Angiogenese-Hemmer, entweder in Kombination Olaparib/Cediranib (bei Liu et al.) oder Niraparib/Bevacizumab (AVANOVA2). Im Vorfeld wurden die Kombinationsdaten gezeigt; die Chemotherapie-freie Behandlung mit Cediranib und Olaparib zeigte ein langes PFS von 17 Monaten, welches im Vergleich zu anderen Studien in dieser Situation genauso gut wie Chemotherapie war. Es wurde also mit Spannung auf die Phase-III-Daten gewartet, die Dr. med. Liu am ASCO-Kongress 2020 vorstellte.
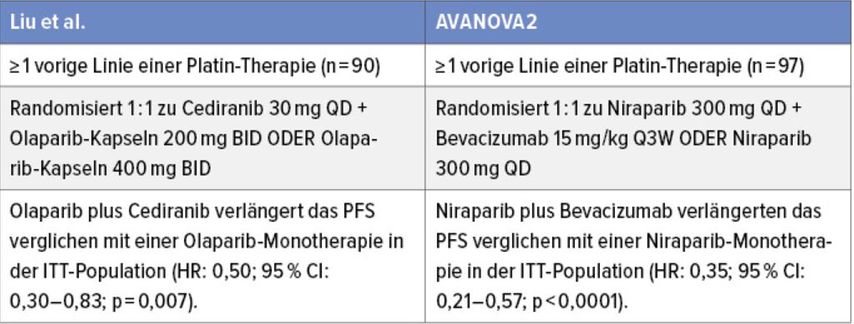
Tab. 3: Phase-II-Studien zur Kombinationstherapie mit PARP- und Angiogenese-Inhibitoren. Modifiziert nach 13, 14, 15
Hierbei wurde im «Platin is an option»-Rezidiv das Chemotherapie-freie Regime von Olaparib und Cediranib mit der Standard-Zweitlinien-Chemotherapie und einer Olaparib-Monotherapie verglichen. Cediranib ist ein potenter Tyrosinkinase-Inhibitor (TKI, Multikinase-Inhibitor) gegen den «vascular endothelial growth factor» (VEGFR) 1,2,3, wobei es in der Studie darum ging, ob die beiden Chemotherapie-freien Regime besser als die Standard-of-Care-Chemotherapie war.5 Das mediane PFS lag bei 10,3 Monaten (Chemotherapie), 8,2 Monaten (Olaparib) und 10,4 Monaten (Olaparib/Cediranib). Die Ansprechraten lagen bei 71,3% (Chemotherapie), 52,4% (Olaparib) und 69,4% (Olaparib/Cediranib). Damit konnte keine Überlegenheit der Olaparib/Cediranib-Kombination gegenüber Chemotherapie gezeigt werden. Ob eine Chemotherapie mit anschliessender Olaparib/Cediranib-Kombination ein besseres Outcome zeigen würde, bleibt zu prüfen. Als Gründe für die Diskrepanz zwischen den Phase-II- und den Phase-III-Daten könnten drei Unterschiede verantwortlich sein. Erstens die Patientinnen-Selektion: In der Phase-II-Studie hatten 50% der Patientinnen eine Keimbahn-BRCA(gBRCA)-Mutation, während dies in der Phase III nur bei 24% der Fall war; die vorherige Chemotherapie-Linien-Anzahl war in der Phase II im Vergleich zur Phase-III-Studie nicht balanciert; in der Phase III waren 25% der Patientinnen über 70 Jahre alt. Zweitens die Dosierung: Olaparib wurde in der Phase II als Kapsel, in der Phase III als Tablette verabreicht. Drittens das Nebenwirkungs-Management: In der Phase-II-Studie beendeten nur 27% der Patientinnen wegen Nebenwirkungen die Studie, in der Phase III waren dies jedoch 43% der Patientinnen.
Andere neue Therapiekonzepte beim epithelialen Ovarialkarzinom
Seit Längerem wird der Folat-Rezeptor (FLR) beim Ovarialkarzinom untersucht, er scheint ein guter Angriffspunkt zu sein, da er beim Ovarialkarzinom hoch exprimiert ist. Bei über 90% der Ovarialkarzinome lässt sich der FLR nachweisen. Mirvetuximab soravtansine (MIRV) ist ein Antibody-Drug-
Konjugat aus FR-alpha-bindenden Antikörpern, einem Linker und einem Chemotherapeutikum namens Maytansinoid DM4. In die am ASCO-Kongress gezeigte Phase-IB-Studie konnten Patientinnen mit und ohne «platinum is an option» im Rezidiv eingeschlossen werden, wenn sie eine FR-alpha-Expression >50% hatten.6 In der Studie wurden alle drei Wochen 6mg/kg MIRV appliziert in Kombination mit Bevacizumab (15mg/kg). In die Studie wurden insgesamt 56 Patientinnen eingeschlossen mit einer mittleren Anzahl an Behandlungslinien von 2 (Range 1–4). Die wichtigsten Nebenwirkungen waren Diarrhö, Sehstörungen, Nausea und Fatigue. Die Gesamtansprechrate (ORR) lag bei 43% (95% CI: 31–57). Bei Patientinnen, deren Tumoren eine Expressionsrate des FLR über 50% hatten, lag die ORR bei 60%. Die präsentierten Daten für PFS und OS waren noch unreif und werden an den nächsten Kongressen präsentiert. Der Ansatz erscheint vielversprechend, wenn der FLR erhöht exprimiert ist. Zur weiteren Prüfung sind grössere Phase-II/III-Studien erforderlich.
Auf dem Gebiet der Immuntherapie sind die Erfolge beim Ovarialkarzinom bisher eher bescheiden, obgleich schon länger bekannt ist, dass eine Infiltration von TILs beim Ovarialkarzinom die Prognose verbessert. Für die Monotherapie mit Pembrolizumab (Keynote-100-Studie) wurden am diesjährigen ASCO-Kongress finale Outcome-Daten und Biomarker-Daten vorgestellt.7 Die Studie bestand aus zwei Kohorten. Kohorte A erhielt höchstens 2 Vorbehandlungen und Kohorte B erhielt maximal 5 Linien Therapie. Gesamthaft wurden 376 Patientinnen eingeschlossen (Kohorte A: 285 Patientinnen, Kohorte B: 91). Die Gesamtansprechrate lag bei 8,1% (A) und 9,9% (B) und zeigte auch abhängig vom CombinedPositivityScore (CPS) keinen signifikanten Unterschied. Die grösste Ansprechrate mit einer ORR von 21% gab es bei den klarzelligen Ovarialkarzinomen. Die Immuntherapie scheint nur bei sehr wenigen Patientinnen mit Ovarialkarzinom zu funktionieren und es fehlt weiterhin ein starker prädiktiver Marker, der die Patientinnen identifiziert, bei denen eine Therapie von Nutzen sein könnte.
Neuigkeiten bei anderen gynäkologischen Tumoren
Bei den Trophoblasttumoren (GTD) gab es in den letzten Jahren wenige Neuerungen. Die Standardtherapie besteht aus einer Chemotherapie mit Methotrexat (MTX) oder Actinomycin D und beim Rezidiv aus der Kombination von EMA-CO (Etoposid, MTX, Actinomycin D, Cyclophosphamid, Vincristin). Das Management bei resistenter Erkrankung ist schwierig und es bestehen nur wenige Optionen, dies bei einer jungen Patientinnenkohorte im fertilen Alter und mit weiterhin bestehendem Kinderwunsch. Dies ist von grossem Interesse, da diese junge Patientinnengruppe anderenfalls eine Langzeit-Toxizität durch die Poly-Chemotherapie zu 33% erleiden muss, die es zu vermeiden gilt. Eine französische Arbeitsgruppe hat nun erstmalig Daten zum Immuncheckpoint-Inhibitor Avelumab präsentiert.8 In der TROPHIMMUN-Studie wurden 15 Patientinnen eingeschlossen, die unter einer initialen Mono-Chemotherapie mit MTX oder Actinomycin D resistent wurden. Im Median erhielten die Patientinnen danach 8 Gaben Avelumab 10mg/kg q2w (Range 2–11). Die Behandlung wurde gut toleriert. Die häufigsten Nebenwirkungen waren Fatigue, Nausea, Emesis, Infusionsreaktionen, Schilddrüsenreaktionen, Augentrockenheit und Diarrhö. Das mittlere Follow-up lag bei 30 Monaten, der primäre Endpunkt war eine Normalisierung des hCG-Wertes. Insgesamt hatten 8 Patientinnen (53%, 9 Zyklen im Median) den Endpunkt der Studie erreicht und wurden unter dieser Therapie geheilt. Die Behandlung mit Avelumab stellt daher eine neue, gut verträgliche Behandlungsoption für Patientinnen mit dieser seltenen Tumorerkrankung dar, aber es bedarf weiterer Evidenz in einer grösseren Studie.
Literatur:
1 Du Bois A et al.: ASCO 2020; Abstr. #6000 2 Zang R et al.: ASCO 2020; Abstr. #6001 3 Coleman RL et al.: N Engl J Med 2019; 381(20): 1929-39 4 Poveda A et al.: ASCO 2020; Abstr. #6002 5 Liu JF A et al.: ASCO 2020; Abstr. #6003 6Gilbert L et al.: ASCO 2020; Abstr. #6004 7 Matulonis UA et al.: ASCO 2020; Abstr. #6005 8 You B et al.: ASCO 2020; Abstr. #LBA6008 9 Harter P et al.: Ann Surg Oncol 2006; 13(12): 1702-10 10 Harter P et al.: Int J Gynecol Cancer 2011; 21(2): 289-95 11 MacKay Helen: Gynecologic Cancer. Präsentiert am ASCO 2020 12 Poveda A et al.: ASCO 2020; Abstr. #6002 13 Liu JF et al.: Lancet Oncol 2014; 15(11):1207-14 14 Liu JF et al.: Ann Oncol 2019; 30(4): 551-7 15 Mirza MR et al.: Lancet Oncol 2019; 20(10): 1409-19
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...


