Primäre Thromboembolieprophylaxe bei Hodentumorpatienten
Autorin:
Priv.-Doz. Dr. Angelika Terbuch
Klinische Abteilung für Onkologie
Medizinische Universität Graz
E-Mail: angelika.terbuch@medunigraz.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Eine primäre Thromboembolieprophylaxe bei Krebspatient:innen sollte nach Nutzen- und Risikoabschätzung erfolgen. Hilfreich dafür können Risiko-Scores sein.
Keypoints
-
Bei Hodentumorpatienten soll für die Dauer der cisplatinhaltigen Chemotherapie eine primäre Thromboembolieprophylaxe erfolgen.
-
Auf eine Verwendung von zentralvenösen Kathetern sollte aufgrund des erhöhten Thromboembolierisikos wenn möglich verzichtet werden.
Etwa 20% aller venösen Thromboembolien (VTE) treten bei Krebspatient:innen auf.1 Das Auftreten einer VTE ist mit einem erhöhten Risiko für ein Thromboserezidiv und einem verkürzten Gesamtüberleben verbunden.2 Eine VTE kann zur Hospitalisierung von Patient:innen führen und eine Verzögerung in der krebsspezifischen Therapie verursachen.2 Daher empfehlen Leitlinien bei hospitalisierten Krebspatient:innen eine Thromboembolieprophylaxe.3
Im ambulanten Bereich kann eine Thromboembolieprophylaxe für Krebspatient:innen in Abhängigkeit von Risikofaktoren empfohlen werden. Das höchste VTE-Risiko weisen Patient:innen mit Pankreas- und Magenkarzinomen auf, gefolgt von Patient:innen mit Lungen- und Harnblasenkarzinomen sowie solchen mit gynäkologischen und Hodentumoren.
Studien:PROTECHT und SAVE-ONCO
Die Effektivität und Sicherheit einer primären Thromboembolieprophylaxe im abulanten Setting wurden in randomisierten, placebokontrollierten Studien untersucht. In der PROTECHT- und der SAVE-ONCO-Studie führte die primäre Thromboembolieprophylaxe mit Nadroparin und Semuloparin zu einer Reduktion des relativen Risikos von ca. 50% für das Auftreten einer VTE (von 3,9% auf 2% bzw. von 3,4% auf 1,2%), ohne dass die Zahl der Blutungskomplikationen erhöht wurde.4,5 Allerdings war in diesen Studien ohne weitere Stratifizierung der Krebspatient:innen das Inzidenzrisiko für eine VTE gering.
Khorana-Score & Co.
Zur Abschätzung des Risikos für das Auftreten einer VTE eignen sich Modelle wie zum Beispiel der Khorana-Score.6 Es werden Punkte in Abhängigkeit von Tumorart (1 Punkt für Lungenkarzinome, Lymphome, gynäkologische Malignome, Harnblasen- und Hodentumoren; 2 Punkte für Magen- und Pankreaskarzinome), Thrombozytenzahl (1 Punkt bei >350x109/L), Leukozytenzahl (1 Punkt bei >11x109/L), Hämoglobinwert (1 Punkt bei <10g/dl) und Body-Mass-Index (1 Punkt bei BMI ≥35kg/m2) vergeben. Ab einem Khorana-Score ≥2 soll eine Thromboembolieprophylaxe erwogen werden.
In Folgestudien mit direkten oralen Antikoagulanzien zur Thromboembolieprophylaxe wurden nur Krebspatient:innen mit einem Khorana-Score ≥2 eingeschlossen. So wurden in der randomisierten Phase-III-Studie AVERT 563 Krebspatient:innen mit intermediärem bis hohem Thromboserisiko (Khorana-Score ≥2) eingeschlossen und mit Apixaban oder Placebo behandelt.7 Im Apixaban-Arm zeigte sich eine signifikant geringere Rate an VTE im Vergleich zu Placebo (4,2% vs. 10,2%; HR: 0,41; p<0,001.7 Allerdings ergab sich für die mit Apixaban behandelten Patient:innen ein erhöhtes Risiko für Blutungskomplikationen (3,5% vs. 1,8%; HR: 2,0; p=0,046).7
Im Fokus: Hodentumoren
Patienten mit Hodentumoren waren in all den Studien unterrepräsentiert. Beispielsweise wurden in der PROTECHT-Studie keine Hodentumorpatienten eingeschlossen. In der AVERT-Studie fanden sich unter den eingeschlossenen Krebspatienten drei Patienten mit Hodentumoren.
Um das VTE-Risiko für Hodentumorpatienten besser abschätzen zu können, führten wir deshalb an der Onkologie der Medizinischen Universität Graz eine retrospektive Datenerhebung aller im Zeitraum von 2000 bis 2013 behandelten Hodentumorpatienten durch.8 In der Folge wurden 657 Patienten in die Kohortenstudie eingeschlossen.
Das allgemeine Inzidenzrisiko für eine VTE betrug 5,2%. Das häufigste erhobene Ereignis war eine Lungenembolie (59% aller Ereignisse), gefolgt von einer isolierten tiefen Beinvenenthrombose (23%) oder einer Kombination aus beiden Ereignissen (15%) und viszeralen Thromboembolien (3%). 65% der Ereignisse waren von Symptomen begleitet, während 35% der VTE Zufallsbefunde waren.
Hauptrisikofaktoren
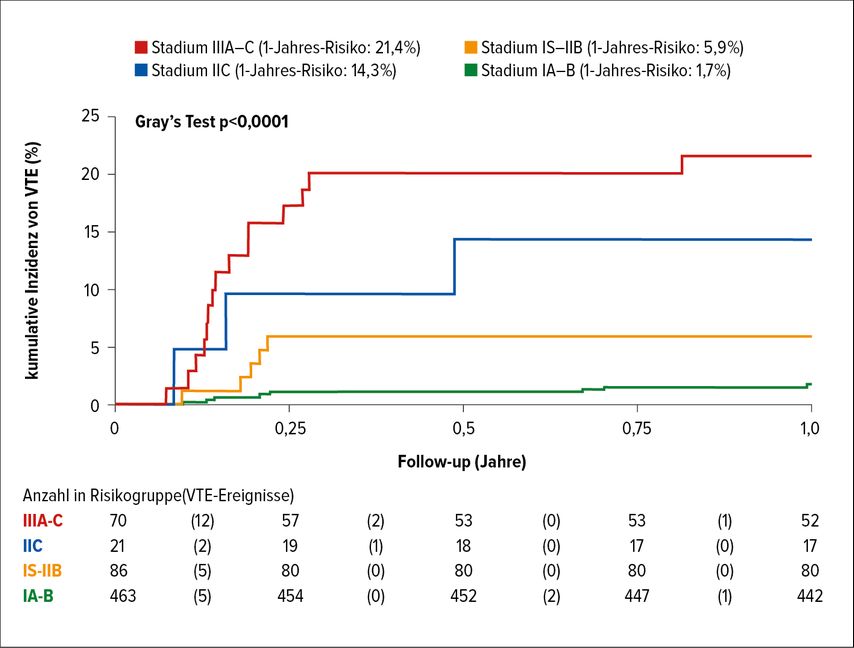
Als Hauptrisikofaktoren für das Auftreten einer VTE konnten ein fortgeschrittenes Tumorstadium sowie das Vorliegen einer retroperitonealen Lymphadenopathie identifiziert werden. Das so erstellte Risikomodell mit vier Kategorien ergab ein 12-Monate-Risiko für das Auftreten einer VTE von 1,7% für die Tumorstadien IA–IB, von 5,9% für die Stadien IS–IIB, von 14,3% für das Stadium IIC und von 21,4% für das Stadium III (Abb. 1).8
Abb. 1: 12-Monats-Inzidenz von venösen Thromboembolien bei Hodentumorpatienten unter Behandlung mit einer cisplatinhaltigen Chemotherapie © Angelika Terbuch, 2016
Dieses Risikomodell wurde in einer Schweizer Kohorte validiert und zeigte für Hodentumorpatienten eine bessere Einschätzung des Risikos für das Auftreten einer VTE als der Khorana- und Srikanthan-Score.8,9 Die venösen thromboembolischen Ereignisse traten fast ausschließlich während des Zeitraums der Chemotherapie auf.
Gezielte Prophylaxe
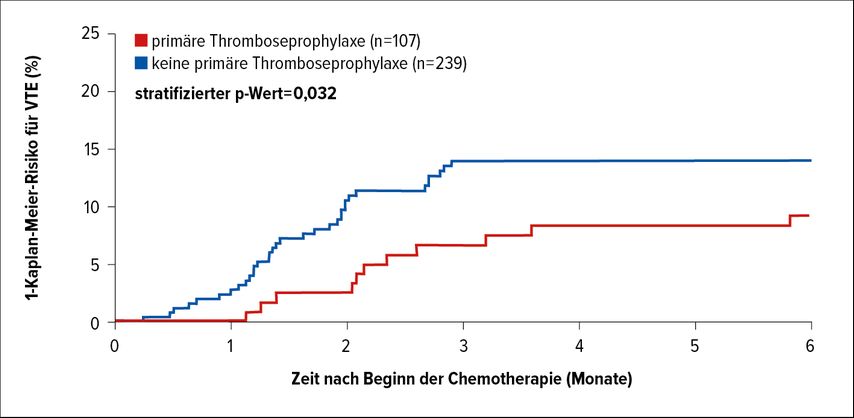
In den Folgejahren führten wir eine konsequente Thromboembolieprophylaxe bei Hodentumorpatienten unter Cisplatin-haltiger Therapie durch und konnten ermitteln, dass eine primäre Thromboembolieprophylaxe zu einer Reduktion des relativen Risikos für das Auftreten einer VTE von 52% führt (Abb. 2).10 Dies zeigte sich auch im Stadium I unter adjuvanter Chemotherapie, weshalb auch hier eine Thromboembolieprophylaxe in Abhängigkeit vom Nutzen-Risiko-Profil zu erwägen ist.
Abb. 2: Primäre Thromboembolieprophylaxe und das Risiko für das Auftreten einer venösen Thromboembolie bei Hodentumorpatienten unter Behandlung mit einer cisplatinhaltigen Chemotherapie. © Angelika Terbuch, 2022
In der aktuellen deutschen S3-Leitlinie zur Behandlung von Hodentumorpatienten wird eine Thromboembolieprophylaxe mit niedermolekularem Heparin zur Senkung des Risikos für VTE bei metastasierten Hodentumorpatienten empfohlen.
Weiters sollte in der Behandlung von Hodentumorpatienten eine Verwendung von zentralvenösen Kathetern wenn möglich vermieden werden, da auch dies zu einer Erhöhung der Zahl an thromboembolischen Komplikationen führen kann, wie in einer multizentrischen retrospektiven Datenerhebung gezeigt werden konnte.11 Diese Empfehlung wurde auch von der Europäischen Gesellschaft für Urologie ausgesprochen und in deren Leitlinien festgehalten (EAU Guidelines).
Literatur:
1 Falanga A, Russo L: Epidemiology, risk and outcomes of venous thromboembolism in cancer. Hamostaseologie 2012; 32: 115-25 2 Khorana AA et al.: Cancer-associated venous thromboembolism. Nat Rev Dis Primers 2022; 8: 11 3 Lyman GH et al.: American Society of Hematology 2021 guidelines for management of venous thromboembolism: prevention and treatment in patients with cancer. Blood Adv 2021; 5: 927-74 4 Agnelli G et al.: Nadroparin for the prevention of thromboembolic events in ambulatory patients with metastatic or locally advanced solid cancer receiving chemotherapy: a randomised, placebo-controlled, double-blind study. Lancet Oncol 2009; 10: 943-9 5 Agnelli G et al.: Semuloparin for thromboprophylaxis in patients receiving chemotherapy for cancer. N Engl J Med 2012; 366: 601-9 6 Khorana AA et al.: Development and validation of a predictive model for chemotherapy-associated thrombosis. Blood 2008; 111: 4902-7 7 Carrier M et al.: Apixaban to prevent venous thromboembolism in patients with cancer. N Engl J Med 2019; 380: 711-9 8 Bezan A et al.: Risk stratification for venous thromboembolism in patients with testicular germ cell tumors. PLoS One 2017; 12: e0176283 9 Srikanthan A et al.: Large retroperitoneal lymphadenopathy as a predictor of venous thromboembolism in patients with disseminated germ cell tumors treated with chemotherapy. J Clin Oncol 2015; 33: 582-7 10 Terbuch A et al.: Primary thromboprophylaxis and the risk of venous thromboembolic events in patients with testicular germ cell tumors treated with cisplatinum-based chemotherapy. Clin Genitourin Cancer 2023; 21: 24-31 11 Fankhauser CD et al.: A risk-benefit analysis of prophylactic anticoagulation for patients with metastatic germ cell tumours undergoing first-line chemotherapy. Eur Urol Focus 2021; 7: 1130-6
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...