Therapie einer vielschichtigen Entität
Autorin:
Dr. med. Ilaria Colombo
Istituto Oncologico della Svizzera Italiana
Bellinzona
E-Mail: ilaria.colombo@eoc.ch
Das Management von Patient:innen mit Endometriumkarzinom hat sich durch die Definition molekularer Subtypen und die Etablierung der Immuncheckpoint-Inhibitoren grundlegend verändert. Zahlreiche Studien evaluieren neue Therapieoptionen und potenzielle Biomarker.
Das Endometriumkarzinom (EC) umfasst vier molekulare Subtypen mit prognostischer und prädiktiver Wertigkeit, die für die Auswahl der adjuvanten Therapie Relevanz besitzen: POLE-mutiert, Mismatch-Repair-defizient (dMMR), p53-mutiert und NSMP («non-specific molecular profile»).1 In der PORTEC-3-Studie entwickelten Patient:innen mit POLE-Mutationen unabhängig von der adjuvanten Behandlung keine Rezidive, während jene mit p53-mutiertem EC zwar die schlechteste Prognose aufwiesen, jedoch von einer adjuvanten Chemotherapie profitierten.2 dMMR und NSMP waren mit einer intermediären Prognose und minimalem Benefit von einer adjuvanten systemischen Therapie assoziiert.
Aktuell wurde der Östrogenrezeptor(ER)-Status in die molekulare Klassifikation laut ESGO-ESTRO-ESP-Leitlinien integriert und dadurch die Risikostratifikation weiter verfeinert.3 Innerhalb der NSMP-Subgruppe ist die Prognose der ER-negativen Patient:innen ungünstig, während bei ER-Positivität eine deutlich höhere Überlebenswahrscheinlichkeit besteht.4
Immuntherapie bei frühem und fortgeschrittenem EC
Immuncheckpoint-Inhibitoren (ICIs) werden derzeit im adjuvanten Setting evaluiert. Die KEYNOTE-B21-Studie prüfte Pembrolizumab zusätzlich zur adjuvanten Chemotherapie bei Hochrisikopatient:innen nach kurativer Operation. Im Vergleich zu Placebo plus Chemotherapie verlängerte die Kombination das krankheitsfreie Überleben in der Gesamtpopulation nicht, wenngleich die Subgruppenanalyse eine signifikante Verbesserung bei Patient:innen mit dMMR (HR: 0,31) zeigte.5 Die RAINBO-Studie testet derzeit mit dem Ziel der Personalisierung auch bei früher Erkrankung adjuvante Therapien, die auf das molekulare Profil zugeschnitten sind.
Beim fortgeschrittenen EC ist Carboplatin/Paclitaxel plus ICI mit oder ohne PARP-Inhibition mittlerweile die Standard-Erstlinientherapie – basierend auf den vier randomisierten Phase-III-Studien RUBY (Dostarlimab), NRG-GY018 (Pembrolizumab), AtTEnd (Atezolizumab) und DUO-E (Durvalumab + Olaparib). In diesen Studien zeigten die Subgruppen mit dMMR/hoher Mikrosatelliteninstabilität vergleichbare klinisch relevante und anhaltende Verlängerungen des progressionsfreien Überlebens (PFS).6–9 Dagegen war der PFS-Benefit in allen Populationen mit profizienter Mismatch-Reparatur (pMMR)/Mikrosatellitenstabilität deutlich geringer. Ähnliche Ergebnisse wurden in RUBY hinsichtlich des Gesamtüberlebens evident; auch hier erfuhren die Subgruppen mit dMMR grössere Vorteile als jene mit pMMR.10,11
Thematik der Selektion geeigneter Patient:innen
Angesichts dieser Erkenntnisse stellt sich die wichtige Frage, ob dMMR-Patient:innen überhaupt eine Chemotherapie benötigen. Derzeit vergleichen die Studien KEYNOTE-C93 und DOMENICA ICIs mit Chemotherapie, um in diesem Bereich Daten zu liefern. Hingegen wird es bei pMMR von grösster Bedeutung sein, Biomarker für die Selektion jener Patient:innen zu identifizieren, die von ICIs profitieren.
Die Zugabe von PARP-Inhibitoren zur ICI-Erhaltungstherapie in der Erstlinie kann die Outcomes bei pMMR verbessern, wie die dreiarmige DUO-E-Studie gezeigt hat, die eine Erhaltungstherapie mit Durvalumab mit oder ohne Olaparib prüfte.9 Hier waren TP53- und HRR(homologe Rekombinationsreparatur)-Mutationen für den klinischen Nutzen der Kombination prädiktiv.12
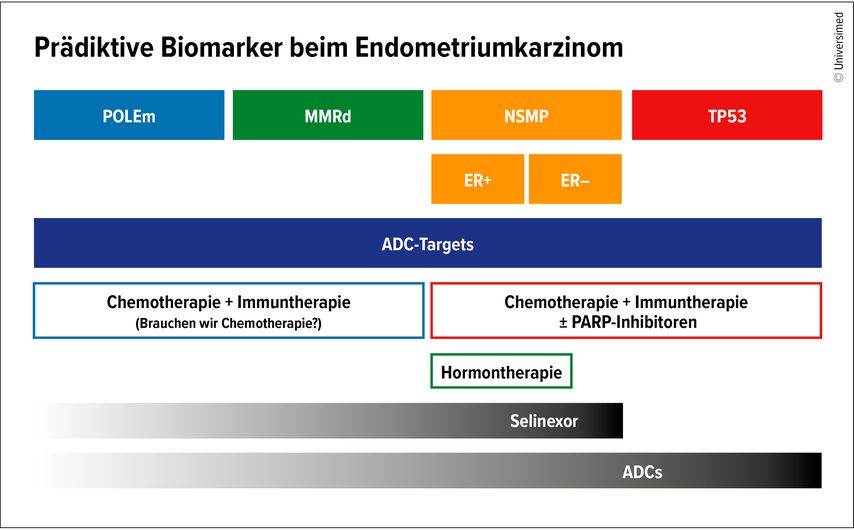
Somit besteht die Standardtherapie bei dMMR aus Chemotherapie plus ICIs (Abb. 1). Chemotherapie plus ICIs wird auch bei NSMP und TP53-Mutationen eingesetzt, wobei PARP-Inhibitoren zusätzlich eine Rolle spielen. Darüber hinaus sollten wir die endokrine Therapie bei ER-positiven Patient:innen nicht vergessen. Weitere Optionen, die derzeit untersucht werden, sind der XPO1-Inhibitor Selinexor sowie Antikörper-Wirkstoff-Konjugate (ADCs), deren Targets über alle Subtypen hinweg exprimiert werden.
Abb. 1: Prädiktive Biomarker und die jeweils zugeordneten Therapien (modifiziert nach van Gorp T, 2024)5
Neue Substanzen
Verschiedene ADCs, die unter anderem gegen HER2, FRα, TROP2 und B7-H4 gerichtet sind, werden derzeit bei Patient:innen mit EC getestet. In der DESTINY-PanTumor02-Studie zeigte Trastuzumab Deruxtecan vielversprechende Ergebnisse beim vorbehandelten EC; in der Gruppe mit hoher HER2-Expression betrug die Gesamtansprechrate (ORR) 84,6%.13 Die TROP2-gerichteten ADCs Sacituzumab Govitecan, Sacituzumab Tirumotecan und Datopotamab Deruxtecan legten eine ähnliche Aktivität mit ORRs von 22–32% an den Tag.14–16 Aktuell stehen die Ergebnisse von Phase-III-Studien noch aus.
Der XPO1-Inhibitor Selinexor bedingte als Erhaltungstherapie nach platinbasierter Erstlinien-Chemotherapie eine Verlängerung des PFS gegenüber Placebo, was vor allem auf die TP53-Wildtyp-Population zutraf (HR: 0,407), während in der Gruppe mit TP53-Mutationen kein Benefit festgestellt wurde.17 Patient:innen mit pMMR-/TP53-Wildtyp-Tumoren erfuhren einen anhaltenden PFS-Vorteil.18 Die Phase-III-Studie XPORT-EC-042 untersucht derzeit Selinexor beim fortgeschrittenen EC mit TP53-Wildtyp nach platinbasierter Chemotherapie. Darüber hinaus sind andere Regime wie Zellzyklus-Checkpoint-Inhibitoren und Kombinationen aus CDK4/6-Inhibitoren mit endokriner Therapie Gegenstand der Forschung. Die Ergebnisse zahlreicher Phase-III-Studien werden die Behandlungslandschaft in Zukunft weiter verändern.
Literatur:
1 Oaknin A et al.: Endometrial cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol 2022; 33(9): 860-77 2 León-Castillo A et al.: Molecular classification of the PORTEC-3 trial for high-risk endometrial cancer: impact on prognosis and benefit from adjuvant therapy. J Clin Oncol 2022; 38(29): 3388-97 3 Concin N et al.: ESGO-ESTRO-ESP guidelines for the management of patients with endometrial carcinoma: update 2025. Lancet Oncol 2025; 26(8): e423-35 4 Vermij L et al.: Prognostic refinement of NSMP high-risk endometrial cancers using oestrogen receptor immunohistochemistry. Br J Cancer 2023; 128(7): 1360-8 5 Van Gorp T et al.: ENGOT-en11/GOG-3053/KEYNOTE-B21: a randomised, double-blind, phase III study of pembrolizumab or placebo plus adjuvant chemotherapy with or without radiotherapy in patients with newly diagnosed, high-risk endometrial cancer. Ann Oncol 2024; 35(11): 968-80 6 Mirza NR et al.: Dostarlimab for primary advanced or recurrent endometrial cancer. Engl J Med 2023; 388(23): 2145-58 7 Eskander RN et al.: Pembrolizumab plus chemotherapy in advanced endometrial cancer. N Engl J Med 2023; 388 (23): 2159-70 8 Colombo N et al.: Phase III double-blind randomized placebo controlled trial of atezolizumab in combination with carboplatin and paclitaxel in women with advanced/recurrent endometrial carcinoma. Ann Oncol 2023; 34(Suppl. 2): 1281-2 9 Westin SN et al.: Durvalumab plus carboplatin/paclitaxel followed by maintenance durvalumab with or without olaparib as first-line treatment for advanced endometrial cancer: the phase III DUO-E trial. J Clin Oncol 2024; 42(3): 283-99 10 Powell MA et al.: Overall survival in patients with endometrial cancer treated with dostarlimab plus carboplatin–paclitaxel in the randomized ENGOT-EN6/GOG-3031/RUBY trial. Ann Oncol 2024; 35(8): 728-38 11 Barretina Ginesta MP et al.: Final overall survival results from the randomized double-blind phase III AtTEnd/ENGOT-EN7 trial evaluating atezolizumab in combination with paclitaxel and carboplatin in women with advanced/recurrent endometrial cancer. Ann Oncol 2023; 36(Suppl. 2): S1698 12 Moore K et al.: Durvalumab plus carboplatin/paclitaxel followed by durvalumab with/without olaparib in endometrial cancer: biomarkers, histological heterogeneity, baseline circulating tumor DNA, and efficacy in the DUO-E mismatch repair proficient subpopulation. Gynecol Oncol 2025; 200(Suppl. 1): 345-6 13 Meric-Bernstam F et al.: Efficacy and safety of tastuzumab deruxtecan in patients with HER2-expressing solid tumors: primary results from the DESTINY-PanTumor02 phase II Trial. J Clin Oncol 2024; 42(1): 47-58 14 Santin AD et al.: Efficacy and safety of sacituzumab govitecan in patients with advanced solid tumors (TROPiCS-03): analysis in patients with advanced endometrial cancer. J Clin Oncol 2024; 42(29): 3421-9 15 Wang K et al.: Sacituzumab tirumotecan monotherapy in advanced/metastatic endometrial carcinoma (EC): results from a phase I/II study (MK-2870-001/KL264-01). Ann Oncol 2025; 36(Suppl. 2): 739-40 16 Oaknin A et al.: Datopotamab deruxtecan in patients with endometrial or ovarian cancer: Results from the phase II TROPION-PanTumor03 study. Ann Oncol 2024; 35(Suppl. 2): 547-8 17 Vergote I et al.: Oral selinexor as maintenance therapy after first-line chemotherapy for advanced or recurrent endometrial cancer. J Clin Oncol 2023; 41(35): 5400-10 18 Valabrega G et al.: Longer-term safety and efficacy of selinexor maintenance therapy for patients with TP53wt advanced or recurrent endometrial cancer: follow-up subgroup analysis of the ENGOT-EN5/GOG-3055/SIENDO study. Int J Gynecol Cancer 2025; 35(Suppl. 1): 100081
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...