«Real-World Data» zum Prostatakarzinom
Autoren:
PD Dr. med. Ursula Vogl
Dr. Fabio Turco
Istituto Oncologico della Svizzera Italiana (IOSI)
Bellinzona
E-Mail: ursula.vogl@eoc.ch
Änderungen der Leitlinien in der Onkologie erfolgen auf Basis der Daten von großen randomisierten Phase-III-Studien. Dies stellt sicher, dass Therapieempfehlungen auf einer hohen Evidenz basieren. Jedoch reflektieren die Patienten, die in diese Studien eingeschlossen werden, nicht immer die Realität. Patienten in unserer Sprechstunde entsprechen sehr oft nicht den Einschlusskriterien und es gibt auch Subgruppen, die aufgrund ihrer Fallzahl nicht Ziel von großen Studien sind. Dieser Artikel beleuchtet diese Aspekte und schildert Ergebnisse aus randomisierten Landmark-Trials sowie Real-World-Studien.
Keypoints
-
Randomisierte Studien sichern eine hohe Datenqualität und Evidenz, jedoch reflektieren die eingeschlossenen Patienten nicht immer den klinischen Alltag.
-
Die Ein-und Ausschlusskriterien sind oftmals sehr streng, um möglichst grosse Sicherheit zu bieten. In der Realität sind wir jedoch mit Patienten mit eingeschränkter Organfunktion und Komorbiditäten konfrontiert, die nicht dem erlaubten Patientenkollektiv der Zulassungsstudien entsprechen.
-
Die Therapie mit 177 Lutetium-PSMA-617 wird schon angewandt und stellt eine weitere Therapieoption für mCRPC-Patienten nach Versagen einer Linie mit einem «novel hormonal agent» und einer Taxan-basierten Therapie dar.
-
Real-World-Studien, die in der Praxis Anwendung finden könnten, waren vor allem Studien zu «treatment patterns» beim mCRPC, welche 2021 vor dem ESMO Meeting publiziert wurden.
-
Kollaborationen zwischen großen Zentren mit einer hohen Anzahl an Prostatakarzinompatienten sind wichtig, um Patientenregister mit hoher Qualität zu kreieren, um «Real-World-Data» abseits von randomisierten Studien attraktiv zu machen. Nur so können diese Daten auch einen Einfluss auf Leitlinien haben.
Nutzen und Datenqualität von Real-World-Studien
«Real-World Data» (RWD) werden immer wieder herangezogen, um Therapiezulassungen zu unterstützen und die Daten der jeweiligen Zulassungsstudien zu untermauern. Jedoch gibt es immer wieder Kritik an der Qualität dieser Daten. Etwa ein Drittel aller Real-World-Studien wird auf dem Gebiet des Prostatakarzinoms durchgeführt, wie eine Analyse von Boyle und Kollegen von über 200 RWD-Studien zeigen konnte,2 etwa ein Viertel davon warvon Pharmaunternehmen gesponsert.
Die große Spanne an berichteten Outcome-Daten im Vergleich zu den randomisierten Zulassungsstudien zeigt, dass die Qualität der Studien mitunter gering ist und dass hier Vorsicht bei der Interpretation dieser Real World-Ergebnisse geboten ist.
Der Vorteil von Daten aus «Cancer Registries» sind die hohe Fallzahl und das einheitliche Setting des jeweiligen Landes oder der Region. Aber nur wenige Länder oder Regionen verfügen über ein solches Netzwerk und dahingehend müssen dringend mehr Kollaborationen in Europa aufgebaut werden. Ein Projekt mit US-Zentren ist «PROMISE: a real-world clinical-genomic database»,3 für Patienten mit metastasiertem hormonsensitiven (mHSPC) bzw. kastrationsresistenten (mCRPC) Prostatakarzinom, bei denen eine somatische oder Keimbahn-Testung durchgeführt wurde. Konzept und Protokoll wurden dieses Jahr publiziert.
Ein wesentlicher Vorteil solch großer Register ist darüber hinaus, dass Patienten über mehrere Therapielinien verfolgt werden und nicht nur ein «Snapshot» einer Linie gemacht wird, wie zumeist in randomisierten Studien.
In der Schweiz nehmen wir an der IRONMAN-Studie (NCT03151629) teil, einer prospektiven Observationsstudie, die die Motivation der onkologischen Verschreiber beim mHSPC, beim nicht metastasierten CRPC und beim mCRPC in verschiedenen Regionen der Welt aufzeichnet.4 Sie inkludiert akademische und nichtakademische Zentren und hat auch einen Fokus auf Lebensqualität mit der Erhebung von «patient-reported outcome measurements» (PROMs). Auch eine translationaler Ansatz mit Blutabnahme zu Beginn und bei jedem Wechsel einer Therapielinie ist Teil des Protokolls. Es ist geplant, dass über 5000 Patienten eingeschlossen werden.
Mein Highlight vor ESMO 2021 als Landmark Studie beim mCRPC: Die Phase-III-Studie VISION
Die PSMA-PET-CT Bildgebung mit 66Ga-PSMA oder 18F-PSMA ist heutzutage in der Schweiz weitreichend verfügbar und wurde dementsprechend in den Therapiealgorithmus gemäß den Stadien der Erkrankung, in denen eine Zulassung besteht, eingebaut: lokalisiertes Hochrisiko-Prostatakarzinom und biochemisches Rezidiv nach definitiver kurativer Lokaltherapie. Eine zusätzliche Indikation, wenngleich noch keine Zulassung besteht, ist die Durchführung zur Evaluierung einer Tauglichkeit für eine Radionuklidtherapie mit 177Lu-PSMA.
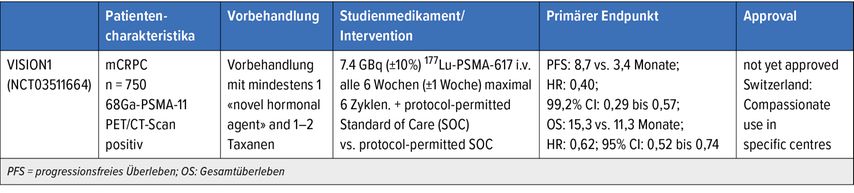
Mit der positiven Studie VISION wird sehr bald eine weitere Therapieoption für das mCRPC bei vorbehandelten Patienten zur Verfügung stehen.1 Diese vor dem diesjährigen Jahreskongress der European Society of Medical Oncology (ESMO) durchgeführte Studie war meine persönliche Landmark randomisierte Phase-III-Studie mit 177Lutetium-PSMA-617. Die Studie schloss 831 mCRPC-Patienten mit PSMA-PET-positiven Läsionen ein, die mit mindestens einem «novel hormonal agent» und einer Linie einer Taxan-basierten Chemotherapie vorbehandelt waren. Die Patienten wurden randomisiert, entweder 6 Zyklen mit 177Lu-PSMA-617 als sechswöchentlicher Infusion mit einem im Protokoll erlaubten Standard of Care (SOC) zu erhalten oder nur den SOC (zumeist bestehend aus Glukokortikosteroiden oder einem zweiten «novel hormonal agent», da Cabazitaxel oder Radium-223 nicht erlaubt waren).
Die Studie hat ihren primären Endpunkt Gesamtüberleben (OS) erreicht, mit einem medianen OS von 15,3 Monaten versus 11,3 Monate (HR: 0,62, 95%CI: 0,52–0,74; p<0,001). Höhergradige unerwünschte Wirkungen (>Grad 3) wurden bei 52,7% der Patienten berichtet, zumeist Thrombopenie und Anämie (Tab. 1). Insgesamt waren die Nebenwirkungen aber gut handhabbar und die Lebensqualität wurde nicht beeinflusst.5
In der Schweiz wird in einigen Zentren mit spezialisierter Nuklearmedizin diese Therapie schon seit Längerem im Rahmen eines «Compassionate Use»-Programmes angeboten, so auch in unserem Zentrum in Bellinzona. Derzeit besteht noch keine Zulassung in der Schweiz, die FDA hat eine «Breakthrough Designation for Approval» gleich nach der Präsentation beim Jahreskongress der American Society for Clinical Oncology (ASCO) 2021 gestellt.
Real-World-Studien 2021
Eine australische Gruppe publizierte die Outcome-Daten von 74 Patienten, die an einem Zentrum zwischen 2014 und 2019 Abirateron/Prednison oder Enzalutamid im Setting mCRPC erhielten.6 Der primäre Endpunkt dieser retrospektiven Single-Center-Analyse war ein PSA-Ansprechen >50%. Die Autoren beschreiben, dass das PSA-Ansprechen in der Gruppe der mit Enzalutamid behandelten Patienten höher war im Vergleich zur Abirateron/Prednison-Gruppe. Jedoch dürfte dies vor allem an der nicht ausbalancierten Tumorlast liegen, denn in der Abirateron-Gruppe waren mehr Patienten mit hoher Tumorlast vertreten. Auch waren mehr von ihnen mit Docetaxel vorbehandelt.
Das OS war deutlich länger in der Enzalutamid-Gruppe mit 30 Monaten gegenüber 11 Monaten bei Abirateron/Prednison. Diese Resultate weichen sehr stark von den Zulassungsstudien der beiden Substanzen ab und zeigen, dass die Qualität von RWD immer sehr zu hinterfragen ist.7–10
Ähnliche Ergebnisse berichtete eine retrospektive türkische Studie mit 250 Patienten im gleichen Setting, die zwischen 2012 und 2020 durchgeführt wurde. Allerdings war das Patientenkollektiv sehr heterogen, mit oder ohne Docetaxel in der Vorbehandlung.11 Auch hier zeigte Enzalutamid eine höhere Anzahl an PSA-Abfällen sowie ein längeres progressionsfreies Überleben (PFS) und OS. Die Autoren schreiben jedoch auch hier, dass die Tumorlast der Abirateron/Prednison-Patienten höher war.
Eine weitere Publikation beschrieb die Art der mCRPC-Therapien in einer Datenbank von über 5000 US-Patienten zwischen 2013 und 2019.12 In dieser Zeit erhielt ein hoher Anteil der Patienten eine Therapiesequenz mit zwei aufeinanderfolgenden «novel hormonal agents», wenige andere auch mit einer Zwischenlinie mit einer Taxan-basierten Therapie. Aufgrund von bekannten Kreuzresistenzen zwischen verschiedenen Vertretern der «novel hormonal agents» ist der sequenzielle Gebrauch in den Guidelines nicht empfohlen.
Patienten in dieser retrospektiven Analyse wurden zum Grossteil in «Community-based» Praxen behandelt, was nicht die akademische Behandlungswelt widerspiegelt. Das mediane Überleben in der Erstlinie wurde mit 19 Monaten berichtet, deutlich kürzer als in den Zulassungsstudien von Enzalutamid und Abirateron/Prednison bei Docetaxel-naiven Patienten, in denen es bei etwa 35 Monaten lag.
Die Autoren diskutierten auch, dass damals das Wissen um die Relevanz von BRCA1/2-Mutationen fehlte und eine somatische bzw. Keimbahn-BRCA1/2-Testung nicht möglich war, sodass einige Patienten aus dieser Studie heute Zugang zu PARP-Inhibitoren oder auch 177Lutetium-PSMA gehabt hätten.
Ebenso berichtete eine schwedische Gruppe von über 2000 mCRPC-Patienten und den Real-World-Behandlungsstrategien in den Jahren 2006 bis 2016.13 Hierbei erhielt nur ein Drittel der Patienten überhaupt eine Erstlinientherapie innerhalb der ersten 12 Monaten nach Auftreten eines mCRPC. Dieser Prozentsatz steigerte sich aber am Ende des Beobachtungszeitraumes der retrospektiven Studie.
Ein beim ASCO 2021 präsentierter Abstract beschreibt einen Zusammenhang einer PSA-Progression unter Enzalutamid oder Abirateron/Prednison in mCRPC in Woche 4 nach Behandlungsbeginn mit einer raschen Progression und einem kürzerem OS und somit einer eventuell bestehenden Resistenz auf das jeweils eingesetzte Medikament.14
Die Informationen aus diesen Real-Life-Studien werden die Behandlung des mCRPC nicht beeinflussen, Abirateron/Prednison und Enzalutamid haben den gleichen Stellenwert und Empfehlungsgrad in den Guidelines im Setting des mCRPC.
Zusammenfassung
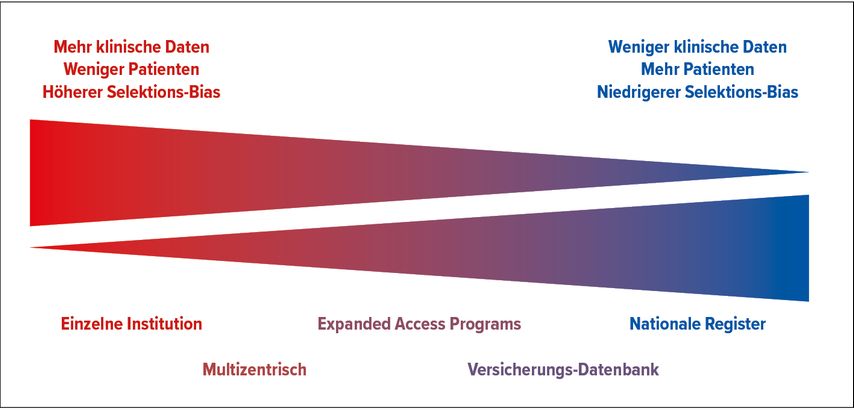
Prospektive, randomisierte Studien bleiben der Goldstandard für Leitlinien, Zulassungen und die klinische Anwendung. Eine Landmark-Studie im Jahr 2021 beim mCRPC war die Phase-III-Studie VISION mit 177Lutetium-PSMA.1 Diese Therapie kommt im klinischen Alltag nun zur Anwendung, sollte jedoch nur Patienten angeboten werden, die den Einschlusskriterien dieser Studie entsprechen, d.h. Patienten mit PSMA-PET-positiven Läsionen und einer Vorbehandlung mit einem «novel hormonal agent» und einer Taxan-basierten Chemotherapie. Diese Studie wählte ich in meiner Präsentation beim diesjährigen ESMO-Kongress als randomisierte Landmark-Studie aus. Diese Studien sichern die Effizienz der Therapien mit den entsprechenden spezifizierten Endpunkten (Abb. 1).
Abb. 1: Darstellung der Datenqualität von Real-World-Studien je nach Art der Datenbank (modifiziert nach Zer A et al.)16
Real-Life-Studien, zumeist Observationsstudien, können aber die Anwendung im klinischen Alltag beschreiben. Nur wenige Patienten bekommen ihre Therapie im Rahmen eines Studienprotokolls, circa 8%, wie aus den USA berichtet.15 Es ist von absoluter Notwendigkeit, bei der Erstellung von Registern und Datenbanken auf ein gut konzipiertes Protokoll zu achten. Die daraus kreierten RWD sind wiederum Hypothesen-generierend und bringen neuen Input für randomisierte Studien.
Literatur:
1 Sartor O et al.: Lutetium-177-PSMA-617 for metastatic castration-resistant prostate cancer. N Engl J Med 2021; 385: 1091-103 2 Boyle JM et al.: Real-world outcomes associated with new cancer medicines approved by the Food and Drug Administration and European Medicines Agency: A retrospective cohort study. Eur J Cancer 2021; 155: 136-44 3 Koshkin VS et al.: PROMISE: a real-world clinical-genomic database to address knowledge gaps in prostate cancer. Prostate Cancer Prostatic Dis 2021; online ahead of print 4 McKay RR et al.: Tackling diversity in prostate cancer clinical trials: a report from the diversity working group of the IRONMAN registry. JCO Glob Oncol 2021; 7: 495-505 5 Fizazi KH et al.: Health-related quality of life (HRQoL), pain and safety outcomes in the phase III VISION study of 177Lu-PSMA-617 in patients with metastatic castration-resistant prostate cancer. Ann Oncol 2021; 32 (suppl_5): S626-77 6 Raju R et al.: Real-World Data on outcomes in metastatic castrate-resistant prostate cancer patients treated with abiraterone or enzalutamide: a regional experience. Front Oncol 2021; 11: 656146 7 Ryan CJ et al.: Abiraterone in metastatic prostate cancer without previous chemotherapy. N Engl J Med 2013; 368: 138-48 8 Beer TM et al.: Enzalutamide in metastatic prostate cancer before chemotherapy. N Engl J Med 2014; 371: 424-33 9 de Bono JS et al.: Abiraterone and increased survival in metastatic prostate cancer. N Engl J Med 2011; 364: 1995-2005 10 Scher HI et al.: Increased survival with enzalutamide in prostate cancer after chemotherapy. N Engl J Med 2012; 367: 1187-97 11 Demirci A et al.: Comparison of real-life data of abiraterone acetate and enzalutamide in metastatic castration-resistant prostate cancer. Scientific Reports 2021; 11(1): 14131 12 Shore ND et al.: Real-world treatment patterns and overall survival of patients with metastatic castration-resistant prostate cancer in the US prior to PARP-Inhibitors. Adv Ther 2021; 38: 4520-40 13 Vigneswaran HT et al.: Real-world treatment utilization patterns in patients with castration-resistant prostate cancer. Scand J Urol 2021; 55(4): 299-306 14 López-Campos F et al.: Evaluation of PSA progression after initiation of enzalutamide or abiraterone: Real-world data on metastatic castration-resistant prostate cancer (mCRPC). JClin Oncol 2021; 39 no. 15_suppl: 5024 15 Unger JM et al.: Systematic review and meta-analysis of the magnitude of structural, clinical, and physician and patient barriers to cancer clinical trial participation. J Natl Cancer Inst 2019; 111: 245-55 16 Zer et al.: Landmark real-life studies published in 2021: Potential impact on clinical practice and guidelines - Update in Lung Cancer. ESMO 2021
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...