Prostatakarzinom: Die Highlights
Beim diesjährigen Jahrestreffen der American Society of Clinical Oncology (ASCO) in Chicago wurden mehrere wichtige Studien zum Prostatakarzinom vorgestellt, welche thematisch in zwei Gruppen eingeteilt werden können. Beim metastasierten hormonsensitiven Prostatakarzinom wurden Updates der ENZAMET-Studie und eine neue Phase-III-Studie mit dem Androgenrezeptor-Antagonisten SHR3680 vorgestellt. Drei andere Präsentationen bezogen sich auf die fortgeschrittene kastrationsresistente Situation und den Einsatz von 177Lutetium-PSMA(prostataspezifisches Membranantigen).
Metastasiertes hormonsensitives Prostatakarzinom
Die ENZAMET-Studie: Follow-up
In der ENZAMET-Studie wurden 1125 Patienten mit metastasiertem hormonsensitivem Prostatakarzinom randomisiert zu:
-
Androgendeprivation (ADT) plus einen nichtsteroidalen Androgenrezeptor-Antagonisten (Bicalutamid, Nilutamid, Flutamid) und optional Docetaxel (6 Zyklen)
ADT plus Enzalutamid und optional Docetaxel (6 Zyklen)1
Bereits 2019 wurde der primäre Endpunkt Gesamtüberleben berichtet und prominent publiziert.
Im Update 2022 zeigte sich das Gesamtüberleben auch mit längerem Follow-up bei der Kombination aus ADT und Enzalutamid weiterhin eindeutig verlängert (nicht erreicht vs. 73,2 Monate, HR: 0,7, 95% KI: 0,58–0,84). Vor allem das mittlere Überleben im Kontrollarm ist mit mehr als 73 Monaten (6,1 Jahre) eindrücklich.2 Hier ist jedoch zu betonen, dass die ENZAMET-Studie eine gemischte Patientenpopulation eingeschlossen hat (39% synchron und «high volume», 22% synchron und «low volume», 15% metachron und «high volume» und 25% metachron und «low volume»). Der Vorteil der zusätzlichen Therapie mit Enzalutamid zeigt sich in allen Subgruppen.
Bedeutsam ist die ENZAMET-Studie vor allem aber auch, weil insgesamt 45% der eingeschlossenen Patienten Docetaxel erhalten haben. Allerdings war der Einsatz der Chemotherapie den Untersuchern freigestellt und es muss davon ausgegangen werden, dass gewisse Selektionskriterien eine Rolle spielten, die im Rahmen der Studie nicht kontrolliert wurden.
Ein möglicher Vorteil für den Einsatz einer Tripeltherapie (ADT plus Enzalutamid plus Docetaxel) zeigt sich am ehesten bei Patienten mit synchroner «High volume»-Erkrankung. Aber auch diese Daten sind mit Vorsicht zu interpretieren und dementsprechend vorsichtig im Alltag umzusetzen, da sie sich mit Subgruppen befassen. Ausserdem war die Tripeltherapie im Vergleich zu ADT und Enzalutamid mit relevant mehr Nebenwirkungen verbunden.
SHR3680 und weitere Therapieoptionen
Eine weitere interessante Studie aus China untersuchte den neuen Androgenrezeptor-Antagonisten SHR3680 bei Patienten mit synchronem metastasiertem hormonsensitivem «High volume»-Prostatakarzinom in Kombination mit ADT verglichen mit ADT plus Bicalutamid.3 Die Kombination aus ADT plus SHR3680 zeigte gegenüber ADT plus Bicalutamid im radiografisch progressionsfreien Überleben (rPFS, HR: 0,44, 95% KI: 0,33–0,58), aber auch im Gesamtüberleben (HR: 0,58, 95% KI: 0,44–0,77) einen signifikanten Vorteil. Die Therapie mit SHR3680 scheint gut verträglich zu sein und zeigt nur eine geringe Häufigkeit an Nebenwirkungen vom Schweregrad 3 oder höher.
Da SHR3680 somit für die Onkologie ein interessantes Molekül ist, wird es gerade in einer weiteren grossen Phase-III-Studie (NCT05009290) bei Patienten mit lokalisiertem beziehungsweise lokal fortgeschrittenem Prostatakarzinom sechs Monate vor und sechs Monate nach radikaler Prostatektomie untersucht.
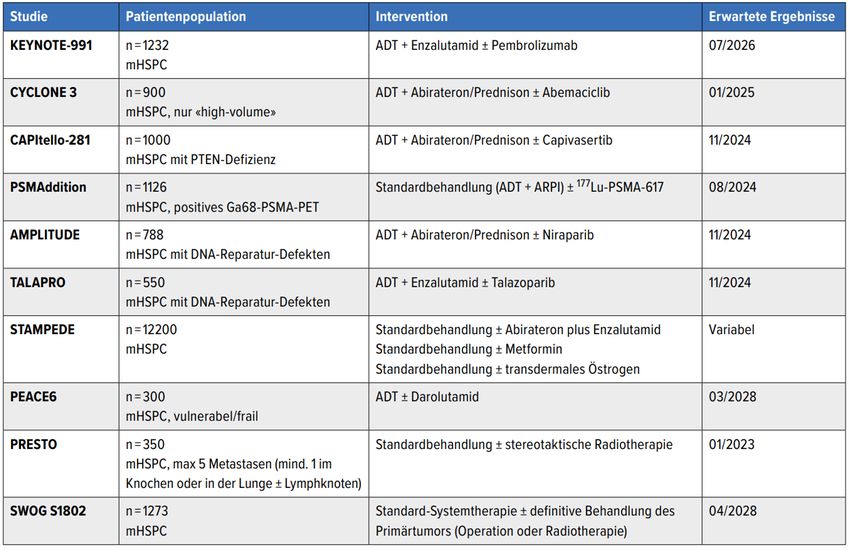
Eine ganze Reihe weiterer Phase-III-Studien befasst sich mit dem Stellenwert der Immuntherapie, zielgerichteter Therapien beziehungsweise der Lokalbehandlung des Primärtumors und der Metastasen-gerichteten Therapie bei Patienten mit metastasiertem hormonsensitivem Prostatakarzinom (Tab. 1).
Fazit für die Praxis:
-
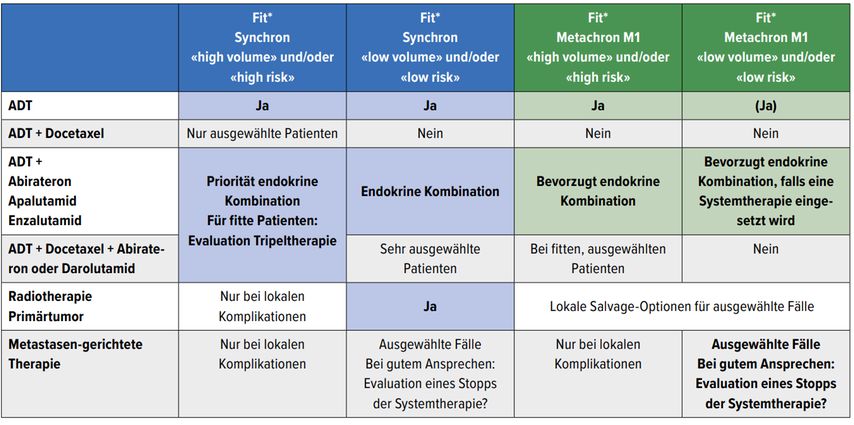
In der Behandlung von Patienten mit metastasiertem hormonsensitivem Prostatakarzinom können anhand des zeitlichen Auftretens von Metastasen (synchron vs. metachron) und anhand der Ausdehnung der Erkrankung («low volume» vs. «high volume») prognostisch wichtige Gruppen unterschieden werden, siehe auch Tabelle 2.
-
Für die Tripeltherapie (ADT plus Docetaxel plus zusätzliche endokrine Therapie) besteht die beste Evidenz bei Patienten mit synchroner «High volume»-Erkrankung.
Der Einsatz von Docetaxel alleine in Kombination mit ADT ist in den Hintergrund gerückt. Besser verträglich und besser untersucht sind die zusätzlichen endokrinen Therapien, vor allem in der metachron metastasierten Situation bzw. auch in der «Low volume»-Situation.
Einsatz vonLutetium177-PSMA beim kastrationsresistenten Prostatakarzinom
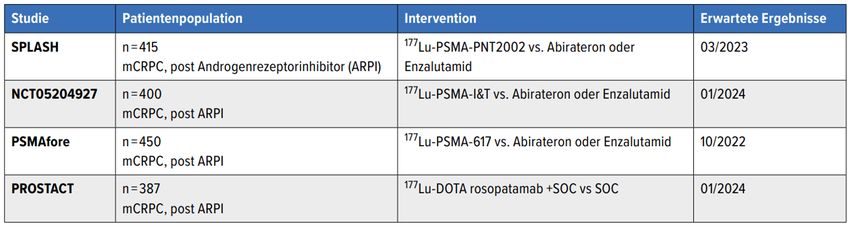
Nachdem 2021 die VISION-Studie für 177Lu-PSMA-617 in Kombination mit einer Standardbehandlung (endokrine Therapie, Steroide, Osteoprotektion) gegenüber einer Standardbehandlung alleine einen signifikanten Vorteil im radiografisch progressionsfreien Überleben aber auch im Gesamtüberleben zeigen hatte können, wurden beim ASCO-Jahrestreffen 2022 zwei weitere interessante Analysen aus der VISION-Studie präsentiert.4 Eine Übersicht über Studien zu 177Lu-PSMA bietet Tabelle3.
177Lu-PSMA-617: Vorbehandlung und Begleitung
In der Präsentation von Dr. Vaishampayan wurden einerseits die Therapien in den Fokus genommen, die Patienten vor Einschluss in die VISION-Studie erhalten hatten, und andererseits die konkomitierenden Medikamente, die Patienten mit oder ohne 177Lu-PSMA-617 erhielten.5
Nicht überraschend zeigt sich ein leicht längeres Gesamtüberleben für Patienten, welche nur eine Taxan-Vorbehandlung erhalten haben (Gesamtüberleben im 177Lu-PSMA-617-Arm: 16,2 Monate [1 Taxan] vs. 13,6 Monate [2 Taxane]). Bei den endokrinen Therapien wurde kein Unterschied dahingehend festgestellt, ob Patienten vor Studieneinschluss eine oder zwei Therapielinien erhalten hatten (Gesamtüberleben im 177Lu-PSMA-617-Arm: je 15,3 Monate).
Indirekt unterstützen diese Daten die Beobachtung, dass die sequenzielle Antitumor-Aktivität von endokrinen Therapien gering ist, dass aber Taxane eine relevante Antitumor-Aktivität haben. Eine interessante Beobachtung ergab sich bei der Analyse der Standardbehandlung in Kombination mit 177Lu-PSMA-617: Das Gesamtüberleben unter 177Lu-PSMA-617 plus endokrine Therapie lag bei 17,8 Monaten verglichen mit 12,4 Monaten unter 177Lu-PSMA-617 ohne zusätzliche endokrine Therapie.
Die Resultate sind mit Vorsicht zu interpretieren, da nicht gezeigt wurde, welche Vortherapien diese Patienten erhalten hatten (möglicherweise wurde eine zusätzliche endokrine Therapie dann eingesetzt, wenn Patienten erst eine Linie erhalten hatten). Verschiedene Arbeiten haben aber gezeigt, dass die PSMA-Expression durch endokrine Therapien hochreguliert wird. Es könnte sein, dass damit 177Lu-PSMA-617 eine bessere Wirkung entfalten kann.6
Der mittlere Ganzkörper-SUV-Wert
In einer zweiten Arbeit aus der VISION-Studie zeigte Dr. Armstrong Daten zur PSMA-Expression in der 68Ga-PSMA-11-Positronenemissions-Tomografie (PET) und zur Korrelation mit dem radiografisch progressionsfreien Überleben und dem Gesamtüberleben.7 Für diese Analysen wurde ein mittlerer Ganzkörper-SUV(«Standardized Uptake Value»)-Wert verwendet, der rechnerisch aus den Bilddaten generiert werden kann. Patienten in der Quartile mit dem höchsten mittleren Ganzkörper-SUV profitierten deutlich mehr von 177Lu-PSMA-617 als Patienten in der Quartile mit dem geringsten mittleren SUV (rPFS: 14,1 vs. 5,6 Monate, OS: 21,4 vs. 14,5 Monate).
Ähnliche Resultate waren beim ASCO-Jahrestreffen 2022 zum Urogenitaltrakt auch für die TheraP-Studie gezeigt worden. Der mittlere Ganzkörper-SUV-Wert kann im Moment nicht routinemässig bei der PSMA-PET/Computertomografie(CT)-Diagnostik angegeben werden, wird aber hoffentlich in naher Zukunft in die Berichte integriert werden.
Tab. 2: Therapieoptionen für mHSPC (* Empfehlungen gelten grundsätzlich für fitte Patienten. Bei Patienten ≥75 Jahre sollte vor einer Therapieempfehlung ein geriatrisches Screening (z.B. mit G8 und mini-COG) durchgeführt werden
Fazit für die Praxis:
-
Für Patienten mit kastrationsresistentem Prostatakarzinom und PSMA-positiven Metastasen steht die Therapie mit 177Lu-PSMA-617 als neue Standard-Option ab der dritten Therapielinie zur Verfügung (nach einer neuen endokrinen Therapie und einer Linie Taxan-Behandlung).
-
Für die 177Lu-PSMA-617-Therapie ist eine vorgängige PSMA-PET-Bildgebung notwendig. Hierbei ist zu beachten, dass in den Studien zu 68Ga-PSMA-11 meist eine PET/CT verwendet wurde, in der Schweiz wird aber überwiegend ein anderer PET-Tracer verwendet (18F-PSMA-1007), dessen Bioverfügbarkeit sich von der der PET/CT unterscheidet. In der VISION-Studie wurden ca. 13% der Patienten basierend auf der PSMA-PET-Diagnostik ausgeschlossen, in der TheraP-Studie fast 28% der Patienten. Eine strengere Selektion basierend auf der Baseline-PSMA-PET scheint mit besseren Ergebnissen assoziiert zu sein, da das Ansprechen auf die Therapie mit 177Lu-PSMA mit der PSMA-Expression korreliert. Möglicherweise ist eine zusätzliche endokrine Therapie, wie sie in der VISION-Studie erlaubt war, für gewisse Patienten von Vorteil.
-
Der mittlere Ganzkörper-SUV-Wert könnte sich in Zukunft als neuer Biomarker etablieren.
-
Eine gute Patientenselektion ist dann wichtig, wenn die Therapie zunehmend früher (z.B. bei Chemotherapie-naiven) Patienten eingesetzt wird und wenn alternative, etablierte Standard-Therapieoptionen noch zur Verfügung stehen.
Die Ergebnisse zweier grosser Phase-III-Studien sind im Moment offen (auch in der Schweiz): die der PSMAfore-Studie (für Chemotherapie-naive Patienten) und die der PSMAddition-Studie (für Patienten in der metastasierten hormonsensitiven Situation).
Erneut sind viele Fragen aufgeworfen worden. Auf Updates bei zukünftigen Konferenzen darf man gespannt sein. An der Advanced Prostate Cancer Consensus Conference 2021 und 2022 (APCCC 2021 und 2022, www.apccc.org ) wurden viele dieser Fragen mit dem Experten-Panel diskutiert. Die Resultate von 2021 sind inzwischen auch veröffentlicht worden,8 die der Konferenz 2022 werden in Kürze publiziert.
Literatur:
1 Davis ID et al.: ENZAMET trial investigators and the Australian and New Zealand urogenital and prostate cancer trials group. Enzalutamide with standard first-line therapy in metastatic prostate cancer. N Engl J Med 2019; 381(2): 121-31 2 Davis ID et al.: Updated overall survival outcomes in ENZAMET (ANZUP 1304), an international, cooperative group trial of enzalutamide in metastatic hormone-sensitive prostate cancer (mHSPC). J Clin Oncol 2022; 40(suppl. 17): Abstr. #LBA5004 3 Ye DW et al.: A phase 3 trial of SHR3680 versus bicalutamide in combination with androgen deprivation therapy (ADT) in patients with high-volume metastatic hormone-sensitive prostate cancer (mHSPC). J Clin Oncol 2022; 40(suppl. 16): Abstr. #5005 4 Sartor O et al.: VISION investigators. Lutetium-177-PSMA-617 for metastatic castration-resistant prostate cancer. N Engl J Med 2021; 385(12): 1091-103 5 Vaishampayan N et al.: [177Lu]Lu-PSMA-617 in PSMA-positive metastatic castration-resistant prostate cancer: Prior and concomitant treatment subgroup analyses of the VISION trial. J Clin Oncol 2022; 40 (suppl. 16): Abstr. #5001 6 Hadaschik S et al.: Influence of androgen deprivation therapy on PSMA expression and PSMA-ligand PET imaging of prostate cancer patients. Eur J Nucl Med Mol Imaging 2020; 47: 9-15 7 Kuo P et al.: [68Ga]Ga-PSMA-11 PET baseline imaging as a prognostic tool for clinical outcomes to [177Lu]Lu-PSMA-617 in patients with mCRPC: A VISION substudy. J Clin Oncol 2022; 40(suppl. 16): Abstr. #5002 8 Gillessen S et al.: Management of patients with advanced prostate cancer: report from the advanced prostate cancer consensus conference 2021. Eur Urol 2022; 82(1): 115-41
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...