Praxisverändernde Studien in der Onkologie
Bericht:
Mag. pharm. Irene Senn, PhD
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Im Rahmen der OeGHO-Frühjahrstagung in Salzburg präsentierte Priv.-Doz. Dr. Thomas Winder (LKH Feldkirch) seine persönlichen Studienhighlights, die den klinischen Alltag in der Onkologie maßgeblich beeinflussen werden. Die vorgestellten Ergebnisse könnten die Therapiestandards bei verschiedenen soliden Tumorentitäten in naher Zukunft verändern.
Magenkarzinom: Reevaluation der Radiochemotherapie und neue zielgerichtete Ansätze
Die kürzlich aktualisierten ESMO-Guidelines zum Magenkarzinom definieren die perioperative Chemotherapie (CTx) mit dem FLOT-Schema (vier Zyklen präoperativ, vier Zyklen postoperativ) als Standard für lokal fortgeschrittene Magenkarzinome. Die Rolle der Radiochemotherapie (RCT), die in ausgewählten Fällen empfohlen wurde, wird nun aufgrund neuer Studiendaten infrage gestellt.
Die ESOPEC-Studie verglich das CROSS-Protokoll (RCT) mit dem FLOT-Schema (CTx) und fand keinen signifikanten Unterschied hinsichtlich des Gesamtüberlebens (OS) und des progressionsfreien Überlebens (PFS).1 Auch die TOPGEAR-Studie konnte keinen Benefit durch das Hinzufügen einer RCT zur perioperativen CTx nachweisen – selbst bei fortgeschrittenen Tumoren (T3/T4) mit Lymphknotenbefall.2,3 „Derzeit hat die Radiochemotherapie also nur für gewisse Subgruppen einen Benefit, ausgenommen natürlich das Plattenzellkarzinom des Ösophagus“, resümierte Priv.-Doz. Dr. Winder.
Für die postoperative Therapie lieferte die SPACE-FLOT-Studie wertvolle Erkenntnisse aus Real-World-Daten.4 Die Ergebnisse zeigten, dass Patient:innen mit minimalem Ansprechen oder komplettem Ansprechen (CR) keinen wesentlichen Benefit von der adjuvanten Therapie hatten, während Patient:innen mit partiellem Ansprechen (PR) davon profitierten. „Dies ist ein wichtiges Signal für den klinischen Alltag, wenn wir diskutieren, ob die Therapie frühzeitig beendet werden kann“, so Winder.
Auch bei der zielgerichteten Therapie des Magenkarzinoms präsentierte Winder zwei bedeutende Fortschritte: Die Studie KEYNOTE-811 untersuchte das Hinzufügen von Pembrolizumab zur Standardtherapie mit Trastuzumab plus CTx beim HER2-positiven, fortgeschrittenen Magenkarzinom. Die Analyse zeigte, dass Patient:innen mit einem PD-L1 „combined positive score“ (CPS) ≥1 einen signifikanten Überlebensvorteil durch die Hinzunahme von Pembrolizumab hatten (mOS: 20,1 vs. 15,7 Monate), während Patient:innen mit CPS <1 keinen Vorteil zeigten.5,6
Für Claudin-18.2-positive Tumoren (≥75% IHC 2+/3+) zeigte die kombinierte Auswertung der Ergebnisse aus den Studien SPOTLIGHT und GLOW einen signifikanten Gesamtüberlebensvorteil durch das Hinzufügen von Zolbetuximab zur CTx (mOS: 16,4 vs. 13,7 Monate; HR für Tod: 0,77; 95% CI: 0,67–0,89).7
Kolorektales Karzinom: von Aspirin bis Immuntherapie
Der Einsatz von Aspirin zur Rezidivprävention beim kolorektalen Karzinom (CRC) wird seit Langem diskutiert.8 Die randomisierte ALASCCA-Studie liefert nun spannende Evidenz: Bei Patient:innen mit CRC im Stadium I–III (n=1823) und molekularen Alterationen in PIK3CA/PTEN (37% der Kohorte) reduzierte Aspirin 160mg täglich über drei Jahre die Rezidivrate signifikant um etwa 50%.9 „Dies ist die erste randomisierte Studie, die einen signifikanten Nutzen von Aspirin bei dieser Patient:innengruppe zeigt, und sie wird unseren klinischen Alltag voraussichtlich verändern“, so Winder.
Bei lokal fortgeschrittenen Mikrosatelliten-instabilen (MSI-high) CRC wurden in der NICHE-2-Studie beeindruckende Ergebnisse mit einer neoadjuvanten Immuntherapie (ein Zyklus Ipilimumab+Nivolumab, gefolgt von einem weiteren Nivolumab-Zyklus) erzielt.10 Die Rate des pathologischen Ansprechens lag bei 98%, mit einer Major-Response-Rate (≤10% lebensfähiger Resttumor) von 95% und einer kompletten pathologischen Remission bei 68% der Patient:innen.
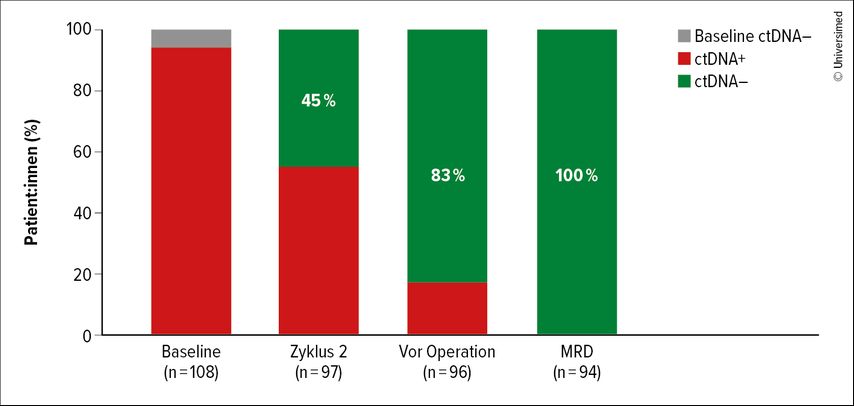
„Besonders bemerkenswert waren die Daten zur zirkulierenden Tumor-DNA (ctDNA): Vor der chirurgischen Intervention waren 83% der Patient:innen ctDNA-negativ, nach der Operation sogar 100%“, führte Winder aus. Das deutet auf eine vollständige Eliminierung der minimalen Resterkrankung hin (MRD; Abb.1). Das krankheitsfreie Überleben über drei Jahre zeigte bisher keine Rezidive in diesem Setting. Winder wies jedoch auch auf die potenziellen Langzeittoxizitäten hin.11
Abb. 1: Verlauf der ctDNA-Negativität in der NICHE-2-Studie (MSI-high Kolonkarzinom, n=108; modifiziert nach Chalabi M et al.)10
Beim metastasierten CRC mit BRAFV600E-Mutation lieferte die BREAKWATER-Studie wichtige Erkenntnisse: Die Kombination aus BRAF-gezielter Therapie, Cetuximab und CTx zeigte ein Ansprechen von 60% vs. 40% mit „standard of care“. Das OS verlängerte sich signifikant (HR: 0,47).12 „Dies deutet darauf hin, dass die zielgerichtete Therapie beim BRAF-mutierten metastasierten kolorektalen Karzinom zunehmend in die Erstlinie rücken wird“, ordnete Winder die Ergebnisse ein.
Für metastasierte MSI-high CRC zeigte die CheckMate-8HW-Studie einen beeindruckenden Vorteil der Kombination aus Nivolumab und Ipilimumab gegenüber der Standard-CTx (HR für PFS: 0,21; 95% CI: 0,13–0,35; p=0,0001). Nach 24 Monaten lag das PFS bei 72% in der Kombinationsgruppe vs. 14% in der CTx-Vergleichsgruppe.13 „Diese Daten untermauern, dass die Kombinationstherapie in diesem Setting zielführend ist“, bewertete Winder dieses Ergebnis.
Analkarzinom: Durchbruch mit Immuntherapie
Beim metastasierten Analkarzinom gab es mit POD1UM-303 (InterAACT 2) erstmals seit Jahren wieder eine praxisverändernde Studie. Sie verglich den PD-1-Inhibitor Retifanlimab in Kombination mit dem bisherigen Therapiestandard Carboplatin/Paclitaxel vs. Carboplatin/Paclitaxel mono. Das Gesamtüberleben verlängerte sich signifikant (HR: 0,70; nach Cross-over-Adjustierung sogar HR: 0,63).14
Melanom Stadium III: neoadjuvante Immuntherapie überlegen
Die NADINA-Studie untersuchte neoadjuvantes Nivolumab plus Ipilimumab vs. adjuvantes Nivolumab beim Melanom im Stadium III. Die neoadjuvante Kombinationstherapie zeigte einen signifikanten Vorteil beim ereignisfreien Überleben (HR: 0,32; 99,9% CI: 0,15–0,66; p<0,001). Das pathologische Ansprechen korrelierte stark mit dem Langzeitüberleben: Patient:innen mit pathologischer Komplettremission (45,8%) oder Near-Komplettremission (10,8%) zeigten ein deutlich längeres rezidivfreies Überleben (>85% nach drei Jahren).15
Urothelkarzinom: perioperative Immuntherapie und neue Erstlinienkombination
„Beim Urothelialkarzinom gab es ebenfalls bahnbrechende Neuigkeiten“, berichtete Winder. Die NIAGARA-Studie untersuchte perioperatives Durvalumab in Kombination mit Gemcitabin/Cisplatin beim muskelinvasiven Harnblasenkarzinom. Das Gesamtüberleben verlängerte sich signifikant (HR: 0,75; 95% CI: 0,59–0,93; p=0,01), wobei die PD-L1-Expression überraschenderweise keinen Einfluss auf den Benefit hatte.16
Eine weitere wichtige Studie war EV-302, die Enfortumab Vedotin plus Pembrolizumab in der Erstlinientherapie des fortgeschrittenen Urothelkarzinoms untersuchte.17 Im Vergleich zur Standard-CTx verlängerte diese Kombination sowohl das PFS (HR: 0,45; 95% CI: 0,38–0,54; p<0,001) als auch das OS (HR: 0,47; 95% CI: 0,38–0,58; p<0,001) signifikant. Das mOS verlängerte sich von 16,1 Monaten auf 31,5 Monate. Diese Ergebnisse könnten zu einem Paradigmenwechsel in der Erstlinientherapie des fortgeschrittenen Urothelkarzinoms führen.
Lungenkarzinome: Konsolidierung und perioperative Konzepte
Die ADRIATIC-Studie untersuchte Durvalumab nach RCT beim kleinzelligen Bronchialkarzinom (SCLC) im Stadium I–III („limited disease“). In dieser randomisierten Phase-III-Studie erhielten Patient:innen nach vorangegangener RCT entweder Durvalumab oder Placebo für zwei Jahre. Das OS verlängerte sich signifikant von 33,4 Monaten auf 55,9 Monate (HR: 0,73; 95% CI: 0,54–0,98; p=0,01).18
Beim nichtkleinzelligen Lungenkarzinom (NSCLC) in den Stadien II–III präsentierte Winder Updates zu drei wichtigen Studien:
-
CheckMate-816: Für neoadjuvantes Nivolumab plus CTx beim operablen NSCLC Stadium II/III liegen nun OS-Daten (sekundärer Endpunkt) vor. Es zeigte sich ein klinisch bedeutsamer Vorteil, wobei das mOS noch nicht erreicht wurde (HR: 0,71; 95% CI: 0,47–1,07; p=0,0451).19
-
CheckMate-77T: Perioperatives Nivolumab (vier Zyklen präoperativ, postoperativ alle vier Wochen für ein Jahr) verlängerte das ereignisfreie Überleben (EFS) signifikant (medianes EFS: 40,1 vs. 17,0 Monate; HR: 0,59; 95% CI: 0,45–0,79).20,21
-
KEYNOTE-671: Perioperatives Pembrolizumab (vier Zyklen präoperativ, 13 Zyklen adjuvant) verlängerte das Gesamtüberleben signifikant (HR: 0,72; 95% CI: 0,56–0,93; p=0,0052).22
Mammakarzinom: OS-Vorteil durch Pembrolizumab und HER2-low
Das Update der Studie KEYNOTE-522 zum tripelnegativen Mammakarzinom (BC) Stadium II–III zeigte einen signifikanten Vorteil im OS durch perioperatives Pembrolizumab in Kombination mit CTx gegenüber CTx mono (HR: 0,66; 95% CI: 0,50–0,87; p=0,00150).23,24 „Etwa 5% der Patient:innen werden durch die Hinzunahme von Pembrolizumab zusätzlich geheilt, während etwa 80% bereits durch die Standard-Chemotherapie und Radiotherapie allein geheilt werden“, erläuterte Winder. „Hier gibt es sicher noch einige Diskussionspunkte wie Deeskalationsstrategien bei Respondern, Eskalation bei Non-Respondern, Toxizität und Kosten.“
Bei metastasiertem, HR-positivem HER2-low- oder -ultra-low-BC zeigte die Studie DESTINY-Breast06 einen signifikanten Vorteil von Trastuzumab Deruxtecan gegenüber CTx (HR für PFS: 0,62; 95% CI: 0,52–0,75; p<0,001).25 „Dieses Ergebnis wird sicher auch unseren klinischen Alltag verändern und es muss diskutiert werden, ob nun alle Patient:innen erneut auf HER2 bestimmt werden müssen“, sagte Winder.
Zusammenfassung und Ausblick
Die PD-1/PD-L1-Inhibition ist in kurativer Intention bei vielen soliden Tumoren zum Standard geworden, wobei der Trend zur neoadjuvanten Gabe geht. Zudem rücken zielgerichtete Therapien zunehmend in frühere Therapielinien. Als Herausforderungen nannte Winder die unterschiedlichen Studienresultate trotz ähnlicher Präparate und die noch unzureichende biomarkerbasierte Patient:innenselektion.
Quelle:
OeGHO- & AHOP-Frühjahrstagung 2025 in Kooperation mit OPG & AAHP, 24.–26. April 2025, Salzburg
Literatur:
1 Hoeppner J et al.: J Clin Oncol 2024; 42(Suppl. 1): Abstr. #LBA1 2 Leong T et al.: Ann Oncol 2024; 35(Suppl. 2): Abstr. #S1249 3 Leong T et al.: N Engl J Med 2024; 391(19): 1810-21 4 Lee M et al.: Ann Oncol 2024; 35(Suppl. 2): S878-912 5 Janjigian YY et al.: Ann Oncol 2023; 34: S851-S2 6 Janjigian YY et al.: Ann Oncol 2024; 35: S877-S8 7Shitara K et al.: N Engl J Med 2024; 391(12): 1159-62 8Liao X et al.: N Engl J Med 2012; 367(17): 1596-606 9Martling A et al.: J Clin Oncol 2025; 43(Suppl. 4): Abstr. #LBA125 10 Chalabi M et al.: Ann Oncol 2024; 35(Suppl 2): S1217-S8 11 Johnson DB et al.: Nat Rev Clin Oncol 2022; 19(4): 254-67 12 Kopetz S et al.: J Clin Oncol 2025; 43(Suppl. 4): 16 13 Andre T et al.: N Engl J Med 2024; 391(21): 2014-26 14 Rao S et al.: Ann Oncol 2024; 35: 1-72 15 Blank CU et al.: N Engl J Med 2024; 391(18): 1696-708 16 Powles T et al.: N Engl J Med 2024; 391(19): 1773-86 17Powles T et al.: N Engl J Med 2024; 390(10): 875-88 18Cheng Y et al.: N Engl J Med 2024; 391(14): 1313-27 19Spicer J et al.: J Clin Oncol 2024; 42(Suppl. 17): Abstr. #LBA8010 20 Cascone T et al.: N Engl J Med 2024; 390(19): 1756-69 21 Provencio Pulla M et al.: Ann Oncol 2024; 35: S1239-S40 22 Spicer JD et al.: Lancet 2024; 404(10459): 1240-52 23 Schmid P et al.: N Engl J Med 2024; 391(21): 1981-91 24Schmid P et al.: Ann Oncol 2024; 35(Suppl. 2): S1204-S5 25 Bardia A et al.: N Engl J Med 2024; 391(22): 2110-22
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...