
Praxisverändernde Fortschritte und richtungsweisende Signale
Bericht:
Dr. Therese Schwender
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Der SOHC-Kongress 2025 verdeutlichte eindrucksvoll, wie unterschiedlich sich der therapeutische Fortschritt in der Onkologie derzeit vollzieht. Entsprechend spannte das Programm der Highlights-of-the-Year-Session den Bogen von unmittelbar relevanten Neuerungen, etwa auf dem Gebiet der Mamma- und Lungenkarzinome, bis zu Konzepten, die vorerst vor allem als Wegweiser für kommende Therapiestrategien zu verstehen sind.
Ein Schwerpunkt der Präsentation von Dr. med. Khalil Zaman, Universitätsspital (CHUV), Lausanne, zum Mammakarzinom lag auf der Weiterentwicklung der endokrinen Therapie (ET) beim hormonrezeptorpositiven (HR+) fortgeschrittenen Brustkrebs. Nach einer langen Phase ohne grössere Innovationen rücken seit einiger Zeit erstmals orale selektive Östrogenrezeptor-Degrader (SERDs) in den Fokus. Substanzen wie Elacestrant, Camizestrant und Imlunestrant zeigten in klinischen Studien, darunter EMERALD, eine mit etablierten endokrinen Therapien vergleichbare Wirksamkeit, vor allem aber eine deutlich höhere Aktivität bei Patient:innen mit ESR1-Mutationen.1
Ein weiterer neuer Vertreter der oralen SERDs ist Giredestrant. Am ESMO 2025 wurden Resultate der Phase-III-Studie evERA BC vorgestellt, die Giredestrant in Kombination mit Everolimus mit einer Standard-ET plus Everolimus bei Patient:innen mit Progress nach ET und CDK4/6-Inhibitor verglich (55% mit ESR1-Mutation).2 Die Kombination aus Giredestrant und Everolimus erwies sich dabei hinsichtlich des progressionsfreien Überlebens (PFS) als überlegen – sowohl in der Subgruppe mit ESR1-Mutation (Hazard-Ratio [HR]: 0,38; 95%- Konfidenzintervall [CI]: 0,27–0,54; p<0,0001) als auch in der «Intention to treat»-Population (HR 0,56; 95% CI: 0,44–0,71; p<0,0001). Zaman wies zudem auf eine kürzlich veröffentlichte Pressemitteilung zu Giredestrant hin, die über positive Resultate im Hinblick auf das krankheitsfreie Überleben (DFS) im adjuvanten Setting berichtete.3 Sollten sich diese Ergebnisse bestätigen, käme dies – so Zaman – einer Revolution gleich, da in der adjuvanten ET seit rund 20 Jahren keine substanzielle Weiterentwicklung mehr erzielt wurde.
Ebenfalls eine wesentliche Rolle spielt die gezielte Hemmung der PI3K-/AKT-/mTOR-Signalkaskade. Besonders diskutiert wurden in diesem Zusammenhang Daten aus der INAVO-120-Studie, in der die Triplet-Kombination aus Fulvestrant, Palbociclib und Inavolisib bei Patientinnen mit PIK3CA-mutierten Tumoren ein signifikantes Wirksamkeitssignal zeigte.4 So konnte neben einer Verlängerung des PFS gegenüber Fulvestrant-Palbociclib-Placebo auch ein signifikanter Vorteil im Gesamtüberleben (OS) beobachtet werden (medianes OS 34,0 vs. 27,0 Monate; HR: 0,67, p=0,02).
Reifere Daten aus monarchE undNATALEE
MonarchE und NATALEE untersuchten die Zugabe eines CDK4/6-Inhibitors (Abemaciclib bzw. Ribociclib) zur ET im adjuvanten Setting. Zu beiden Studien wurden am ESMO aktuelle Updates präsentiert, die eine weiterführende Einordnung der Langzeitwirksamkeit erlauben.
In monarchE zeigte die Kombination aus Abemaciclib plus ET nach einem medianen Follow-up von 76,2 Monaten ein signifikant reduziertes Risiko zu sterben im Vergleich zur alleinigen ET (HR: 0,84; 95%; CI: 0,72–0,98; p=0,027).5 Die 7-Jahres-OS-Rate betrug 86,8% unter Abemaciclib plus ET gegenüber 85,0% unter alleiniger ET, entsprechend einer absoluten Differenz von 1,8%.
Das Update der NATALEE-Studie belegte, dass auch nodal-negative Patient:innen von der adjuvanten Therapie mit Ribociclib profitieren können, mit einer absoluten Verbesserung der Rate des Überlebens frei von invasiver Krankheit (iDFS) um 5,7 Prozentpunkte nach fünf Jahren.6
Endokrine Therapie und Lebensqualität
Als nächsten Punkt erläuterte Zaman die POSITIVE-Studie.7 Sie untersuchte, ob eine Unterbrechung der ET für bis zu zwei Jahre – um den Patient:innen eine Schwangerschaft zu ermöglichen – einen negativen Einfluss auf die Prognose hat. Erste Ergebnisse waren beruhigend und wurden nun durch ein aktuelles Update weiter bestätigt.8 Nach fünf Jahren zeigte sich im Vergleich zur SOFT/TEXT-Kontrollkohorte weder für brustkrebsspezifische Ereignisse noch für Fernrezidive ein relevanter Unterschied. Die kumulative 5-Jahres-Inzidenz betrug 12,3% versus 13,2% für brustkrebsspezifische Ereignisse sowie 6,2% versus 8,3% für Fernrezidive.
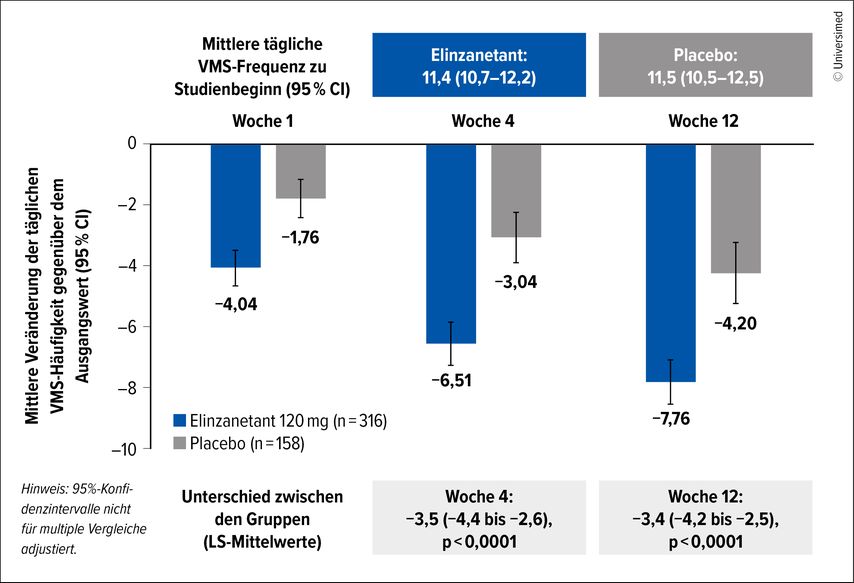
Zudem wurden am ASCO erstmals Ergebnisse der OASIS-4-Studie vorgestellt.9 Sie zeigte, dass der neue duale Neurokinin-1/3-Inhibitor Elinzanetant im Vergleich zu Placebo die Häufigkeit moderater bis schwerer vasomotorischer Symptome unter endokriner Therapie nach 4 und 12 Wochen signifikant reduzierte (Abb.1). Darüber hinaus kam es zu einer numerischen Verbesserung im Schweregrad der Symptome nach 4 und 12 Wochen sowie zu einer signifikanten Zunahme der Schlafqualität und der Menopause-spezifischen Lebensqualität nach 12 Wochen.
Abb. 1: Im Vergleich zu Placebo reduzierte Elinzanetant die Häufigkeit moderater bis schwerer vasomotorischer Symptome unter endokriner Therapie signifikant (modifiziert nach Cardoso F et al.)9
SCLC: verbesserte Prognose durch Erhaltungstherapie
Zu den besonderen Highlights auf dem Gebiet der Lungentumoren gehören ohne Zweifel die therapeutischen Fortschritte beim schwierig zu behandelnden kleinzelligen Lungenkarzinom (SCLC). Dr. med. Laetitia Mauti, Kantonsspital Winterthur, stellte in diesem Zusammenhang die Phase-III-Studie IMforte vor. Diese schloss Patient:innen mit einem SCLC im extensiven Stadium (ES-SCLC) ein und zeigte, dass eine Erhaltungstherapie mit Lurbinectedin und Atezolizumab im Vergleich zu Atezolizumab allein nach Standardinduktion mit platinbasierter Chemotherapie und Atezolizumab zu einer signifikanten Verlängerung des PFS und OS führte (medianes OS plus 2,6 Monate).10
Mauti wies aber auch darauf hin, dass die Erhaltungstherapie mit Lurbinectedin plus Atezolizumab mit einer deutlich höheren Rate an Nebenwirkungen, einschliesslich schwerer Ereignisse, einherging (behandlungsbedingte Nebenwirkungen Grad 3/4: 25,6% vs. 5,8%). Bislang seien zudem keine Daten zur Lebensqualität dieser Patient:innen verfügbar, was sie als wesentlichen Nachteil beurteilte. Zu berücksichtigen ist ausserdem, dass nach Abschluss der Induktionstherapie nur noch rund zwei Drittel der ursprünglich gescreenten Patient:innen in die Erhaltungstherapie eingeschlossen werden konnten. Eine sorgfältige Selektion geeigneter Patient:innen für dieses Behandlungsschema sei daher entscheidend, so Mauti.
DLL3 als neues therapeutisches Zielbeim SCLC
Als «grösstes Highlight beim SCLC» bezeichnete Mauti den Einsatz DLL3-gerichteter T-Zell-Engager. So erzielte mit Tarlatamab erstmals ein bispezifischer T-Zell-Engager (BiTE) bei einem soliden Tumor überzeugende klinische Ergebnisse. Tarlatamab verbindet DLL3 auf Tumorzellen mit CD3 auf zytotoxischen T-Zellen und löst so eine gezielte Immunantwort aus. In der randomisierten Phase-III-Studie DeLLphi-304 erzielte der Antikörper bei Patient:innen mit überwiegend ES-SCLC und Progress während oder nach einer platinbasierten Chemotherapie einen klaren Überlebensvorteil gegenüber der Standardchemotherapie (medianes OS: 13,6 vs. 8,3 Monate, HR: 0,60; p<0,001) (Tab.1).11 Ein Überlebensvorteil zeigte sich konsistent über alle untersuchten Subgruppen hinweg, auch bei platinresistenter Erkrankung (knapp 50% der Teilnehmenden). Zudem bewirkte die Therapie eine signifikante Verbesserung tumorassoziierter Symptome wie Dyspnoe, Husten oder thorakaler Schmerzen.
Tab. 1: Medianes Gesamtüberleben (OS) und progressionsfreies Überleben (PFS) unter Therapie mit dem bispezifischen T-Zell-Engager Tarlatamab bei Patient:innen mit einem kleinzelligen Lungenkarzinom im extensiven Stadium und Progress während oder nach einer platinbasierten Chemotherapie (DeLLphi-303-Studie) (modifiziert nach Wermke M et al.)12
Zum BiTE-spezifischen Nebenwirkungsprofil gehört das Zytokinfreisetzungssyndrom (CRS), das unter Tarlatamab überwiegend niedriggradig verlief und nur selten zu Therapieabbrüchen führte. Häufig wurde zudem eine Dysgeusie beobachtet, die trotz meist geringer Schwere für die Patient:innen sehr belastend sein kann.
Erste Resultate der Phase-Ib-Studie DeLLphi-303 zum Erstlinieneinsatz von Tarlatamab in Kombination mit einer Chemoimmuntherapie beim ES-SCLC zeigten eine bisher unerreichte OS-Rate von 81,1% nach 12 Monaten.12 Mauti äusserte sich daher überzeugt, dass DLL3-gerichtete BiTEs rasch Eingang in frühere Therapielinien finden werden.
Lymphome: starke Signale mit nochbegrenzter Praxisrelevanz
Während beim Lungenkarzinom mehrere unmittelbar praxisrelevante Fortschritte präsentiert wurden, zeigten sich im Bereich der Lymphome vor allem vielversprechende Entwicklungen, deren definitive Einordnung jedoch in Teilen noch aussteht. Wie Dr. med. Fatime Krasniqi, Universitätsspital Basel, berichtete, werden vor allem die Resultate der Phase-III-Studie Skyglo mit Spannung erwartet, da diese für die Erstlinientherapie von Hochrisikopatient:innen mit diffusem grosszelligem B-Zell-Lymphom richtungsweisend sein könnten.
Bereits klinisch überzeugende Daten wurden für die Rezidiv- und Refraktärsituation vorgestellt: So erwies sich die Kombination aus einem BiTE und einem Antikörper-Wirkstoff-Konjugat (Mosunetuzumab und Polatuzumab vedotin) gegenüber Rituximab, Gemcitabin und Oxaliplatin als deutlich überlegen (medianes PFS 11,5 vs. 3,8 Monate; HR: 0,41; p<0,0001), was auf ein relevantes therapeutisches Potenzial dieser Strategie hinweist.13
Auch beim Mantelzelllymphom mit niedrigem Risiko sorgten die Ergebnisse der ENRICH-Studie für Aufmerksamkeit, da sich mit Rituximab plus Ibrutinib erstmals ein chemotherapiefreies Regime gegenüber der Standardimmunchemotherapie R-CHOP durchsetzen konnte.14 Beim follikulären Lymphom wiederum zeigten sich in der Zweitlinientherapie mit Tafasitamab in Kombination mit Rituximab und Lenalidomid (inMIND-Studie) klinisch relevante Verbesserungen, die die künftige Therapiesequenz beeinflussen könnten.15
◾15081207◆
Quelle:
Session «Highlights of the Year». Swiss Oncology & Hematology Congress, 21. November 2025, Basel
Literatur:
1 Bidard FC et al.: Elacestrant (oral selective estrogen receptor degrader) versus standard endocrine therapy for estrogen receptor-positive, human epidermal growth factor receptor 2-negative advanced breast cancer: results from the randomized phase III EMERALD trial. J Clin Oncol 2022; 40(28): 3246-56 2 Mayer E et al.: Giredestrant, an oral selective oestrogen receptor antagonist and degrader, + everolimus in patients with ER-positive, HER2-negative advanced breast cancer previously treated with a CDK4/6 inhibitor: primary results of the phase III evERA BC trial. ESMO 2025; Abstr. #LBA16 3 Genentech Press Release vom 17. November 2025. Verfügbar unter: www.gene.com/media/press-releases/15090/2025-11-17/genentechs-giredestrant-becomes-the-firs , zuletzt aufgerufen: 19. Januar 2026 4 Jhaveri KL et al.: Overall survival with inavolisib in PIK3CA-mutated advanced breast cancer. N Engl J Med 2025; 393(2): 151-61 5 Johnston S et al.: monarchE: primary overall survival results of adjuvant abemaciclib + endocrine therapy for HR+, HER2-, high-risk early breast cancer. ESMO 2025; Abstr. #LBA13 6 Crown J et al.: Adjuvant ribociclib plus nonsteroidal aromatase inhibitor therapy in patients with HR-positive/HER2-negative early breast cancer: 5-year follow-up of NATALEE efficacy outcomes and updated overall survival. ESMO Open 2025; 10: 105858 7 Partridge AH et al.: Interrupting endocrine therapy to attempt pregnancy after breast cancer. NEngl J Med 2023; 388(18): 1645-56 8 Pagani O et al.: 5-year follow-up results from the POSITIVE (Pregnancy Outcome and Safety of Interrupting Therapy for Women with Endocrine Responsive Breast Cancer) trial. ESMO 2025; Abstr. #LBA12 9 Cardoso F et al.: Efficacy and safety of elinzanetant for vasomotor symptoms associated with adjuvant endocrine therapy: phase 3 OASIS 4 trial. JClin Oncol 2025; 43: 508 10 Paz-Ares L et al.: Efficacy and safety of first-line maintenance therapy with lurbinectedin plus atezolizumab in extensive-stage small-cell lung cancer (IMforte): a randomised, multicentre, open-label, phase 3 trial. Lancet 2025; 405(10495): 2129-43 11 Mountzios G et al.: Tarlatamab in small-cell lung cancer after platinum-based chemotherapy. N Engl J Med 2025; 393(4): 349-61 12 Wermke M et al.: Tarlatamab with first-line chemoimmunotherapy for extensive stage small cell lung cancer (ES-SCLC): DeLLphi-303 study. Ann Oncol 2025; 36(Suppl. 2): S1479-501 13 Westin J et al.: Mosunetuzumab plus polatuzumab vedotin is superior to R-GemOx in transplant-ineligible patients with r/r LBCL: primary results of the phase III SUNMO trial. ICML 2025; Abstr. #LBA3 14 Lewis DJ et al.: Ibrutinib and rituximab versus immunochemotherapy in patients with previously untreated mantle cell lymphoma (ENRICH): a randomised, open-label, phase 2/3 superiority trial. Lancet 2025; 406(10514): 1953-68 15 Sehn LH et al.: Outcomes from the phase 3 InMIND study of tafasitamab plus lenalidomide and rituximab for patients with relapsed/refractory follicular lymphoma. ICML 2025; Abstr. #28
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...
%20und%20progressionsfreies%20%C3%9Cberleben%20(PFS).jpg)


