Neues aus der Pathologie
Autorin:
Assoc. Prof. Priv.-Doz. Dr. Zsuzsanna Bagó-Horváth
Klinisches Institut für Pathologie
Medizinische Universität Wien
Für Patholog:innen hatte das 46. San Antonio Breast Cancer Symposium zwei große Themenschwerpunkte zu bieten: Einerseits wurden erste translationelle Studien über einen innovativen, bisher nicht verwendeten prognostischen und prädiktiven Biomarker präsentiert,andererseits wurden mehrere Analysen über den Einsatz künstlicher Intelligenz zur besseren Charakterisierung morphologischer und molekularer Tumoreigenschaften vorgestellt. Ein weiteres Highlight waren die lang erwarteten, prospektiv geplanten translationellen Analysen großer klinischer Studien.
Fresia Pareja, Memorial Sloan Kettering Cancer Center, hat über neue, bisher nicht beschriebene Mechanismen des Verlustes der E-Cadherin-Funktion beim invasiven lobulären Mammakarzinom (ILC) berichtet.
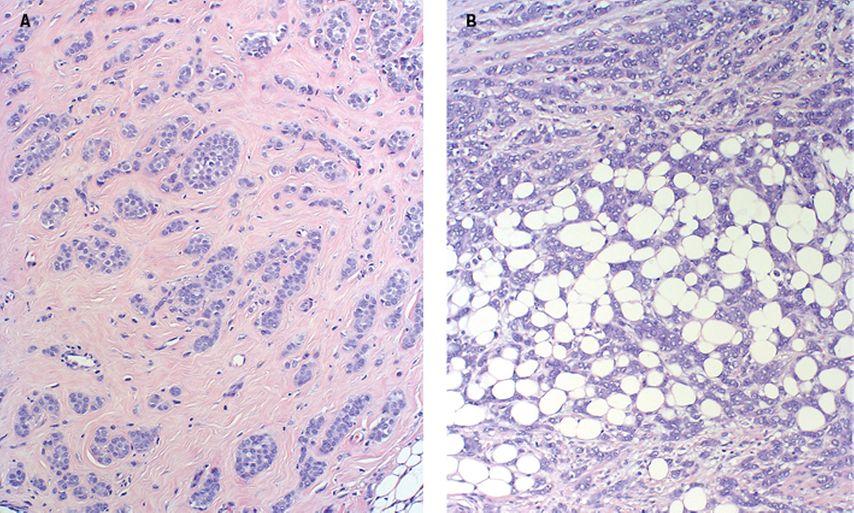
Das lobuläre Mammakarzinom ist der häufigste spezielle Subtyp beim Mammakarzinom, der anhand histomorphologischer Merkmale diagnostiziert wird. Die Tumorzellen zeigen ein charakteristisches, dyskohäsives Wachstumsmuster: Sie liegen einzeln oder in Einzelzellreihen im Stroma und umgeben präexistente Parenchymstrukturen. Diese Eigenschaft basiert auf einem Funktionsverlust des ZelladhäsionsmolekülsE-Cadherin, welches das pathognomonische genomische Korrelat beim ILC darstellt: Das Gen E-Cadherin (CDH1) zeigt eine biallelische Mutation in etwa 80% der Tumoren. Außer einer biallelischen Mutation kann auch eine homozygote Deletion oder die Promotormethylierung zum Funktionsverlust mit ähnlichen morphologischen Merkmalen führen. Allerdings ist die Interobserver-Diskordanz bei dieser morphologischen Diagnostik relativ hoch, weil die morphologischen Kriterien einer breiten Varianz der Ausprägung unterliegen. Wir Patholog:innen sind mit diesen Abweichungen vertraut und ungewöhnliche Ausprägungsformen werden als „special morphological features“ beschrieben (Abb. 1). Dies sind eine ungewöhnlich hochgradige Kernpolymorphie, stark erhöhte Mitosefrequenz, das Auftreten solider Zellgruppen statt Einzellzellen und Lymphgefäßeinbrüche.
Abb. 1: Spezielle morphologische Subtypen beim invasiven lobulären Mammakarzinom A: alveolärer Subtyp, B: pleomorpher Subtyp
Die Autor:innen der Studie haben gezeigt, dass diese Abweichungen mit alternativen E-Cadherin-Inaktivierungsmechanismen assoziiert sind und mithilfe von digitaler Imageanalyse und künstlicher Intelligenz identifiziert werden können. Dazu wurde eine große Kohorte von ILCs genetisch auf das Vorhandensein einer biallelischen E-Cadherin-Mutation analysiert. Anschließend wurden die morphologischen Eigenschaften dieser Fälle in Abhängigkeit vom Mutationstatus mittels eines maschinellen Lernalgorithmus trainiert. Der so entwickelte Algorithmus war daraufhin in der Lage, eine biallelische E-Cadherin-Mutation mit hoher Sensitivität und Spezifität nur aufgrund der Morphologie des HE-Schnittes zu identifizieren. Zusätzlich konnten durch die Analyse der „falsch positiven“ Fälle alternative molekulare Mechanismen des CDH1-Verlustes identifiziert werden, darunter Promotormethylierung, Deletionen innerhalb des betroffenen Gens oder neuartige dysfunktionale Fusionen. Tatsächlich konnte eine bisher unbekannte Fusion zwischen den Chromosomen 13 und 16 beschrieben werden, die – ähnlich der biallelischen Mutation – ebenfalls zum Funktionsverlust des E-Cadherins führt. Diese alternativen Mechanismen können Patholog:innen morphologisch anhand einer aberranten, schwachen oder granulären E-Cadherin-Immunhistochemie erkennen.
Relevanz von RNA-Fusionsprodukten für die Therapie
Nolan Priedigkeit von der Harvard-Universität untersuchte die prognostische und therapeutische Relevanz von RNA-Fusionsprodukten. Das Mammakarzinom gehört zu den Tumorerkrankungen mit den meisten karyotypischen Aberrationen und daraus resultierenden „RNA splice variant“-Fusionsprodukten. Diese charakteristischen Fusions-RNAs treten im Rahmen der Karzinomgenese relativ früh auf und scheinen über weite Strecken der Tumorprogression konserviert zu sein oder sogar zuzunehmen.
Mithilfe eines mehrstufigen Identifikationsalgorithmus mit überwachten und nicht überwachten statistischen Methoden wurden solche Fusions-RNAs in silico aus Datenbanken identifiziert. Dabei war die Anzahl der identifizierten Fusionstranskripte von dem intrinsischen Subtyp der Mammakarzinome abhängig: Luminale Erkrankungen wiesen die meisten unterschiedlichen Fusionstranskripte auf, allerdings war die Frequenz dieser Transkripte beim tripelnegativen (TNBC) oder HER2-positiven Mammakarzinom höher. Die genaue Analyse der gefundenen Transkripte hat mehrere biologisch relevante und therapierbare Fusionspartner wie ESR, FGFR, BRAF oder PIK3CA identifiziert. Durch eine longitudinale Analyse von Patient:innenproben konnte gezeigt werden, dass solche ESR1-Fusionstranskripte die Wirksamkeit palliativer Therapien im metastasierten Setting negativ beeinflussen. Die medikamentöse Hemmung solcher Transkripte könnte die Behandlungsmöglichkeiten und die Prognose des metastasierten Mammakarzinoms weiter verbessern.
Einfluss der genetischen Disposition auf die Antitumorimmunantwort
Ein ebenfalls vielversprechender Therapieansatz ist die Immuntherapie. Die Arbeitsgruppe von Cristina Curtis von der Stanford-Universität hat genetische Determinanten identifiziert, die beim Immunoediting eine wichtige Rolle spielen. Danach kann die eigene genetische Veranlagung die Effektivität einer Antitumorimmunantwort maßgeblich beeinflussen. Je nach genetischer Prädisposition gibt es Unterschiede in der Anzahl und Affinität von Keimbahn-assoziierten Epitopen an der Zelloberfläche von somatischen Zellen und Tumorzellen. Die Autor:innen nannten dies „germline epitope burden“ (GEB). Der GEB ist mit fokalen Amplifikationen im Genom assoziiert. Dadurch lassen sich mehrere genomisch definierte Untergruppen identifizieren.
Die jetzt präsentierte Studie konnte eine inverse Assoziation zwischen diesen Epitopen und der Wahrscheinlichkeit, ein HER2-positives Mammakarzinom zu entwickeln, nachweisen. Allerdings konnte sie auch demonstrieren, dass ein hoher GEB bei einem bereits bestehenden Karzinom die Immunantwort durch die Depletion von Antitumor-Lymphozyten beeinträchtigt. Patient:innen mit einem niedrigen GEB hatten ein signifikant längeres Überleben als jene mit einem hohen GEB. Ob und wie solche genetische Prädispositionen eine Änderung der bekannten Immuntherapieschemata erfordern, muss in zukünftigen Studien untersucht werden.
Neue Biomarker für Prognose und Therapieansprechen
Ein weiterer Höhepunkt war die Präsentation der Ergebnisse von translationellen Analysen der randomisierten Studien monarchE und PALLAS. Bei beiden Studien war die prospektive Sammlung von Tumorproben Einschlusskriterium, um neue Biomarker zu identifizieren. Die Studie monarchE untersuchte die Wirksamkeit einer adjuvanten Gabe des „Cyclin-abhängiger Kinase“(CDK)-Inhibitors Abemaciclib in Kombination mit endokriner Standardtherapie beim luminalen Mammakarzinom mit erhöhtem Rezidivrisiko.1 Die „Intention to treat“(ITT)-Population inkludierte 5637 Patient:innen, die translationelle Kohorte umfasste etwa 1200 Patient:innen. Aus den gewonnenen Tumorproben wurde sowohl DNA als auch RNA isoliert, um Whole-Exome-Sequencing sowie RNA-Sequencing durchzuführen. Die translationelle Kohorte wies keine statistisch signifikanten Unterschiede zur ITT-Kohorte auf: In allen Kohorten konnte ein Benefit durch die Zugabe von Abemaciclib erzielt werden. Dieser war unabhängig vom intrinsischen Subtyp der Tumorerkrankung. Eine initiale Korrelation der häufigsten genomischen Aberrationen zeigte, dass eine Amplifikation des MYC-Gens möglicherweise diesen Benefit schmälern könnte. Allerdings sind weitere, größere Analysen notwendig, um die Interaktion statistisch signifikant zu bestätigen.
Eine weitere internationale randomisierte Studie mit einer ambitionierten translationellen Begleitanalyse ist PALLAS. Diese Studie untersuchte, ob die Zugabe des CDK-Inhibitors Palbociclib die Prognose beim luminalen Mammakarzinom mit erhöhtem Rezidivrisiko verbessert.2 Die Studie verlief negativ: Palbociclib konnte das rezidivfreie und das Gesamtüberleben dieser Patient:innen nicht verlängern. Ein explorativer Endpunkt der translationellen Studie war der Einfluss des intrinsischen Subtyps nach PAM50 auf die Prognose und auf das Therapieansprechen. Die statistischen Analysen wurden dadurch erschwert, dass die translationelle Kohorte ein signifikant kürzeres Überleben aufwies als die ursprüngliche ITT-Population. Dies könnte laut Autor:innen der Studie daran liegen, dass kleinere Tumoren und bestimmte ethnische Gruppen in der translationellen Kohorte unterrepräsentiert waren. Unabhängig von der Ursache verschlechterte dieser Umstand die Aussagekraft der Analysen. So war in der PALLAS-Studie der intrinsische Subtyp nach PAM50 weder prognostisch noch prädiktiv. Dies ist ein unerwartetes Ergebnis, das neben der fraglichen Repräsentativität der untersuchten Kohorte weitere Fragen aufwirft: Inwieweit ist der Primärtumor auch für die Lymphknotenmetastasen repräsentativ, die letztendlich den stärksten prognostischen Faktor beim Mammakarzinom darstellen? Möglicherweise wäre Tumorgewebe aus den Lymphknotenmetastasen geeigneter, um die Prognose und das Therapieansprechen bei diesen Patient:innen zu untersuchen.
Zusammengefasst hat das SABCS 2023 mehrere innovative Wege zur Entwicklung von Biomarkern und zielgerichteten Therapieoptionen aufgezeigt. Ob diese Ergebnisse auch in die Praxis umgesetzt werden können, werden zukünftige Untersuchungen zeigen.
Literatur:
1 Johnston SRD et al.: Abemaciclib combined with endocrine therapy for the adjuvant treatment of HR+, HER2-, node-positive, high-risk, early breast cancer (monarchE). JClin Oncol 2020; 38(34): 3987-98 2 Gnant M et al.: Adjuvant palbociclib for early breast cancer: the PALLAS trial results (ABCSG-42/AFT-05/BIG-14-03). J Clin Oncol 2022; 40(3): 282-93
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...