Manchmal reicht Abwarten
Bericht:
Dr. med. Judith Moser
Autor:
PD Dr. med. Aurelius Omlin
Onkozentrum Zürich und
Chairman Uroonkologisches Zentrum
Hirslanden Zürich
E-Mail: aurelius.omlin@ozh.ch
Vor dem Hintergrund der Vielzahl an mittlerweile vorhandenen zielgerichteten und immuntherapeutischen Behandlungsoptionen orientiert sich das Management des Nierenzellkarzinoms im adjuvanten und fortgeschrittenen Setting an einer Reihe von Faktoren. Bei sehr guter Prognose kann auch nur «watchful waiting» angezeigt sein.
Beim frühen Nierenzellkarzinom (RCC) gibt das Leibovich-Modell Auskunft über die individuelle Wahrscheinlichkeit des krebsspezifischen Überlebens in den nächsten 15 Jahren und kann somit bei der Risikoeinschätzung helfen.1 Auf therapeutischer Ebene hat im Bereich der Tyrosinkinasehemmer (TKI) nur Sunitinib im adjuvanten Setting einen Vorteil in Bezug auf das krankheitsfreie Überleben (DFS) gezeigt.2 Fünf weitere Studien mit anderen TKI verliefen negativ.
Ähnlich stellt sich die Situation in Bezug auf die Checkpoint-Inhibitoren (CPI) dar. Für adjuvantes Pembrolizumab konnte in der Studie KEYNOTE-564 gegenüber Placebo ein DFS-Benefit nachgewiesen werden (HR: 0,63; p<0,0001).2 Auch im Hinblick auf die Gesamtüberlebensrate nach 48 Monaten schnitt der CPI signifikant besser ab (91,2% vs. 86,0%).3 Dagegen erbrachten drei andere Studien keine DFS-Vorteile von Atezolizumab bzw. Nivolumab mit oder ohne Ipilimumab.2
Empfehlungen imadjuvanten Setting
Die internationalen Guidelines legen übereinstimmend nahe, dass die Gabe von adjuvantem Pembrolizumab beim frühen RCC in Erwägung gezogen werden kann.4–6 Eine Aufklärung der Patient:innen im Hinblick auf potenzielle Nebenwirkungen sowie Information über den Umstand, dass mehrere Studien keine Vorteile ergeben haben, wird empfohlen.
Insgesamt stellt die Individualisierung den wichtigsten Aspekt im Zusammenhang mit der adjuvanten RCC-Therapie dar. An meiner Abteilung werden die Patient:innen prä- und postoperativ im Tumorboard besprochen. Bei Vorliegen einer klarzelligen Histologie und der Kriterien für eine adjuvante Therapie erfolgen eine onkologische Beratung und klinische Beurteilung sowie eine Risikoberechnung gemäss dem Leibovich-Modell. Die Vor- und Nachteile der Behandlung werden besprochen und eine individuelle Entscheidung gefällt. Keine Indikation zur adjuvanten Therapie besteht derzeit bei nichtklarzelligen Histologien.
Wenn unter oder nach einer adjuvanten Behandlung eine Progression eintritt, richtet sich das Vorgehen nach deren Ausmass.7 Bei einem oligometastatischen Rezidiv kommen lokale Massnahmen (Metastasektomie, stereotaktische Bestrahlung) oder auch nur aktive Surveillance infrage. Ist dagegen von einer primären Resistenz auszugehen (Progression innerhalb von drei Monaten), wird eine TKI-Therapie empfohlen. Patient:innen mit Frührezidiv (Progression nach 3–12 Monaten) sollen ebenfalls einen TKI alleine bzw. in ausgewählten Fällen zusätzlich zum CPI erhalten. Bei späteren Rezidiven kommt primär wieder die TKI-Gabe infrage, aber auch eine TKI/CPI- oder CPI/CPI-Kombinationsstrategie.
Metastasiertes RCC:Zurückhaltung bei guter Prognose
Im Setting des metastasierten RCC steht angesichts der Vielzahl an verfügbaren Optionen ebenfalls die individuelle Entscheidungsfindung im Fokus. Dafür sind klinische Beurteilung, Komorbiditäten/Medikamente, Labor inklusive Blutbild, Nieren- und Leberfunktionswerten, CRP-Spiegel und Kalzium ebenso ausschlaggebend wie die Bildgebung (CT, eventuell cMRI, Szintigrafie) und die Histologie. Eine genetische Beratung erscheint vor allem bei einem Erkrankungsalter <47 Jahren, bilateralen oder multifokalen Tumoren und positiver Familienanamnese angezeigt. Der IMDC-Risikoscore ermöglicht auch in der Ära der CPI/CPI- bzw. TKI/CPI-Kombinationen eine gute Differenzierung in die drei Risikogruppen günstig, intermediär und ungünstig.8
2024 präsentierte Daten konnten zeigen, dass bei Patient:innen mit sehr günstigem Risikoprofil (Intervall seit der Diagnose >3 Jahre, keine ZNS-, Leber- oder Knochenmetastasen, Performance-Status 90–100%) eine Surveillance ausreichen kann.9 Bei Oligometastasierung genügt unter Umständen eine fokale Therapie. Insgesamt belegten die Daten bei günstiger Prognose keinen Vorteil der TKI/CPI-Kombination gegenüber der TKI-Monotherapie. Allerdings bewirkte die Kombination aus Ipilimumab und Nivolumab langfristig einen Gesamtüberlebens(OS)-Benefit und wurde daher von den ESMO- und NCCN-Guidelines als Option in der günstigen Prognosegruppe aufgenommen.4,5,10
Differenzierung zwischen den TKI
Bei Patient:innen mit intermediärer/ungünstiger Prognose laut IMDC bilden CPI/CPI- und TKI/CPI-Regimes den Behandlungsstandard.4,5 In den Guidelines werden die Kombinationen ohne Ranking aufgelistet, de facto bestehen zwischen den TKI jedoch Unterschiede in Bezug auf Wirkmechanismus und Halbwertszeiten.11 Der VEGF-Rezeptor stellt allgemein das wichtigste Target dar. Lenvatinib setzt zusätzlich an FGFR an, während Cabozantinib ein breiteres Spektrum aufweist. Axitinib besticht durch die weitaus kürzeste Halbwertszeit aller TKI und eine flexible Dosierung.
Ein frühzeitiges Nebenwirkungsmanagement trägt dazu bei, die Patient:innen länger auf Therapie zu halten. Zum Teil bestehen überlappende Toxizitäten unter Nivolumab und Cabozantinib, etwa Hautausschläge oder Diarrhö.12 Dosismodifikationen werden bei fast allen Patient:innen unter TKI-Therapie erforderlich. Die immunassoziierten Toxizitäten der CPI sind bekannt und mit den etablierten Massnahmen behandelbar.
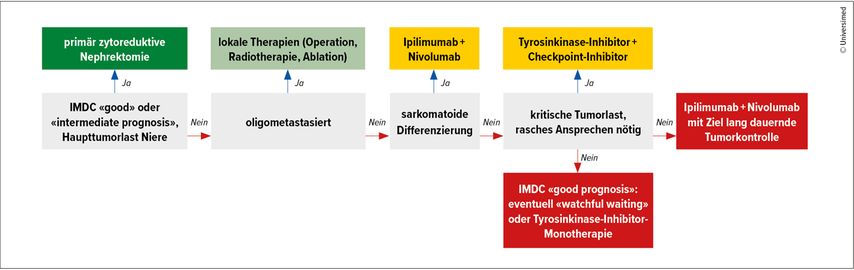
Ein möglicher Algorithmus beim klarzelligen metastasierten RCC ist in der Abbildung 1 dargestellt.13 Initial erscheint eine zytoreduktive Nephrektomie vor allem dann sinnvoll, wenn die Haupttumorlast von der Niere ausgeht. Bei Oligometastasierung soll, wenn möglich, eine lokale Behandlung erfolgen, bei sarkomatoider Differenzierung primär eine CPI/CPI-Kombinationstherapie. Falls der/die Patient:in ein rasches Ansprechen benötigt, kommt vorrangig eine TKI/CPI-Kombination infrage, andernfalls Nivolumab/Ipilimumab oder eine TKI-Monotherapie bzw. «watchful waiting».
Abb. 1: Möglicher Therapiealgorithmus beim metastasierten klarzelligen Nierenzellkarzinom (modifiziert nach Braun DA)13
Nichtklarzelliges RCC: neue Daten
Im Setting des nichtklarzelligen RCC liegt aufgrund der Seltenheit der Tumoren kein hoher Evidenzgrad vor. Die Guidelines führen eine Palette an Optionen abhängig vom Subtyp an.4 Mit SUNNIFORECAST wurde am ESMO-Jahrestreffen 2024 eine interessante Studie präsentiert, die einen OS-Vorteil durch Ipilimumab/Nivolumab im Vergleich zur Standardtherapie ergab (86,9% vs. 76,8% nach zwölf Monaten).14 Eine Aufnahme der Kombination in die Guidelines erscheint denkbar.
Bei allen Tumoren steht die Wichtigkeit regelmässiger Kontrollen zwecks Erfassung von Wirksamkeit und Toxizität der Therapie ausser Frage. Eine enge Zusammenarbeit zwischen dem behandelnden Team und den Patient:innen ist entscheidend, um optimale Ergebnisse zu erzielen.
Literatur:
1 Leibovich BC et al.: Predicting oncologic outcomes in renal cell carcinoma after surgery. Eur Urol 2018; 73(5): 772-80 2 Boyle JJ et al.: Adjuvant therapy for renal cell carcinoma: end points, outcomes, and risk assessments. JCO Precis Oncol 2023; 7: e2200407 3 Choueiri TK et al.: Overall survival with adjuvant pembrolizumab in renal-cell carcinoma. N Engl J Med 2024; 390(15): 1359-71 4 Escudier B et al.: Renal cell carcinoma: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 2019; 30(5): 706-20 5 NCCN Guidelines Kidney Cancer, Version 2.2025, September 6, 2024 6 Ljungberg B et al.: EAU Guidelines on Renal Cell Carcinoma, Limited Update, March 2024 7 Bourlon MT et al.: ASCO Daily News, 10. Januar 2024 8 Ernst MS et al.: Outcomes for International Metastatic Renal Cell Carcinoma Database Consortium prognostic groups in contemporary first-line combination therapies for metastatic renal cell carcinoma. Eur Urol 2023; 84(1): 109-16 9 Plimack ER et al.: Pembrolizumab plus axitinib versus sunitinib as first-line treatment of advanced renal cell carcinoma: 43-month follow-up of the phase 3 KEYNOTE-426 study. Eur Urol 2023; 84(5): 449-54 10 Tannir NM et al.: Nivolumab plus ipilimumab versus sunitinib for first-line treatment of advanced renal cell carcinoma: extended 8-year follow-up results of efficacy and safety from the phase III CheckMate 214 trial. Ann Oncol 2024; 35(11): 1026-103 11 Puissent F et al.: Therapeutic drug monitoring of tyrosine kinase inhibitors in the treatment of advanced renal cancer. Cancers (Basel) 2023; 15(1): 313 12 McGregor B et al.: Management of adverse events associated with cabozantinib plus nivolumab in renal cell carcinoma: a review. Cancer Treat Rev 2022; 103: 102333 13 Braun DA: Harnessing the immune system in renal cell carcinoma: current and novel immunotherapy approaches. ASCO 2023; oral presentation 14 Bergmann L et al.: Prospective randomised phase-II trial of ipilimumab/nivolumab versus standard of care in non-clear cell renal cell cancer: results of the SUNNIFORECAST trial. ESMO 2024; Abstr. #LBA75
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...