Neuigkeiten aus der gynäkologischen Onkologie
Autor*innen:
PD Dr. med. Marcus Vetter1, 3
Prof. Dr. med. Viola Heinzelmann1, 2
1 Gynäkologisches Tumorzentrum,
Universitätsspital Basel
2 Klinik für Gynäkologische Onkologie,
Universitätsspital Basel
3 Medizinische Onkologie, Hämatologie und
Immuntherapie, Medizinische Universitätsklinik,
Kantonsspital Baselland
Korrespondenz:
E-Mail: marcus.vetter@ksbl.ch
Das Fachgebiet der gynäkologischen Onkologie entwickelt sich stetig weiter. Dies wurde auch wieder eindrucksvoll am amerikanischen Krebskongress ASCO 2022 in Chicago gezeigt. Schwerpunkt waren Arbeiten auf dem Gebiet des Ovarialkarzinoms. Hier ging es vor allem um Daten zur Erhaltungstherapie mit PARP-Inhibitoren, aber auch neue Substanzen wurden vorgestellt. Im Bereich des Endometriumkarzinoms wurden vor allem Daten und Subgruppenanalysen zur Immuntherapie präsentiert. Eine wichtige Frage war hier auch der frühere Einsatz von Immuntherapien. In Bezug auf das Zervixkarzinom wurden interessante Daten zu den Antikörper-Wirkstoff-Konjugaten (ADC) vorgestellt. Die Entwicklung geht bei dieser Substanzklasse in vielen kleinen Schritten voran und die Behandlungsoptionen werden sich weiter verbessern. Der folgende Artikel gibt Auskunft über die wichtigsten «Practice changing»-Beiträge vom ASCO-Jahrestreffen.
Neue Daten zum Ovarialkarzinom
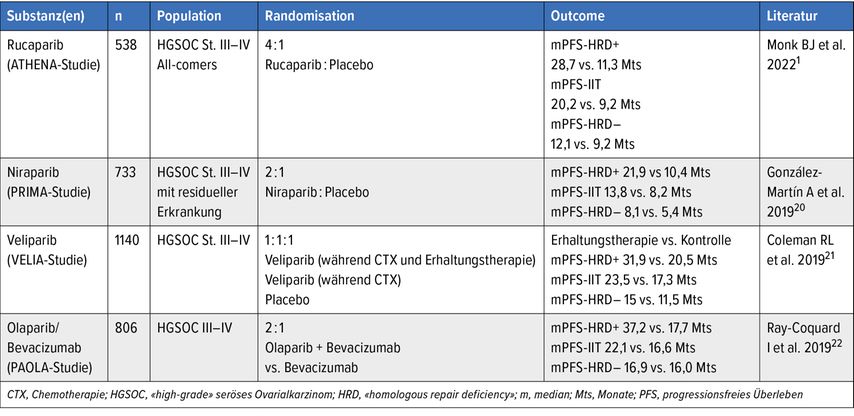
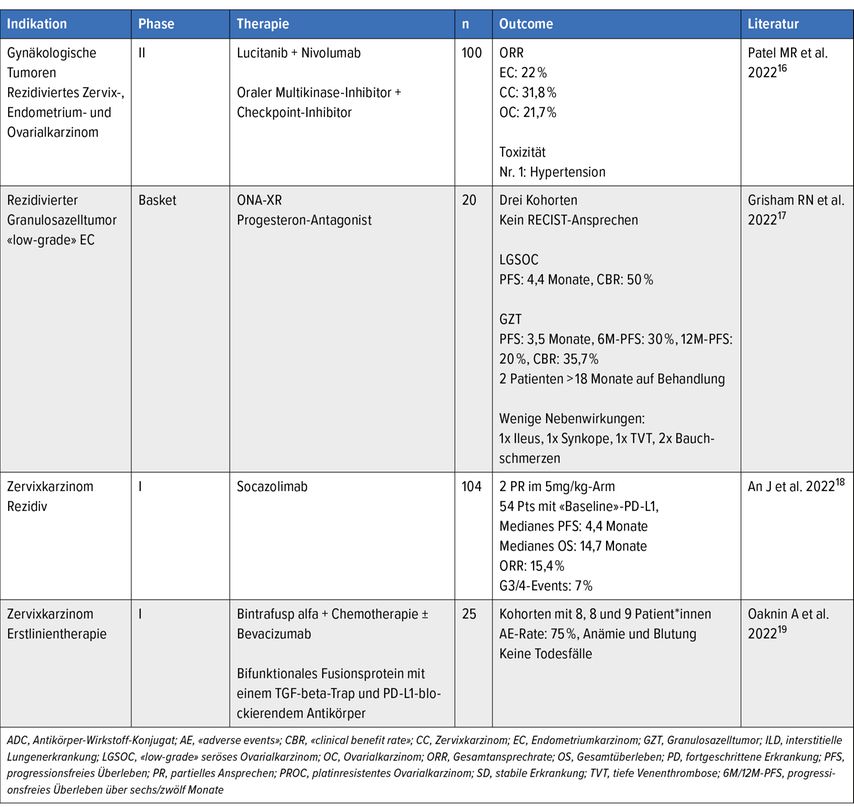
Das Ovarialkarzinom bleibt mit einer 5-Jahres-Überlebensrate von 40% weiterhin eine grosse Herausforderung für die Klinik und die Forschung. Die Erhaltungstherapie mit VEGF-/PARP-Inhibitoren (Tab. 1) brachte in den letzten Jahren eine deutliche Verbesserung im Bereich der Systemtherapie.
Beim «high-grade» serösen Ovarialkarzinom wurden nun Daten zur primären Erhaltungstherapie mit Rucaparib gezeigt, so zum Beispiel in der mehrarmigen ATHENA-Studie.1 Die eingeschlossene Patient*innenpopulation ist mit der der PRIMA-Studie vergleichbar (Erhaltungstherapie mit Niraparib). Bemerkenswert war das lange progressionsfreie Überleben (PFS) bei Patient*innen mit Tumoren, die eine «homologous repair deficiency» (HRD) aufwiesen. Hier zeigte sich ein medianes progressionsfreies Überleben (PFS) von 28,7 Monaten (Rucaparib) gegenüber 11,3 Monaten (Placebo; 95% CI: 23,0–NR).
Die häufigsten Nebenwirkungen (≥Grad3) waren Anämie (28,7%) und Neutropenie (14,6%). Mit der Studie konnte erneut die Wichtigkeit einer «Up-front»-Erhaltungstherapie mit PARP-Inhibitoren gezeigt werden, vor allem mit den Biomarkern HRD+ und BRCA. Tabelle 1 gibt eine Übersicht über die wichtigsten klinischen Studien zur primären Erhaltungstherapie.
In einer retrospektiven Analyse aus Japan wurde beim fortgeschrittenen klarzelligen Ovarialkarzinom der Stellenwert von Bevacizumab untersucht.2 Insgesamt wurden 145 Patient*innen in diese Analyse eingeschlossen. Zu bemerken bleibt, dass auch dosisdichte Chemotherapie-Regime verwendet wurden und dass in der Gruppe mit Bevacizumab-Therapie mehr komplette Resektionen erreicht werden konnten.
Nach 36 Monaten Follow-up wurde ein signifikanter Anstieg des medianen PFS von 12,5 auf 29,7 Monate verzeichnet. («Log-rank»-Test: p=0,023, Wilcoxon-Test: p=0,006). Das mediane Gesamtüberleben (OS) stieg von 34,7 auf 51,4 Monate («Log-rank»-Test: p=0,085, Wilcoxon-Test: p=0,027). Der Gebrauch von Bevacizumab, ECOG PS<2 und die komplette Resektion waren in einer Multivariatanalyse unabhängige prognostische Faktoren.
Die Studie wies in einem relativ grossen Kollektiv von Patient*innen mit klarzelligem Ovarialkarzinom ein klares PFS/OS-Signal auf, welches auf jeden Fall weiter untersucht werden sollte. Studien zur Antiangiogenese beim klarzelligen Ovarialkarzinom laufen. In der westlichen Welt macht das klarzellige Ovarialkarzinom rund 5% aller Histosubtypen aus. Damit ist es nicht einfach, Teilnehmende für Studien zu rekrutieren.
Beim platinrefraktären Ovarialkarzinom wurden erstmalig Daten für eine Therapie mit Relacorilant (Rela) in Kombination mit Nab-Paclitaxel (NP) gezeigt. Diese Patient*innengruppe hat in der Regel ein sehr kurzes behandlungsfreies Intervall und ein Gesamtüberleben von median zwölf Monaten.
Relacorilant ist ein präklinisch und klinisch untersuchter Glukokortikoidrezeptor(GC-Rezeptor)-Modulator und interagiert mit «Apoptose-Pathways». Damit wird die zytotoxische Wirksamkeit der Chemotherapie gesteigert. In die dreiarmige Phase-II-Studie wurden insgesamt 178 Patient*innen eingeschlossen:3
-
a) NP 80mg/m2 plus intermittierendes Rela (150mg 4x/d, Tag –1, 0 und +1; n=60)
-
b) NP 80mg/m2 plus kontinuierliches Rela (100mg 4x/d; n=58)
-
c) NP 100mg/m2 (n=60)
Das mediane OS betrug 13,9, 11,3 und 12,2 Monate für a), b) und c). Die intermittierende Gabe zeigte damit einen Überlebensvorteil. Für eine Phase-III-Studie mit dem GC-Rezeptor-Modulator werden bereits Teilnehmende rekrutiert. Die Studie wirft jedoch die alte Frage auf, ob Glukokortikoide für Patient*innen unter Chemotherapie nicht einen Prognosenachteil aufweisen.
Eine weitere Studie im Bereich des platinrefraktären Ovarialkarzinoms untersuchte das ADC Mirvetuximab Soravtansin (MIRV).4 Dieses ADC bindet an den Folatrezeptor-alpha. Es wurde bereits auf mehreren Kongressen präsentiert. Das «Payload» ist Maytansinoid DM4, ein potentes Tubulin-hemmendes Zytostatikum. In diese Phase-III-Studie wurden Patient*innen mit rezidiviertem Ovarialkarzinom mit hoher Folatrezeptor-alpha-Dichte (Roche FOLR1-Assay: ≥75% der Zellen mit Färbeintensität von PS2+) eingeschlossen. Bis zu drei Vorbehandlungen inklusive PARP-Inhibitor und Bevacizumab waren erlaubt.
Zu dieser Studie wurde am ASCO-Jahrestreffen eine genaue Analyse des Ansprechens gezeigt. Die Gesamtansprechrate lag bei 32,4%. Die mittlere Zeit bis zum Ansprechen lag bei 1,5 Monaten (1–5,6 Monate). Bei 71% aller Patient*innen war eine Tumorverkleinerung festzustellen. Die wichtigsten Nebenwirkungen umfassten Verschlechterung des Sehvermögens, Keratopathie und Nausea. Die Autor*innen schlossen aus ihrer Arbeit die Wichtigkeit einer Biomarker-gerichteten Therapie beim platinrefraktären Ovarialkarzinom. Die Substanz soll weiterentwickelt werden.
Eine weitere Studie zum «high grade» serösen Ovarialkarzinom (MITO23/ET-743) untersucht in einem randomisierten Phase-III-Setting die Chemotherapie Trabectedin gegenüber «treatment of physician’s choice» (TPC).5 Trabectedin ist bisher vor allem als Einzelsubstanz bei Patient*innen mit Rezidiv untersucht worden, hier zeigte sich eine Ansprechrate von 20–40%.
In einer früheren Phase-II-Studie mit Patient*innen mit BRCA-Mutationen oder «BRCAness» zeigte Trabectedin eine hohe Ansprechrate und ein Gesamtüberleben von 18 Monaten. Nun wurde in der Phase-III-Studie das Konzept weiter untersucht. In die Studie wurden ebenfalls Patient*innen mit Rezidiv und einer BRCA-Mutation oder «BRCAness»-Phänotyp eingeschlossen (Definition: Ansprechen auf die beiden letzten Carboplatin-basierten Chemotherapien).
Insgesamt wurden 244 Patient*innen in den Studienarm mit Trabectedin 1,3mg/m2 q3w und den Studienarm mit TPC (Carboplatin, Gemcitabin, wöchentlich Paclitaxel, «pegylated liposomal doxorubicine» [PLD] oder Topotecan) randomisiert.
Nach 40-monatigem Follow-up wurde kein Vorteil für die Behandlung mit Trabectedin gesehen. Das mediane PFS lag bei 4,4 und 4,9 Monaten (HR: 1,03; p=0,848) und das mediane OS bei 17,9 und 15,8 Monaten (HR: 1,15; p=0,304). Die Gesamtansprechrate betrug 15,4% für Trabectedin und 20,2% für TPC. Damit konnte in der Population von Patient*innen mit BRCA/«BRCAness»-Phänotyp kein Vorteil gegenüber TPC gezeigt werden.
Zum «low-grade» serösen Ovarialkarzinom (LGSOC) wurden ebenfalls Daten präsentiert.6 Die Therapie dieser Tumoren ist komplex, nur selten findet sich einChemotherapie-Ansprechen (Ansprechrate 11%). In eine Phase-II-Pilotstudie wurden Patient*innen mit nicht resezierbarem LGSOC eingeschlossen. Der Studienarm untersuchte die Kombination des selektiven Östrogenrezeptor-Modulators (SERD) Fulvestrant und des CDK4/6-Inhibitors Abemaciclib bei 15 Patient*innen. Es zeigte sich eine sehr gute klinische Benefitrate von 80% (47% komplettes Ansprechen [CR], 33% stabile Erkrankung [SD]). Die Autor*innen folgerten, dass die Kombination eine sehr hohe Kontrollrate und gute Verträglichkeit hatte. Weitere Studien sind geplant.
Am Kongress wurden auch Daten der chirurgischen Studie DESKTOP III präsentiert. DESKTOP III zeigte den Stellenwert des sekundären Tumordebulkings beim Ovarialkarzinom. Die initialen Ergebnisse der Phase-III-Studie zeigten einen signifikanten Überlebensvorteil für das sekundäre Debulking bei Patient*innen mit Ovarialkarzinom, die nach dem AGO Score selektioniert wurden (kein Aszites, «single site», längeres [>6 Monate] therapiefreies Intervall).
Die jetzt gezeigte Analyse ging der Frage nach, ob Patient*innen, die im Chemotherapie-Arm der DESKTOP-III-Studie waren, von einem Debulking nach dem zweiten Progress profitieren würden.7 In der Analyse erlitten 171 Patient*innen einen Progress. Insgesamt erhielten 32 Patient*innen (19%) ein sekundäres Debulking (R0-Rate 60%). Die Gesamtüberlebensrate nach Debulking lag bei 54 Monaten, allerdings fand sich eine 30- bzw. 90-Tages-Mortalität von 3% bzw. 6%.
Neue Daten zum Endometriumkarzinom
Beim Endometriumkarzinom scheint die Immuntherapie eine wichtige Rolle zu spielen. Mittlerweile sind auch Checkpoint-Inhibitoren für die Behandlung verfügbar. Am ASCO-Kongress wurde die dritte Interimsanalyse zur GARNET-Studie vorgestellt.8 Die GARNET-Studie untersuchte den PD-1-Checkpoint-Inhibitor Dostarlimab nach Versagen einer platinbasierten Chemotherapie beim metastasierten Endometriumkarzinom.
Die Gesamtansprechrate lag für Tumoren mit Mikrosatelliteninstabilität (MSI) bei 45,5% und für Tumoren mit Mikrosatellitenstabilität (MSS) bei 15,4%. Entsprechend betrug das mediane PFS sechs Monate und 2,7 Monate. Das mediane Gesamtüberleben lag bei «nicht erreicht» und 16,9 Monaten. Die Autor*innen folgerten aus den Daten, dass Dostarlimab auch in der MSS-Gruppe ein konstantes Ansprechen zeigte und die Behandlung bzgl. Toxizität keine neuen Signale aufwies.
Eine weitere kleine Phase-II-Studie untersuchte beim metastasierten Endometriumkarzinom eine Chemotherapie-freie Dreierkombination aus Rucaparib, Atezolizumab und Bevacizumab.9 In die Studie konnten Patient*innen mit bis zu zwei Chemotherapien in der Vorbehandlung einschlossen werden. Alle histologischen Subtypen wurden inkludiert (50% seröse Histologie, 20% endometroide Histologie und 13% Karzinosarkom).
Von den 30 eingeschlossenen Patient*innen konnten 26 in der Studie evaluiert werden. 23 Patient*innen hatten einen klinischen Benefit: eine CR (4%), neun partielles Ansprechen [PR] (39%) und 13 SD (57%). Das ereignisfreie Überleben lag bei 5,3 Monaten, bei den Patient*innen mit MSI lag es bei 11,9 Monaten. Mit 50% wurde eine hohe Rate von Grad-3/4-Toxizität beobachtet. Die Kombination zeigte insgesamt eine sehr hohe Ansprechrate und sollte in weiteren Studien untersucht werden.
Neben der Immuntherapie gibt es weitere interessante zielgerichtete Ansätze beim Endometriumkarzinom, die die molekularen Marker berücksichtigen. So wurden am Kongress die Daten der SIENDO-Studie vorgestellt, die Selinexor in der Erhaltungstherapie beim metastasierten Endometriumkarzinom untersucht. Selinexor ist ein spezifischer XPO1-Inhibitor, der zur Nukleusretention und Aktivierung des Tumorsuppressorproteins TSP inkl. p53 führt. In diese Phase-III-Studie wurden Patient*innen mit metastasiertem Endometriumkarzinom und nach Abschluss einer Erstlinientherapie mit platin-/taxanhaltiger Chemotherapie eingeschlossen. Die Studie wurde 2:1 randomisiert und war placebokontrolliert. Das mediane PFS lag bei 5,7 Monaten (Selinexor) vs. 3,8 Monate (Placebo).
Neue Daten zum Zervixkarzinom
Die Prognose des metastasierten Zervixkarzinoms ist mit einer 5-Jahres-Gesamtüberlebensrate von ca. 10% immer noch sehr schlecht. Am ASCO-Jahrestreffen wurde eine Subgruppenanalyse der KEYNOTE-826-Studie gezeigt.10 In der Studie wurden Patient*innen mit metastasiertem/nicht resezierbarem Zervixkarzinom, sowohl Plattenepithel- als auch Adenokarzinome, eingeschlossen. Die Patient*innen erhielten Chemotherapie ± Pembrolizumab, Bevacizumab war in beiden Armen erlaubt.
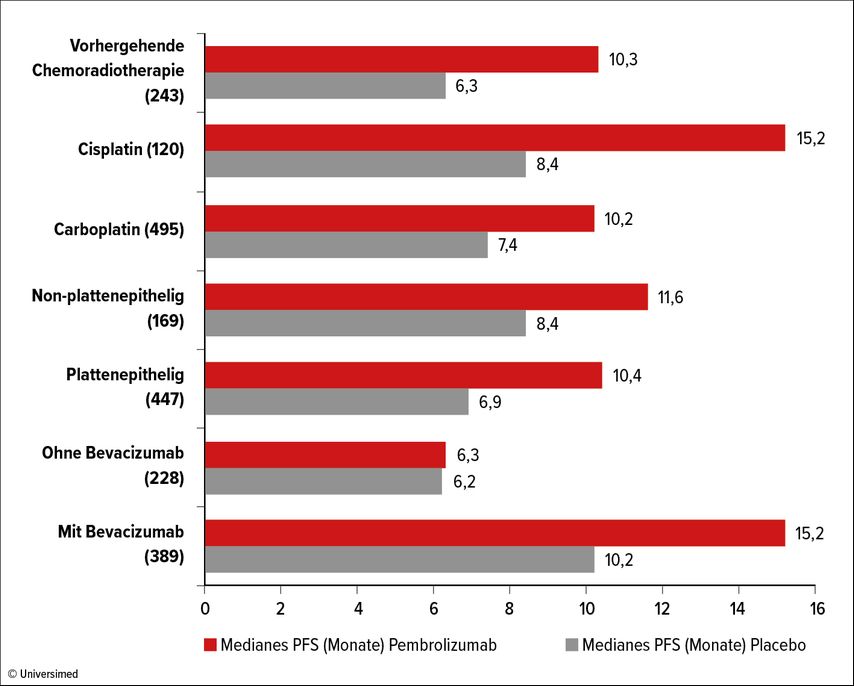
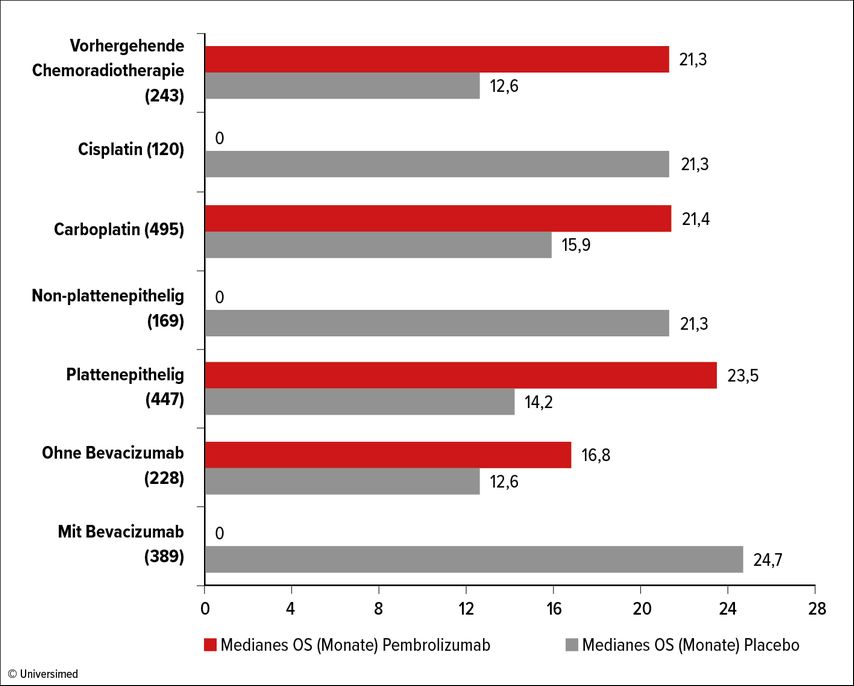
Die Kombinationstherapie zeigte einen deutlichen PFS/OS-Vorteil für den Studienarm mit Chemotherapie + Pembrolizumab. Nun wurden auch die Subgruppenanalysen präsentiert. In allen Subgruppen war die Behandlung im Studienarm von signifikantem Vorteil für das PFS/OS (Chemotherapie mit Carboplatin/Cisplatin, mit/ohne Bevacizumab, Vorbehandlung mit Radiochemotherapie ja/nein, Adenokarzinom/Plattenepithelkarzinom-Histologie). Die Daten weisen nun einen klaren Vorteil des bereits verwendeten Regimes (Chemotherapie + Pembrolizumab) auf und stellen damit den neuen Therapiestandard in der Erstlinie beim metastasierten Zervixkarzinom dar (Abb. 1).
Abb. 1a: Daten zum progressionsfreien Überleben (PFS, in Monaten) aus der KEYNOTE-826-Subgruppenanalyse
Das ADC Tisotumab Vedotin (TV) wurde beim vorbehandelten metastasierten Zervixkarzinom basierend auf der Phase-II-Studie innovaTV in den USA bereits zugelassen. TV ist ein ADC mit einem Antikörper gegen den Tissue-Faktor. Vedotin (Zytostatikum = Monomethyl-Auristatin E) ist ein Spindelgift, das zum G2/M-Zellzyklusarrest und zur Apoptose führt. In der Phase-II-Studie lag die Gesamtansprechrate bei 24%.
In einer weiteren Studie wurden nun in der Erstlinientherapie Tisotumab Vedotin und Pembrolizumab an 33 Patient*innen in einer Dosis-Expansionskohorte untersucht.11 Die Gesamtansprechrate lag bei 41%. Die mittlere Zeit bis zum Ansprechen lag bei 1,4 Monaten. Das mediane PFS betrug 5,1 Monate, das mediane OS wurde in der Follow-up-Zeit von zwölf Monaten nicht erreicht. Die häufigsten Nebenwirkungen waren Alopezie, Diarrhö, Epistaxis, Konjunktivitis und Nausea. Die Autor*innen schlussfolgerten, dass die Interimsanalyse eine gute Ansprechrate zeigt und die Studie fortgeführt wird.
Schlussfolgerung
Die Behandlung der gynäkologischen Karzinome hat sich in den letzten Jahren deutlich verbessert.
Beim Ovarialkarzinom spielt die Erhaltungstherapie eine wichtige Rolle. Der PARP-Inhibitor Rucaparib hat dabei sehr gute und robuste Daten in der primären Erhaltungstherapie für HRD-positive Tumoren gezeigt. Beim Endometriumkarzinom ist die molekulare Subklassifikation in den Guidelines bereits angekommen. Die Immuntherapie spielt derzeit noch eine wichtige Rolle in der Zweitlinie.
Auch Kombinationstherapien aus Antiangiogenese-Therapie und Immuntherapie spielen eine wichtige Rolle. Selinox, ein Apoptose-Induktor, konnte in der Erhaltungstherapie einen kleinen Benefit beim «High-risk»-Endometriumkarzinom aufweisen. Beim Zervixkarzinom ist die Chemoimmuntherapie mittlerweile Standard, in der Zweitlinientherapie sind neue Ansätze mit Antikörper-Wirkstoff-Konjugaten bereits zugelassen oder in Entwicklung.
Die Zahl der Behandlungsmöglichkeiten wird weiter zunehmen, in Zukunft wird das Feld der kurativen Optionen also erweitert sein.
Literatur:
1 Monk BJ et al.: A randomized, phase III trial to evaluate rucaparib monotherapy as maintenance treatment in patients with newly diagnosed ovarian cancer (ATHENA-MONO/GOG-3020/ENGOT-ov45). J Clin Oncol 2022; Online unter 10.1200/JCO.22.01003. Abgerufen am 26.09.2022 2 Seki T et al.: Bevacizumab in first-line chemotherapy to improve the survival outcome for advanced ovarian clear cell carcinoma: a multicenter, retrospective analysis. J Clin Oncol 2022; 40(suppl_16): Abstr. #5502 3 Colombo N et al.: Overall survival data from a 3-arm, randomized, open-label, phase 2 study of relacorilant, a selective glucocorticoid receptor modulator, combined with nab-paclitaxel in patients with recurrent platinum-resistant ovarian cancer. J Clin Oncol 2022; 40(suppl_17): Abstr. #LBA5503 4 Matulonis UA et al.: Mirvetuximab soravtansine (MIRV) in patients with platinum-resistant ovarian cancer with high folate receptor alpha (FRα) expression: Characterization of antitumor activity in the SORAYA study. J Clin Oncol 2022; 40(suppl_16): Abstr. #5512 5 Scambia G et al.: Randomized phase III trial on trabectedin (ET-743) single agent versus clinician’s choice chemotherapy in recurrent ovarian, primary peritoneal, or fallopian tube cancers of BRCA-mutated or BRCAness phenotype patients (MITO23). J Clin Oncol 2022; 40(suppl_17): Abstr. #LBA5504 6 Cobb LP et al.: A pilot phase II study of neoadjuvant fulvestrant plus abemaciclib in women with advanced low-grade serous carcinoma. J Clin Oncol 2022; 40(suppl_16): Abstr. #5522 7 Sehouli J et al.: Role of cytoreductive surgery for the second ovarian cancer relapse in patients previously treated with chemotherapy alone at first relapse: a subanalysis of the DESKTOP III trial. J Clin Oncol 2022; 40(suppl_16): Abstr. #5520 8 Oaknin A et al.: Dostarlimab in advanced/recurrent (AR) mismatch repair deficient/microsatellite instability–high or proficient/stable (dMMR/MSI-H or MMRp/MSS) endometrial cancer (EC): The GARNETstudy. J Clin Oncol 2022; 40(suppl_16): Abstr. #5509 9 Hampton W et al.: An open label, nonrandomized, multisite phase II trial combining bevacizumab, atezolizumab, and rucaparib for the treatment of previously treated recurrent and progressive endometrial cancer. William Hampton. J Clin Oncol 2022; 40(suppl_16): Abstr. #5519 10 Tewari KS et al.: Pembrolizumab + chemotherapy in patients with persistent, recurrent, or metastatic cervical cancer: subgroup analysis of KEYNOTE-826. J Clin Oncol 2022; 40(suppl_16): Abstr. #5506 11 Lorusso D et al.: Tisotumab vedotin (TV) + pembrolizumab (pembro) in first-line (1L) recurrent or metastatic cervical cancer (r/mCC): Interim results of ENGOT Cx8/GOG 3024/innovaTV 205. J Clin Oncol 2022; 40(suppl_16): Abstr. #5507 12 Veneziani A et al.: Pembrolizumab, maveropepimut-S, and low-dose cyclophosphamide in advanced epithelial ovarian cancer: Results from phase 1 and expansion cohort of PESCO trial. J Clin Oncol 2022; 40(suppl_16): Abstr. #5505 13 Nishio S et al.: Safety and efficacy of MORAb-202 in patients (pts) with platinum-resistant ovarian cancer (PROC): Results from the expansion part of a phase 1 trial. J Clin Oncol 2022; 40(suppl_16): Abstr. #5513 14 Au-Yeung G et al.: Poster discussion session IGNITE: a phase II signal-seeking trial of adavosertib targeting recurrent high-grade, serous ovarian cancer with cyclin E1 overexpression with and without gene amplification. J Clin Oncol 2022; 40(suppl_16): Abstr. #5515 15 Embaby A et al.: Adavosertib in combination with carboplatin in advanced TP53-mutated platinumresistant ovarian cancer. J Clin Oncol 2022; 40(suppl_16): Abstr. #5516 16 Patel MR et al.: Efficacy and safety of lucitanib + nivolumab in patients with advanced gynecologic malignancies: phase 2 results from the LIO-1 study (NCT04042116; ENGOT-GYN3/ AGO/LIO). J Clin Oncol 2022; 40(suppl_16): Abstr. #5517 17 Grisham RN et al.: Basket study of oral progesterone antagonist onapristone extended release (ONA-XR) in progesterone receptor positive (PR+) recurrent granulosa cell (GCT), low-grade serous ovarian (LGSOC), or endometrioid endometrial cancer (EEC). J Clin Oncol 2022; 40(suppl_16): Abstr. #5521 18 An Jet al.: Poster Session Efficacy and safety of the anti–PD-L1 monoclonal antibody socazolimab for recurrent or metastatic cervical cancer: Results from the phase I dose-escalation and expansion study. J Clin Oncol 2022; 40(suppl_16): Abstr. #5526 19 Oaknin A et al.: Poster session phase 1 trial of first-line bintrafusp alfa in combination with other anticancer therapies in patients (pts) with locally advanced or advanced cervical cancer. J Clin Oncol 2022; 40(suppl_16): Abstr. #5528 20 González-Martín A et al.: Niraparib in patients with newly diagnosed advanced ovarian cancer. N Engl J Med 2019; 381(25): 2391-402 21 Coleman RL et al.: Veliparib with first-line chemotherapy and as maintenance therapy in ovarian cancer. N Engl J Med 2019; 381(25): 2403-15 22 Ray-Coquard I et al.: Olaparib plus bevacizumab as first-line maintenance in ovarian cancer. N Engl J Med 2019; 381(25): 2416-28
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...