Neue Trends in der Stammzelltransplantation – Update vom ASH 2020
Autorin:
PD Dr. Alexandra Böhm
3. Medizinische Abteilung
Hanusch-Krankenhaus, Wien
E-Mail: alexandra.boehm@oegk.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Bei der 62. Jahrestagung der American Society of Hematology (ASH) 2020 – die erstmals virtuell stattgefunden hat – wurden wieder zahlreiche klinische Studien und Forschungsergebnisse aus dem Bereich der Hämatologie präsentiert. Die neuesten Trends und spannende Entwicklungen aus dem Gebiet der Stammzelltransplantation finden Sie im folgenden Artikel zusammengefasst.
Keypoints
-
Auch bei den Mismatch-Spendern für Patienten, die einer ethnischen Minorität angehören, überzeugt PT-Cy als Immunsuppression.
-
Älteren, fitten Patienten mit High-Risk-MDS und passendem Spender sollte eine allogene SZT nicht vorenthalten werden.
-
Eine ASCT kann bei ALL-Patienten in erster CR mit MRD-Negativität zu vergleichbaren Ergebnissen führen wie die allogene SZT.
-
Ruxolitinib als Zweitlinienbehandlung bei steroidrefraktären oder -abhängigen Patienten mit chronischer GvHD überzeugt mit gutem Ansprechen.
-
Die Rolle der ASCT in der Erstlinienbehandlung beim MM bestätigt sich beim ASH 2020.
-
Der Ernährungszustand und das Mikrobiom sollten neben den Komorbiditäten präTransplantation berücksichtigt werden.
-
Lebenslange Nachsorge für Kinder und Jugendliche nach einer allogenen SZT ist essenziell.
Universaler Spender?
Nicht nur eine Education Session, sondern auch mehrere orale Präsentationen haben sich mit der Frage beschäftigt, ob es möglich wäre, die Verfügbarkeit eines passenden Spenders für eine allogene Stammzelltransplantation (SZT) noch weiter zu steigern, insbesondere für ethnische Minoritäten, die in den üblichen Registern oft nicht gut vertreten sind. Eine dieser Arbeiten war eine prospektive Phase-II-Studie des amerikanischen Stammzellregisters (CIBMTR) an insgesamt 11 Zentren.1 Hier wurden im Zeitraum 2016–2019 ausschließlich Mismatch-Spender mit 1-, 2-, 3- oder 4-Antigen-Mismatches, die üblicherweise nicht erste Wahl sind oder gar nicht zum Einsatz kommen, untersucht – sowohl im myeloablativen (n=40) als auch im dosisreduzierten Setting (n=40), jeweils mit Knochenmark als Stammzellquelle. Die Immunsuppression wurde aus einer Kombination mit Sirolimus/MMF und Post-Transplant-Cyclophosphamid (PT-Cy) durchgeführt. In einer multivariaten Analyse wurden die Ergebnisse mit einer rezenten Kontrollgruppe verglichen, die sich aus unterschiedlichen Spendergruppen zusammensetzte (Mismatch-Spender mit peripheren Stammzellen und Standardimmunsuppression, haploidente Spender mit Knochenmark und peripheren Stammzellen und PT-Cy). Hierbei zeigte sich kein Unterschied im 1-Jahres-Gesamtüberleben (OS), progressionsfreien Überleben (PFS), in der „non-relapse mortality“ (NRM) oder bei akuter Graft-versus-Host-Erkrankung Grad II–IV (GvHD). Daraus kann man schlussfolgern, dass somit auch für Patienten, die über keinen HLA-identen Spender verfügen, mit einem Mismatch-Spender und der hier angewandten Immunsuppression eine SZT sicher durchgeführt werden kann.
Allogene Stammzelltransplantation beim myelodysplastischen Syndrom
Älteren Patienten mit myelodysplastischem Syndrom (MDS) wird eine frühzeitige SZT in der klinischen Routine oftmals nicht angeboten, weil der Vorteil gegenüber anderen Therapien nur in kleinen Studien, die häufig retrospektiv waren, gezeigt werden konnte. Eine multizentrische US-amerikanische Studie untersuchte nun den Nutzen der allogenen SZT in der Altersgruppe der 50- bis 75-jährigen MDS-Patienten.2
Die Studie schloss 384 Patienten mit Hochrisiko-Erkrankung (IPSS Int-2/high-risk) ein. Für 260 Patienten wurde binnen 90 Tagen ein HLA-identer Spender gefunden und dann eine dosisreduzierte SZT durchgeführt, die restlichen 124 Patienten erhielten eine Standardtherapie mit hypomethylierenden Substanzen oder nur „best supportive care“, je nach Zentrum. Bei den Ergebnissen der Überlebensanalysen zeigte sich ein klarer Benefit zugunsten der SZT, die 3-Jahres-OS-Rate im Transplantationsarm lag bei 47,9% vs. 26,6% im Kontrollarm (in allen Subgruppen, auch bei den Patienten >65 Jahre). Kein Unterschied konnte hingegen in der Lebensqualität gefunden werden, die mittels standardisierter Fragebögen erhoben wurde. Das Fazit aus dieser wichtigen Studie ist, dass eine dosisreduzierte SZT allen fitten High-Risk-MDS-Patienten mit passendem Spender angeboten werden sollte.
Autologe versus allogene Transplantation bei der akuten lymphatischen Leukämie
Auch beim heurigen ASH-Meeting waren wieder zahlreiche Studien der EBMT (Europäische Gesellschaft für Stammzelltransplantation) vertreten. Sebastian Giebel aus Polen zeigte einen Vergleich zwischen autologer (ASCT) und allogener SZT bei der akuten lymphatischen Leukämie (ALL) in erster kompletter Remission (CR), wo es für jüngere Patienten bereits vielversprechende Daten zugunsten der ASCT gibt. Hier wurden jetzt retrospektiv ALL-Patienten im Zeitraum zwischen 2000 und 2018 untersucht, die im Median 60 Jahre alt waren, 418 Patienten mit dosisreduzierter SZT (Spender alle HLA-ident) und 142 Patienten mit ASCT.3Die 5-Jahres-OS-Rate zeigte keinen Unterschied, mit 45% bei der ASCT vs. 42% bei der allogenen SZT (p=0,23). Hervorzuheben ist dabei, dass die Konditionierung bei der ASCT hauptsächlich mit einer Ganzkörperbestrahlung (in Kombination mit einer Chemotherapie) durchgeführt wurde und bei 79% der Patienten keine minimale Resterkrankung (MRD) mehr nachweisbar war. Diese beiden Aspekte scheinen wichtig zu sein für eine erfolgreiche ASCT in erster CR bei ALL-Patienten >55 Jahre.
Ruxolitinib bei chronischer Graft-versus-Host-Erkrankung
Für die Behandlung der GvHD steht mit Ruxolitinib (in Kombination mit Steroiden) eine sehr potente Behandlung zur Verfügung, das immunsuppressive Potenzial dieser Substanz wurde bei der akuten GvHD (REACH-1+2-Studie) bereits gezeigt. Jetzt wurde die Substanz auch bei der chronischen GvHD mittels einer großen Phase-III-Studie (REACH3) untersucht.4 Standardbehandlung sind bisher Steroide, allerdings sind 50% der Patienten trotzdem refraktär oder abhängig und es gibt bisher keine einheitlichen, klaren Empfehlungen für die Zweitlinienbehandlung. Für genau diese Patienten (steroidrefraktäre oder -abhängige chronische GvHD-Patienten) wurde die REACH3-Studie designt und nach einer Randomisierung entweder Ruxolitinib in einer Dosierung von 10mg 2 x pro Tag eingesetzt (für 165 Patienten), zusätzlich zur bestehenden Immunsuppression, oder eine andere Zweitlinienbehandlung (insgesamt 10 Optionen, für 164 Patienten). Ruxolitnib wurde für 6 Zyklen à 28 Tage verabreicht, der primäre Endpunkt der Studie war die Gesamtansprechrate (ORR; komplette und partielle Remissionen) nach NIH-Konsensuskriterien am Ende des letzten Zyklus (=Woche 24 nach Therapiebeginn). Die ORR mit Ruxolitinib lag mit 49,7% signifikant höher als im Kontrollarm mit 25,6%, bei einem zu erwartenden Nebenwirkungsprofil (u.a. Hämatotoxizität, erhöhte Lebertransaminasen). Bezüglich der Infektionen war kein Unterschied im klinischen Verlauf zu beobachten, wobei hier für die Details noch die Originalpublikation abzuwarten bleibt. Insgesamt ist die REACH3-Studie aber die erste Phase-III-Studie, die die Überlegenheit einer Zweitlinienbehandlung mit Ruxolitinib bei der chronischen GvHD zeigt.
Autologe Transplantation beim multiplen Myelom
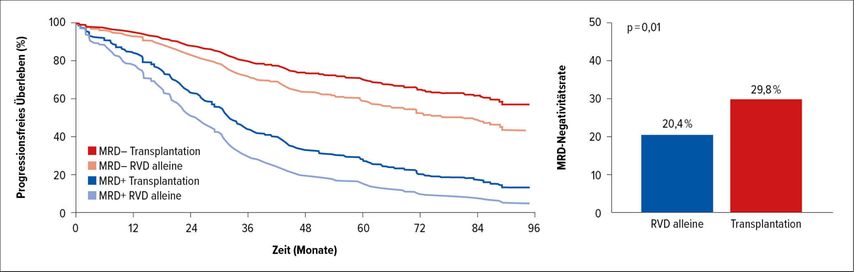
In den letzten Jahren wurden die Notwendigkeit und der optimale Zeitpunkt der ASCT beim multiplen Myelom (MM) in der Erstlinienbehandlung immer wieder infrage gestellt, deswegen wurden beim ASH-Meeting 2020 Langzeitergebnisse der bekannten prospektiv randomisierten IFM-2009-Studie präsentiert (8 Zyklen VRD vs. 3 Zyklen VRD + ASCT + 2 Zyklen VRD-Konsolidierung; 12 Monate Lenalidomid-Erhaltung für beide Gruppen).5 Die erste Interimsanalyse wurde bereits 2017 im NEJM publiziert und zeigte ein signifikant längeres PFS bei der Transplantation (50 vs. 36 Monate). Mittlerweile liegt das Follow-up der Studie bei 9 Jahren. Das PFS bleibt signifikant länger (47,3 vs. 35 Monate), die 8-Jahres-OS-Rate war gleich (62% vs. 60%). Die MRD war ein prognostisch unabhängiger Faktor für das Überleben und interessanterweise erreichen Patienten im Transplantationsarm noch tiefere Remissionen, weil hier die MRD-negativen Patienten ein noch längeres Überleben hatten als die MRD-negativen Patienten im VRD-Arm (Abb. 1). Hier wurden also erneut die Wichtigkeit und Notwendigkeit der ASCT bestätigt.
Abb. 1: Progressionsfreies Überleben in der IFM-2009-Studie nach einem medianen Follow-up von 89,8 Monaten (nach Perrot A et al.)5
Autologe Transplantation beim aggressiven B-Zell-Lymphom
Basierend auf einigen Vorarbeiten hat eine italienische Arbeitsgruppe eine Posterpräsentation einer Studie gezeigt, bei der 63 Patienten >60 Jahre mit aggressivem B-Zell-Lymphom konsolidierend autolog transplantiert wurden.6 65% der Patienten hatten einen „high-intermediate“ oder „high risk international prognostic index“ (IPI). Immunhistochemisch hatten 81% einen „germinal-center B-cell (GCB)-like“ Subtyp, genetisch 34 Patienten ein Double-Hit, 10 Patienten ein Triple-Hit und 19 Patienten ein c-MYC-ICN-B-Zell-Lymphom(ICN=„increased copy numbers“). Die Erstlinientherapie erfolgte mit R-DA-EPOCH. Die ORR lag bei 81% (68% komplette Remission), die 3-Jahres-PFS- und OS-Rate waren 67% und 69%. 10 Patienten waren chemorefraktär und starben letztendlich alle am Lymphom. 24 Patienten (17 in CR, 6 in PR, 1 mit PD) wurden dann Konsolidierung-autolog transplantiert, wobei die ASCT signifikant mit einem längeren Überleben assoziiert war. Die 3-Jahres-PFS- und -OS-Rate waren 100% und 76% für Patienten in CR.
Einfluss von Ernährungszustand und Verlust der Diversität des Mikrobioms auf das Überleben nach einer Stammzelltransplantation
Neben bekannten Faktoren wie z.B. der Intensität der Konditionierung und dem Einfluss des Spenders (haploidenter vs. Geschwister- vs. Fremdspender) auf das Überleben nach einer Stammzelltransplantation wird es immer wichtiger, herauszufinden, wie sich supportive Faktoren wie etwa der Ernährungszustand und das intestinale Mikrobiom auf das Überleben auswirken. Hier wurden bereits zahlreiche Arbeiten zur prognostischen Bedeutung gezeigt, insbesondere gibt es eine Arbeitsgruppe in New York am MSKCC, unter der Leitung von Marcel Van den Brink. Er konnte nachweisen, dass ein Verlust der Diversität des Mikrobioms im Darm einhergeht mit einem kürzeren Überleben aufgrund einer erhöhten TRM. Das gilt nicht nur für die allogene, sondern auch für die autologe Stammzelltransplantation (und wurde ausführlich in einer Education Session am ASH-Meeting 2020 erläutert).
Eine deutsche Arbeit,7 die als Poster präsentiert wurde, untersuchte den Einfluss des Ernährungszustandes von AML-Patienten, die allogen transplantiert wurden.Insgesamt waren es 662 Patienten (medianes Alter 59 Jahre) in CR (68%), CRi (14%), oder mit aktiver Erkrankung (18%). Nach ELN-Kritierien waren 25% „good-“, 30% „intermediate-“ und 45% „high-risk“. Adipöse Patienten (bei Diagnose) hatten eine höhere NRM und kürzeres OS nach der SZT, weiters war ein Gewichtsverlust (∆BMI >–2) zwischen Diagnose und SZT ein unabhängiger Risikofaktor für eine erhöhte NRM und kürzeres OS.
Nachsorge
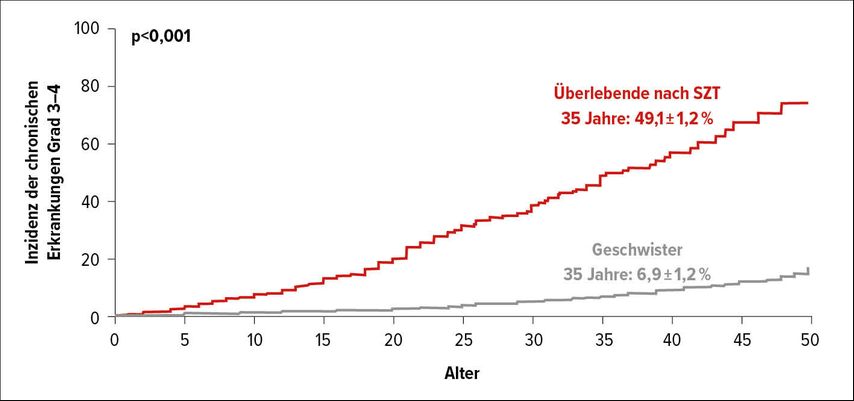
Im Rahmen der BMT Survivor Study (BMTSS) wurden 580 allogen transplantierte junge Erwachsene ≤22 Jahre, die mindestens 2 Jahre post SZT überlebt hatten, nach „chronischen Gesundheitsbeeinträchtigungen“ (CHC) befragt, wie z.B. Diabetes mellitus, Hypertonie, Schilddrüsenerkrankungen etc.8 Diese Ergebnisse wurden dann mit denen ihrer gesunden, unbehandelten Geschwister verglichen. Das mediane Alter zum Zeitpunkt der SZT lag bei 11,5 Jahren, das mediane Follow-up lag bei 10,7 Jahren und die Transplantationen haben zwischen 1974 und 2014 stattgefunden. Die Diagnosen waren ALL (29%), AML/MDS (28%), SAA (13%) und andere (30%). Die Inzidenz der chronischen Erkrankungen vom Grad 3–4lag im 35. Lebensjahr bei den Überlebenden nach SZT signifikant höher als bei den gesunden, unbehandelten Geschwistern (49,1% vs. 6,9%) (Abb. 2). Insbesondere nach einer Ganzkörperbestrahlung war das Risiko deutlich erhöht. Diese Arbeit unterstreicht die Notwendigkeit einer lebenslangen Nachsorge in einer spezialisierten Einrichtung.
Abb. 2: Inzidenz der chronischen Erkrankungen Grad 3–4 in der BMT Survivor Study (BMTSS) (nach Holmqvist AS et al.)8
Literatur:
1 Shaw B et al.: Bridging the gap in access to transplant for underserved minority patients using mismatched unrelated donors and post-transplant cyclophosphamide: A National Marrow Donor Program/Be the Match (NMDP/BTM) Initiative. ASH-Meeting 2020; Abstr. #297 2 Nakamura R et al.: Amulti-center biologic assignment trial comparing reduced intensity allogeneic hematopoietic cell transplantation to hypomethylating therapy or best supportive care in patients aged 50-75 with advanced myelodysplastic syndrome: Blood and Marrow Transplant Clinical Trials Network Study 1102. ASH-Meeting 2020; Abstr. #75 3 Giebel S et al.: Comparison of reduced intensity conditioning - allogeneic hct and autologous hct for elderly patients with acute lymphoblastic leukemia. an analysis from the Acute Leukemia Working Party of the European Society for Blood and Marrow Transplantation. ASH-Meeting 2020; Abstr. #614 4 Zeiser R et al.: Ruxolitinib (RUX) vs best available therapy (BAT) in patients with steroid-refractory/steroid-dependent chronic graft-vs-host disease (cGVHD): Primary findings from the phase 3, randomized REACH3 Study. ASH-Meeting 2020; Abstr. #77 5 Perrot A et al.: Early versus late autologous stem cell transplant in newly diagnosed multiple myeloma: long-term follow-up analysis of the IFM 2009 trial. ASH-Meeting 2020; Abstr. #143 6 Tucci A et al.: Rituximab with dose-adjusted EPOCH (R-DA-EPOCH) with or without autologous stem cell transplantation (ASCT) as first line treatment in patients with aggressive b-cell lymphoma with MYC and BCL-2 and/or BCL-6 gene rearrangements or increase copy number. ASH-Meeting 2020; Abstr. #2131 7 Brauer D et al.: Prognostic impact of nutritional status at diagnosis and weight changes in acute myeloid leukemia patients receiving allogeneic hematopoietic stem cell transplantation. ASH-Meeting 2020; Abstr. #2431 8 Holmqvist AS et al.: Severe/life-threatening/fatal chronic health conditions (CHCs) after allogeneic blood or marrow transplantation (bmt) in childhood – a report from the BMT Survivor Study (BMTSS). ASH-Meeting 2020; Abstr. #69
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...