
Neue Therapiestandards bei Kopf-Hals-Tumoren
Autor:
Assoc. Prof. Priv.-Doz. Dr. Thorsten Füreder
Klin. Abt. für OnkologieUniversitätsklinik für Innere Medizin IAKH Wien/Medizinische Universität Wien
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Auf dem Jahreskongress 2025 der American Society of Clinical Oncology (ASCO) standen im Bereich der Kopf-Hals-Tumoren (KHT) wichtige Studien zu lokal fortgeschrittenen (LA) sowie rezidivierten/metastasierten (r/m) Plattenepithelkarzinomen des Kopf-Hals-Bereichs (HNSCC) und zum Nasopharynxkarzinom (NPC) im Fokus. Insbesondere bei den LA-HNSCC definieren diese Studien den therapeutischen Algorithmus neu; sie werden im folgenden Artikel näher erläutert.
Keypoints
-
Adjuvante Immuntherapie mit Nivolumab plus RCT verlängert das DFS bei resezierten Hochrisiko-LA-HNSCC-Patient:innen und stellt einen neuen Therapiestandard dar.
-
Perioperative Immuntherapie bei resektablen LA-HNSCC-Patienten mit einem PD-L1 CPS ≥1 verlängert das EFS und ist ebenfalls neuer Therapiestandard.
-
Bei r/m HNSCC-Patient:innen mit CPS ≥1 bleibt der Therapiestandard unverändert (Immuntherapie±Chemotherapie); jedoch befinden sich neue, vielversprechende Therapien wie Ficerafusp alfa in fortgeschrittener klinischer Entwicklung.
Lokal fortgeschrittene KHT
NIVOPOSTOP: Immun- plus Radiochemotherapie vs. Radiochemotherapie
Die in der „Plenary Session“ präsentierte randomisierte Phase-III-Studie NIVOPOSTOP evaluierte prospektiv, ob die additive Gabe des PD-1-Inhibitors Nivolumab zur adjuvanten Radiochemotherapie (RCT) nach Resektion eines LA-HNSCC mit hohem Rezidivrisiko das krankheitsfreie Überleben (DFS) verlängern kann.1 Einschlusskriterien umfassten u.a. R1-Resektion, extranodale Ausbreitung (ENE) sowie ≥4 positive Lymphknoten.
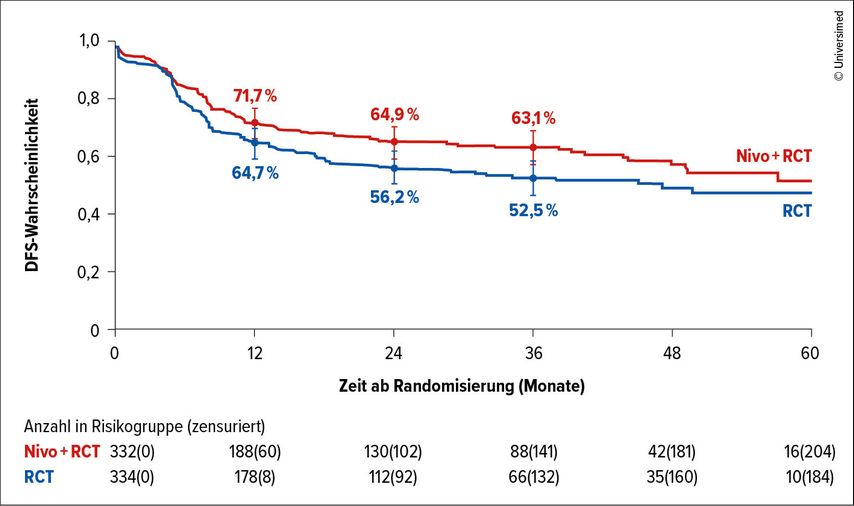
Insgesamt wurden 680 Patient:innen randomisiert. Die kumulative Cisplatin-Dosis ≥200mg/m2 wurde in beiden Armen erreicht (82% bzw. 87%). Der primäre Endpunkt, die 3-Jahres-DFS-Rate, wurde mit Nivolumab signifikant erhöht: 63,1% im experimentellen Arm vs. 52,5% im Standardarm (HR: 0,76; 95% CI: 0,60–0,98; p=0,034; Abb.1). Der DFS-Vorteil zeigte sich konsistent über alle vordefinierten Subgruppen wie PD-L1-Expression oder anatomische Tumorlokalisation hinweg. Es sei jedoch erwähnt, dass die Aussage bei p16-positiven Oropharynxkarzinomen aufgrund der geringen Patient:innenanzahl (jeweils 5%) limitiert ist.
Abb. 1: Krankheitsfreies Überleben (DFS) unter postoperativem Nivolumab (Nivo) plus Radiochemotherapie (RCT, rot) vs. RCT alleine (blau) (modifiziert nach Bourhis J et al.)1
Die Rate lokoregionärer Rückfälle war unter Nivolumab reduziert (HR: 0,63; 95% CI: 0,42–0,94). Die Gesamtüberlebensdaten (OS)waren noch unreif, zeigten aber einen positiven Trend nach drei Jahren (74% vs. 67,8%). Wie erwartet erhöhte die Zugabe von Nivolumab die Rate an Langzeitnebenwirkungen moderat (34,6% vs. 31%).
KEYNOTE-689: perioperative Immuntherapie vs. sofortige Operation
Die randomisierte Phase-III-Studie KEYNOTE-689 evaluierte, ob eine perioperative Immuntherapie mit Pembrolizumab im Vergleich zur Standardtherapie (Operation gefolgt von R[C]T) bei resektablem LA-HNSCC das ereignisfreie Überleben (EFS) verlängert.2,3 Patient:innen im experimentellen Arm erhielten zwei Zyklen Pembrolizumab vor kurativer Tumorresektion und jeweils zusätzlich für drei Zyklen zur standardisierten Radiotherapie plus/minus Chemotherapie gefolgt von zwölf Zyklen Pembrolizumab Erhaltungstherapie.
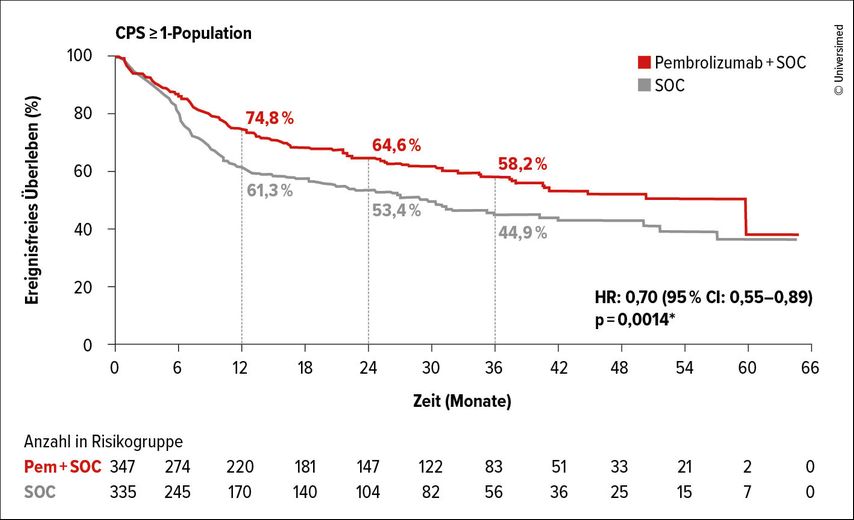
Insgesamt wurden 714 Patient:innen randomisiert. Bereits am AACR-Kongress wurde gezeigt, dass das EFS signifikant zugunsten des Pembrolizumab-Arms in allen prädefinierten PD-L1-Gruppen verlängert wurde (CPS ≥1: HR: 0,68; CPS ≥10: HR: 0,64; Abb.2). Das mediane EFS in der Gesamtpopulation betrug 51,8 Monate vs. 30,4 Monate.
Abb. 2: Ereignisfreies Überleben (EFS) bei Gabe von perioperativem Pembrolizumab (Pembro, rot) vs. sofortige Operation („standard of care“, SOC, grau) in der CPS-≥1-Population (modifiziert nach Adkins D et al.)2
Ein weiteres zentrales Ergebnis war die Erhöhung der Raten des pathologischen Ansprechens im neoadjuvanten Setting: Eine „major pathologic response“ (MPR) wurde bei 9,3% der Patient:innen im Pembrolizumab-Arm beobachtet. Eine pathologische Komplettremission (pCR) wurde bei 3% erreicht.
Auch das fernmetastasenfreie Überleben (DMFS) wurde verlängert: Es lag bei median 51,8 Monaten unter Pembrolizumab vs. 35,7 Monate im Kontrollarm (HR: 0,66; 95% CI: 0,50–0,87). Die kumulative Inzidenz lokoregionärer Rückfälle war vergleichbar.
Zudem zeigte sich eine Reduktion sekundärer Malignome: 2,5% im Pembrolizumab-Arm vs. 5,1%. Das Sicherheitsprofil war insgesamt beherrschbar. Immunvermittelte Nebenwirkungen traten erwartungsgemäß häufiger unter Pembrolizumab auf.
Abschließend sei erwähnt, dass in beiden Studienarmen bei rund 88% der Patient:innen eine chirurgische Resektion durchgeführt wurde – ein Hinweis darauf, dass die perioperative Immuntherapie die Operabilität nicht beeinträchtigte und auch in dieser Hinsicht als sicher gelten kann.
Relevanz für die klinische Praxis
Trotz multimodaler Therapieansätze hat sich das Langzeit-Outcome bei LA-HNSCC über zwei Dekaden kaum verbessert. Ein zentrales klinisches Problem bleibt die hohe Rezidivrate von bis zu 50% nach kurativer Resektion mit adjuvanter R(C)T oder definitiver Radiochemotherapie.
Die NIVOPOSTOP-Studie zeigt nun erstmals einen signifikanten DFS-Vorteil durch die additive Gabe von Nivolumab im postoperativen Hochrisiko-Setting – und definiert damit gemeinsam mit KEYNOTE-689 einen potenziellen neuen Standard.
Für Patient:innen nach Resektion mit R1-Status oder ENE sollte die Immunaddition im klinischen Alltag ernsthaft in Erwägung gezogen werden. Besonders relevant ist dies vor dem Hintergrund, dass andere Studien, die Immuntherapie in postoperative Konzepte integrieren wollten – wie etwa IMvoke010 –, keinen Vorteil zeigen konnten.
Offen bleibt, ob p16-positive Oropharynxkarzinome, die in der klinischen Routine häufig primär mittels definitiver RCT behandelt werden, in gleichem Maße von einer adjuvanten Immuntherapie profitieren. Ebenso ist unklar, ob Patient:innen mit intermediärem Risiko – etwa mit mehr als vier befallenen Lymphknoten, jedoch laut ESMO-Leitlinien ohne klare Indikation für eine adjuvante R(C)T – in zukünftige Strategien aufgenommen werden sollten. Diese Subgruppe machte nur etwa 10% der Studienpopulation pro Arm aus. Eine Zulassung für Nivolumab in dieser Indikation wurde beantragt.
Im Gegensatz zu rein adjuvanten Strategien verfolgt KEYNOTE-689 ein perioperatives Konzept mit neoadjuvanter und adjuvanter Immuntherapie. Aus biologischer Perspektive könnte insbesondere die neoadjuvante Gabe aufgrund intakter Tumorstruktur und Immunmikromilieu eine stärkere systemische Immunaktivierung bewirken als eine rein postoperative Behandlung. Die Studie adressiert zudem eine breitere Population als NIVOPOSTOP: Patient:innen mit „Up-front“-ENE waren jedoch in KEYNOTE-689 explizit ausgeschlossen.
Aufgrund des signifikanten Vorteils im EFS – einem in Metaanalysen validierten Surrogatmarker für das OS – ist aus Sicht des Autors ein Abwarten der finalen OS-Daten nicht erforderlich. Der Befund, dass postoperativ weniger Hochrisikopatient:innen im Pembrolizumab-Arm verblieben, legt zusätzlich einen substanziellen neoadjuvanten Effekt nahe.
Dennoch bleiben offene Fragen: So zeigte sich in der Subgruppe mit Hypopharynxkarzinom kein klarer Effekt, und für p16-positive Oropharynxkarzinome und Tumoren mit CPS=0 ist die klinische Relevanz der Immunaddition ebenfalls ungewiss. Darüber hinaus stellt sich perspektivisch die Frage, ob chirurgische Resektionsgrenzen zukünftig immunologisch neu definiert werden könnten – derzeit orientiert sich das operative Vorgehen jedoch weiterhin an den etablierten Standards.
Logistisch ist das perioperative Konzept komplexer als eine rein postoperative Immuntherapie und erfordert eine enge interdisziplinäre Abstimmung. Dennoch stellt KEYNOTE-689 aus Sicht des Autors das derzeit bevorzugte Behandlungsprinzip dar und definiert einen neuen „standard of care“. Eine Zulassung in Österreich wird im Herbst 2025 erwartet; in den USA wurde Pembrolizumab bereits durch die FDA in dieser Indikation zugelassen.
HNSCC im rezidivierten/metastasierten Stadium
Ficerafusp alfa in Kombination mitPembrolizumab in der Erstlinie
Auf dem ASCO-Jahrestreffen 2025 wurden aktualisierte Daten einer Expansionskohorte der multizentrischen Phase-I/Ib-Studie zu Ficerafusp alfa in Kombination mit Pembrolizumab als Erstlinientherapie bei Patient:innen mit r/m HNSCC vorgestellt.4 Die Analyse fokussierte auf eine biomarkerdefinierte Subgruppe mit HPV-negativem Tumorstatus und CPS ≥1. Ficerafusp alfa (vormals BCA101) ist ein bifunktionaler EGFR/TGF-β-Antikörper.
In Kombination mit Pembrolizumab zeigte sich eine objektive Ansprechrate (ORR) von 54%, wobei 21% der Patient:innen eine komplette Remission erreichten. Das OS wurde mit 21,3 Monaten berichtet – ein für diese Population bemerkenswert langer Zeitraum. Die Kombinationstherapie war insgesamt gut verträglich.
Nasopharynxkarzinom: rezidiviertes/metastasiertes Stadium
Becotatug Vedotin bei vorbehandeltem nasopharyngealem Karzinom
In dieser randomisierten Phase-I/II-Studie wurde das Antikörper-Wirkstoff-Konjugat (ADC) Becotatug Vedotin bei Patient:innen mit Platin- und Immuntherapievorbehandeltem r/m NPC evaluiert. Becotatug Vedotin ist ein ADC, das sich gegen EGFR richtet.5
Insgesamt wurden 173 Patient:innen randomisiert und Becotatug Vedotin wurde mit Chemotherapie (Docetaxel und Capecitabin) verglichen. Die primären Endpunkte waren ORR und PFS. Die ORR betrug 30,2% im experimentellen Arm vs. 11,5% in der Chemotherapie-Gruppe. Das PFS lag bei 5,8 Monaten gegenüber 2,8 Monaten. Das Sicherheitsprofil war konsistent mit anderen Vedotin-basierten ADC.
Relevanz für die klinische Praxis
Ficerafusp alfa zeigt in Kombination mit Pembrolizumab eine höhere ORR und ein längeres OS, als in der bisher etablierten Standardtherapie der KEYNOTE-048-Studie beobachtet wurde.6 Auch wenn diese Daten aus einer frühen Phase stammen, ist die Aktivität bemerkenswert. Für die klinische Routine ist Ficerafusp derzeit noch nicht bereit – allerdings läuft aktuell die randomisierte Phase-II/III-Zulassungsstudie Fortifi-HN01 (NCT06788990). Ein positiver Ausgang dieser Studie könnte einen neuen Meilenstein in der Erstlinientherapie des r/m HNSCC markieren. Die Therapie des vorbehandelten r/m NPC stellt weiterhin eine Herausforderung dar – auch wenn es sich in Österreich um eine seltene Tumorentität handelt. Nach Versagen einer platinhaltigen Chemotherapie plus Immuncheckpoint-Inhibition stehen bislang nur konventionelle Zytostatika zur Verfügung. Die Daten zur Wirksamkeit von Cetuximab in dieser Situation sind limitiert, sodass der Einsatz eines EGFR-targeted ADC wie Becotatug Vedotin ein innovativer und potenziell paradigmatischer Ansatz ist – möglicherweise auch über das NPC hinaus. Derzeit ist Becotatug in Europa jedoch nicht verfügbar.
Zusammenfassung
Kurz zusammengefasst lassen sich aus den in diesem Jahr präsentierten Studien bei KHT folgende Erkenntnisse ableiten:
-
Adjuvante Immuntherapie mit Nivolumab plus RCT verlängert das DFS bei Hochrisiko-LA-HNSCC-Patient:innen nach Resektion und stellt einen neuen Therapiestandard dar.
-
Perioperative Immuntherapie mit einem PD-L1-CPS ≥1 bei LA-HNSCC-Patient:innen, bei denen eine Resektion möglich ist, verlängert das EFS und ist ebenfalls neuer Therapiestandard.
-
Bei r/m HNSCC-Patient:innen mit CPS ≥1 bleibt der Therapiestandard unverändert (Immuntherapie±Chemotherapie); jedoch befinden sich neue, vielversprechende Therapien wie Ficerafusp alfa in fortgeschrittener klinischer Entwicklung.
Literatur:
1 Bourhis J et al.: NIVOPOSTOP (GORTEC 2018-01): Aphase III randomized trial of adjuvant nivolumab added to radio-chemotherapy in patients with resected head and neck squamous cell carcinoma at high risk of relapse. JClin Oncol 2025; 43(Suppl.17): #LBA2 2 Adkins D et al.: Neoadjuvant and adjuvant pembrolizumab plus standard of care (SOC) in resectable locally advanced head and neck squamous cell carcinoma (LA HNSCC): exploratory efficacy analyses of the phase 3 KEYNOTE-689 study. JClin Oncol 2025; 43(Suppl.16): #6012 3 Uppaluri R et al.: Neoadjuvant and adjuvant pembrolizumab in locally advanced head and neck cancer. N Engl J Med 2025; 393(1): 37-50 4 Chung CH et al.: Ficerafusp alfa with pembrolizumab in patients with recurrent or metastatic head and neck squamous cell carcinoma: updated results from an expansion cohort of an open-label, multicenter, phase 1/1b trial. J Clin Oncol 2025; 43(Suppl.16): 6017 5 Han F et al.: Becotatug vedotin vs. chemotherapy in pre-heavily treated advanced nasopharyngeal carcinoma: a randomized, controlled, multicenter, open-label study. J Clin Oncol 2025; 43(Suppl.17): #LBA6005 6 Burtness B et al.: Pembrolizumab alone or with chemotherapy vs. cetuximab with chemotherapy for recurrent or metastatic squamous cell carcinoma of the head and neck (KEYNOTE-048): a randomised, open-label, phase 3 study. Lancet 2019; 394(10212): 1915-28
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...
%20bei%20Gabe%20von%20perioperativem%20Pembrolizumab%20(Pembro,%20rot)%20vs.jpg)


