Neue Standards: CPI, ADC und EV
Bericht:
Dr. med. Judith Moser
Autorin:
Priv.-Doz. Dr. med. Maria De Santis
Sektion interdisziplinäre Urologische Onkologie, Charité Universitätsmedizin Berlin
E-Mail: maria.de-santis@charite.de
Die Erstlinientherapie des lokal fortgeschrittenen oder metastasierten Urothelkarzinoms konnte durch die Phase-III-Studien EV-302/KEYNOTE-A39 und CheckMate 901 revolutioniert werden. Allerdings erfordert die Behandlung mit dem Antikörper-Wirkstoff-Konjugat Enfortumab Vedotin ähnlich wie jene mit Checkpoint-Inhibitoren ein sorgfältiges Nebenwirkungsmanagement.
Nachdem die systemische Therapie des metastasierten Urothelkarzinoms (mUC) jahrzehntelang nur Chemotherapien beinhaltet hatte, bereichert seit 2016 eine wachsende Zahl an neuen Optionen wie Checkpoint-Inhibitoren (CPI) und Antikörper-Wirkstoff-Konjugaten (ADC) die Therapielandschaft. Mit dem ADC Enfortumab Vedotin (EV) konnte in der Erstlinientherapie des mUC auf der Basis der randomisierten Phase-III-Studie EV-302/KEYNOTE-A39 ein neuer Standard etabliert werden.
In EV-302/KEYNOTE-A39 erhielten platinfitte Patient:innen mit lokal fortgeschrittenem/metastasiertem UC entweder EV plus Pembrolizumab (n=442) oder Cisplatin bzw. Carboplatin plus Gemcitabin über sechs Zyklen (n=444).1 Pembrolizumab wurde für maximal 35 Zyklen verabreicht, während EV bis zur Progression zur Anwendung gelangte. Progressionsfreies Überleben (PFS) und Gesamtüberleben (OS) bildeten den dualen primären Endpunkt.
Nie dagewesener OS-Benefit
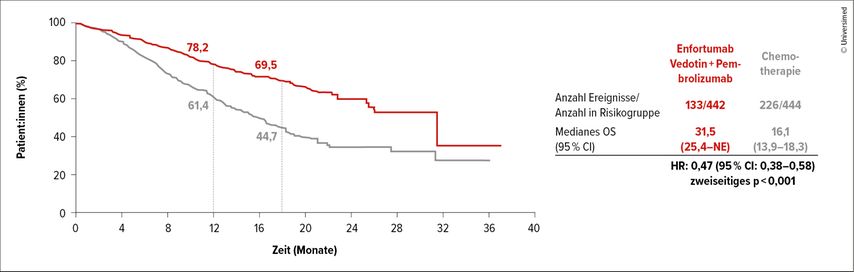
EV plus Pembrolizumab bewirkte gegenüber der Chemotherapie Verdopplungen des PFS (12,5 vs. 6,3 Monate; HR: 0,45; p<0,001) sowie des OS (31,5 vs. 16,1 Monate; Abb. 1) mit einer Mortalitätsreduktion um 53% (HR: 0,47; p<0,001).1 Bei der Präsentation der Studiendaten am ESMO-Kongress 2023 wurde der noch nie dagewesene OS-Vorteil mit stehenden Ovationen begrüsst. Die Gesamtansprechraten beliefen sich auf 67,7% vs. 44,4% (p<0,001), und in 29,1% vs. 12,5% erzielten die Patient:innen Komplettremissionen.
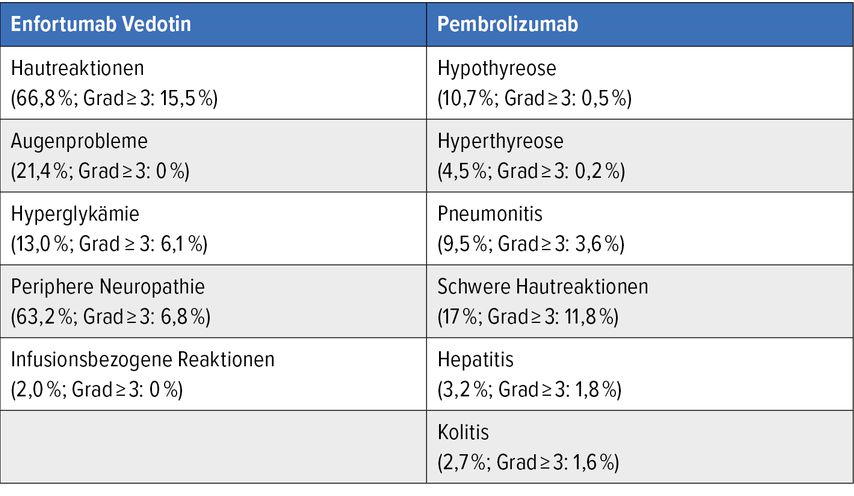
Die EV-Therapie geht mit einem typischen Nebenwirkungsspektrum einher, das Hautreaktionen, okuläre Probleme, Hyperglykämie, periphere Neuropathie und infusionsbezogene Reaktionen umfasst (Tab. 1). Durch die Kombination mit Pembrolizumab ergibt sich eine Überschneidung im Bereich der Hautreaktionen, die auch Teil des bekannten CPI-Nebenwirkungsprofils sind.
Tab. 1: Unerwünschte Ereignisse von besonderem Interesse in der Studie EV-302/KEYNOTE-A39 (modifiziert nach Powles T et al.)1
Als allgemeine Massnahmen zur Hintanhaltung dermatologischer Nebenwirkungen sollten den Patient:innen Schutz vor Sonneneinstrahlung, hypoallergene Hautpflegeprodukte, tägliche prophylaktische Anwendung sanfter, unparfümierter Feuchtigkeitscremes und das Vermeiden von heissen Bädern und heissen Duschen (speziell bei Vorhandensein von Juckreiz) empfohlen werden. Bei Augenproblemen wirkt die Verwendung eines künstlichen Tränenersatzes unterstützend.
Hinsichtlich des Hyperglykämierisikos empfehlen sich eine ausgewogene Ernährung und körperliche Betätigung; bei klinischer Indikation sollen Blutzucker-Selbstmessungen und eine medikamentöse Einstellung erfolgen. Zu den Risikofaktoren für die Entwicklung einer Hyperglykämie zählen Adipositas und ein manifester Diabetes mellitus.
Management von Nebenwirkungen
EV-assoziierte dermatologische Manifestationen können Alopezie ebenso beinhalten wie Stomatitis, makulopapulöse Ausschläge, Hyperpigmentation und Blasenbildung.2 Bullöse Läsionen sollten zur stationären Aufnahme und Beobachtung Anlass geben, um ein Stevens-Johnson-Syndrom (SJS) bzw. eine toxische epidermale Nekrolyse (TEN) auszuschliessen.
Im Fall der Bestätigung einer dieser Diagnosen ist die Behandlung dauerhaft abzubrechen. Allgemein wird bei Hautreaktionen im Fall einer Verschlechterung von Grad-2-Läsionen oder Auftreten von Fieber bei Grad-2- oder Grad-3-Manifestationen ein Behandlungsstopp bis zur Rückbildung auf Grad ≤1 empfohlen. Diese Patient:innen werden an unserer Abteilung stationär beobachtet; auf jeden Fall ist eine dermatologische Begutachtung indiziert. Die Dosis kann bei Grad-2-Läsionen beibehalten werden, während ich bei Grad 3 eine Reduktion auf die nächste Stufe empfehle. Ausgehend von der Anfangsdosis von 1,25mg/kg (maximal 125mg) sind drei Reduktionen in 0,25-mg-Schritten möglich.
Bei Hyperglykämie mit Werten >250mg/dl soll die Gabe von EV bis zum Absinken auf ≤250mg/dl unterbrochen werden, anschliessend kann die Weiterbehandlung mit der gleichen Dosis erfolgen. Erfahrungsgemäss sind nach der Blutzuckereinstellung häufig Dosisreduktionen notwendig.
Pneumonitiden/interstitielle Lungenerkrankungen erfordern ab Grad 3 ein dauerhaftes Absetzen; bei Grad 2 soll die Therapie bis zur Rückbildung auf Grad ≤1 unterbrochen werden. In der Folge ist entweder eine Beibehaltung der Dosis oder eine Reduktion um eine Stufe möglich.
Eine periphere Neuropathie Grad 2 soll zu einer Therapiepause bis Grad ≤1 Anlass geben. Beim erstmaligen Auftreten wird die Behandlung mit der gleichen Dosis fortgesetzt, bei erneuter Manifestation mit reduzierter Dosis. Neuropathien der Grade ≥3 erzwingen eine dauerhafte Beendigung der Behandlung. Grundsätzlich besteht das Ziel darin, die Patient:innen mithilfe von Dosisreduktionen auf der Therapie zu halten, wobei Lebensqualität und Funktionalität nicht leiden sollen.
Änderungen im Algorithmus
Als zweite positive Erstlinienstudie wurde am ESMO-Kongress 2023 CheckMate 901 vorgestellt, die ausschliesslich cisplatinfitte Patient:innen rekrutierte.3
Randomisiert kamen entweder Nivolumab plus sechs Zyklen Cisplatin/Gemcitabin oder nur die Chemotherapie zum Einsatz. Nivolumab wurde im Prüfarm während der Kombinationsphase dreiwöchentlich und danach als Monotherapie alle vier Wochen über bis zu 24 Monate verabreicht.
Auch CheckMate 901 erbrachte eine signifikante OS-Verlängerung im experimentellen Arm, wenngleich diese mit 21,7 vs. 18,9 Monate (HR: 0,78; p=0,02) nicht so spektakulär ausfiel wie jene in EV-302/KEYNOTE-A39. Ein Ansprechen wurde bei 57,6% vs. 43,1% dokumentiert.
Somit hat die «alte» klinische Praxisleitlinie der ESMO zur Therapie des Blasenkarzinoms, die als Standard-Erstlinientherapie Cisplatin oder Carboplatin plus Gemcitabin gefolgt von einer Avelumab-Maintenance empfahl, ausgedient.4 Hier fand EV erst in der Drittlinie Erwähnung. Nun stellt die Kombination aus EV und Pembrolizumab die Erstlinienstrategie der Wahl für alle Patient:innen dar, die eine ausreichende Fitness für eine Chemo- und CPI-Therapie aufweisen (Evidenzlevel I, A).5
Falls zu dieser Behandlungsoption kein Zugang besteht oder Kontraindikationen vorliegen, empfiehlt die neue Richtlinie bei Cisplatin-Eligibilität die Kombination aus Nivolumab und Cisplatin/Gemcitabin (I,A). Carboplatinfitte Patient:innen können Carboplatin/Gemcitabin gefolgt von Avelumab erhalten (I, A).
Für die Sequenztherapie nach Eintreten einer Progression unter EV/Pembrolizumab liegen derzeit erst wenige Daten vor. Es empfiehlt sich jedoch, bereits während der Erstlinientherapie eine Gensequenzierung und erweiterte Diagnostik mit Bestimmung relevanter Alterationen (z.B. FGFR, HER2) durchzuführen, um die nachfolgenden Optionen zeitgerecht festlegen zu können.
Literatur:
1 Powles T et al.: Enfortumab vedotin and pembrolizumab in untreated advanced urothelial cancer. N Engl J Med 2024; 390(10): 875-88 2 Lacouture ME et al.: Management of dermatologic events associated with the nectin-4-directed antibody-drug conjugate enfortumab vedotin. Oncologist 2022; 27(3): e223-32 3 Van der Heijden MS et al.: Nivolumab plus gemcitabine-cisplatin in advanced urothelial carcinoma. N Engl J Med 2023; 389(19): 1778-89 4 Powles T et al.: Bladder cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol 2022; 33(3): 244-58 5 Powles T et al.: ESMO Clinical Practice Guideline interim update on first-line therapy in advanced urothelial carcinoma. Ann Oncol 2024; 35(6): 485-90
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...