Nachsorge nach Brustkrebserkrankung: wie lange, wie häufig, womit?
Autorin:
Dr. med. Katrin Breitling
Leiterin Brustzentrum Schaffhausen-Wetzikon
Leitende Ärztin Frauenklinik, Spitäler Schaffhausen
E-Mail: Katrin.Breitling@spitaeler-sh.ch
Die Zahl der Menschen, die nach der Primärbehandlung geheilt oder in langer Remission sind, nimmt stetig zu. Ursache hierfür sind der demografische Wandel und die wachsende Wirksamkeit onkologischer Therapien. Die Frage ist, ob die starre und strukturierte Nachsorge immer noch aktuell ist und ob sie den Bedürfnissen der «cancer survivors» gerecht wird.
Brustkrebs ist nach wie vor die häufigste Krebserkrankung der Frau. Damit steigt die Zahl der Patientinnen, welche einer Tumornachsorge bedürfen, stetig an. Die Tumornachsorge beginnt nach Abschluss der Primärbehandlung mit Operation, Radiotherapie und adjuvanter Chemo- oder Antikörpertherapie, sofern indiziert. Nach einer brusterhaltenden Operation mit Radiotherapie muss in etwa 10% der Fälle mit einem lokoregionären Rezidiv innerhalb von 5 Jahren gerechnet werden.1 Etwa 40% aller isolierten Lokalrezidive werden im Rahmen der Nachsorgeuntersuchung erkannt.2
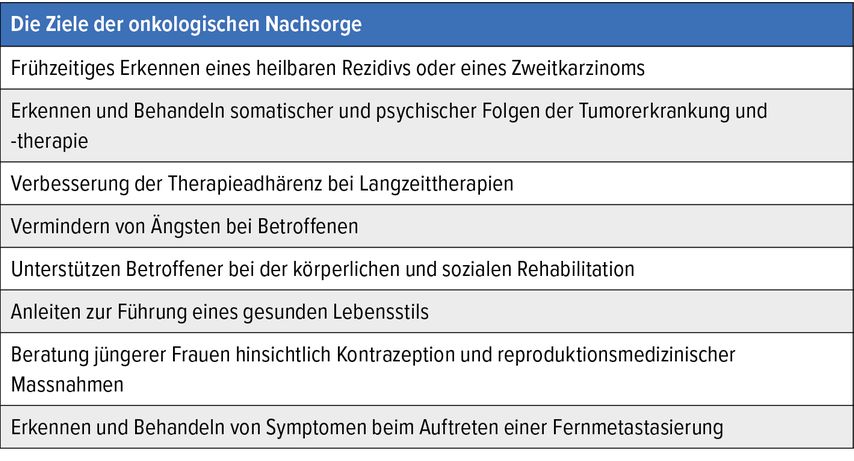
Ziele der onkologischen Nachsorge
Nach erfolgter Primärtherapie kann es Beschwerden geben, welche im unmittelbaren zeitlichen Zusammenhang mit der Behandlung stehen. Das sind z.B. Wundheilungsstörungen nach Operationen, Geschmacksstörungen als Folge der Chemotherapie oder Hautveränderungen im Rahmen der Bestrahlung. Auftretende Spät- oder Langzeitfolgen der durchgeführten Therapie gilt es jedoch ebenso zu erkennen. Zudem erhöht eine Brustkrebserkrankung das Risiko für die Entwicklung von Depressionen und Angststörungen um den Faktor 1,5, sodass hier eine psychoonkologische Betreuung grosszügig angeboten werden sollte.3
Die Ziele der onkologischen Nachsorge sind in Tabelle 1 zusammengefasst. Vor allem die Beratung Betroffener hinsichtlich Führung des Lebensstils, der Familienplanung und Inanspruchnahme weiterer Vorsorgeuntersuchungen ist individuell und zeitintensiv. In die Empfehlungen der aktuellen S3-Leitlinie zur Nachsorge hielt dieser Umstand bereits Einzug.
Modifikation des Lebensstils
Mit neuen Therapiemethoden treten auch neue, bis anhin weniger bekannte, therapiebedingte Nebenwirkungen, Begleiterscheinungen oder Beschwerden auf. Lymphödeme im Bereich der Arme sind nach der Reduktion der Ausdehnung der Axillaoperationen viel seltener geworden und liegen bei alleiniger Entfernung der Sentinellymphknoten nur noch bei etwa 8%.4
Lymphödeme im Bereich der Brust können auftreten, sind jedoch manchmal schwer von Lokalrezidiven oder einem inflammatorischen Mammakarzinom zu unterscheiden. Eine umfassende Diagnostik mit Biopsie ist dann zur Diagnosesicherung unumgänglich. Radiogene Schäden, wie zum Beispiel eine radiogene Pneumopathie, treten subakut als Pneumonitis auf. Diese manifestiert sich mit einer Latenz von vier bis zwölf Wochen nach Abschluss der Bestrahlung.5 Im Verlauf kann sie in eine Fibrose übergehen.
Neben Organtoxizitäten als Folge einer Chemotherapie mit peripherer Neuropathie, kardialen Komplikationen oder kognitiven Dysfunktionen können neu auch Endokrinopathien wie zum Beispiel eine Hypothyreose oder Hypophysitis und Spätkomplikationen wie eine Hepatitis und Pneumonitis unter der Therapie mit Immuncheckpoint-Inhibitoren auftreten.6
Einen wesentlichen Faktor zur Reduktion der Rückfallrate stellt die Sicherung der Therapieadhärenz bei Langzeitbehandlungen dar. Dabei können bereits adjuvante Behandlungen mit Antikörpern bei einer HER2-Protein-Überexpression oder die Therapie mit PARP-Inhibitoren bei BRCA-Genträgern eine Herausforderung bei der Motivation Betroffener zur Durchführung der Behandlung darstellen. Je nach Risikoprofil wird eine adjuvante endokrine Therapie über 5 bis 10 Jahre empfohlen. Bereits 30 bis 50% der Patientinnen nehmen jedoch schon im ersten Jahr die endokrine Therapie nicht mehr konsequent ein.7 Vor allem jüngere Frauen beenden die endokrine Therapie aufgrund der Nebenwirkungen vorzeitig. Wiederholte Aufklärungen, empathische Gespräche unter Einbezug der Breast Care Nurses und der Zugang zu komplementärmedizinischen Behandlungen im Sinne einer integrativen Onkologie können helfen, Betroffene bei der Anwendung der onkologischen Therapien zu unterstützen.8 Auch die Visualisierung des individuellen Rückfallrisikos zur Abschätzung einer erweiterten endokrinen Therapie über 5 Jahre hinaus anhand des CTS-5-Calculators kann zur Verbesserung der Therapieadhärenz beitragen.9
In den letzten Jahren häufen sich die Erkenntnisse, dass Modifikationen des Lebensstils nicht nur zur Verbesserung der Lebensqualität unter laufender Therapie führen, sondern auch die Prognose nach einer Brustkrebserkrankung verbessern. Diese Erkenntnisse sind in die aktuellen Empfehlungen der Arbeitsgruppe Gynäkologische Onkologie (AGO) 2021 eingegangen. Nächtliches Fasten von mindestens 13 Stunden reduziert das Rezidivrisiko um bis zu 36%.10
Braucht es eine individualisierte Nachsorge?
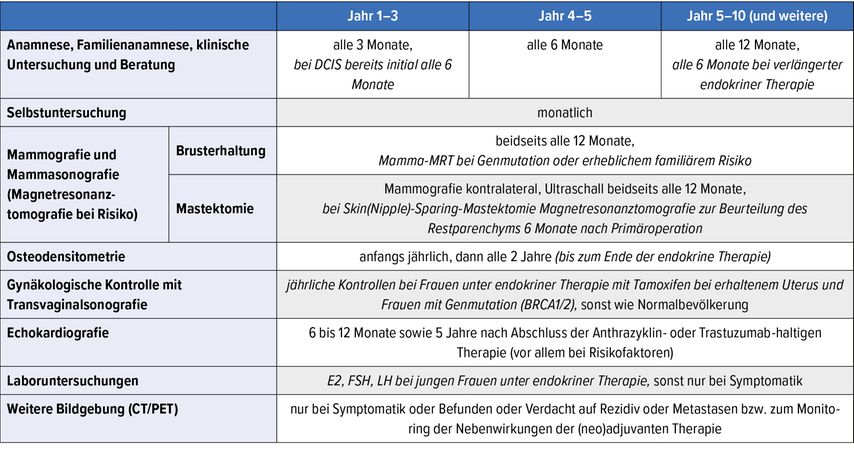
Das relative tumorspezifische Überleben ist auch abhängig vom molekularen Subtyp, von der Tumorgrösse und der Anzahl befallener Lymphknoten bei der Erstdiagnose. Therapieentscheide, vor allem bei der Behandlung von Brustkrebs, werden aufgrund der Tumorbiologie und der daraus resultierenden Risikostratifizierung im Rahmen der Tumorkonferenz bereits sehr individuell getroffen. Es stellt sich somit die Frage, ob nicht auch eine individualisierte risikoadaptierte Nachsorge notwendig wäre (Tab. 2). Valide Studien, die eine individualisierte risikoadaptierte Nachsorge untersucht haben, fehlen aber. Zudem müssten diese über einen sehr langen Zeitraum erfolgen.11
Tab. 2: Tumornachsorge. Kursiv gedruckt sind individualisierte Untersuchungen gemäss Risikoprofil und Lebensalter (adaptiert nach AGO 2021, S3-Leitlinie 2021, ESMO 2019)10, 11, 14
Kriterien zur Modifikation der bis dato etablierten strukturierten Nachsorge fehlen weitgehend und die zeitliche Begrenzung der Nachsorge auf einen Zeitraum von fünf Jahren bei unterschiedlichen Risikokonstellationen ist nicht mehr ausreichend.11
Für junge Frauen sind neben der Therapie des Mammakarzinoms auch Kontrazeption sowie eine allfällige Familienplanung zu berücksichtigen. Hier stehen Möglichkeiten prätherapeutischer reproduktionsmedizinischer Massnahmen wie der Asservierung von Eizellen oder der Entnahme von Ovarialgewebe zur Verfügung, vor allem dann, wenn sich die Patientinnen einer Chemotherapie unterziehen müssen.
Da jedoch auch bei jungen Frauen hormonsensible Tumoren auftreten, welche endokrin behandelt werden, stellt sich die Frage, wann die Frauen die Familienplanung realisieren können, wenn die endokrine Therapie zum Teil bis zu zehn Jahre umfasst. Bis anhin weiss man von retrospektiven Studien, dass Schwangerschaften keine negativen Auswirkungen auf die Prognose des Mammakarzinoms haben.12 Weitere Informationen werden von der prospektiv angelegten POSITIVE-Studie erwartet.
Der Einfluss zirkulierender Tumorzellen (CTC) im peripheren Blut und disseminierter Tumorzellen (DTC) im Knochenmark sind beim Mammakarzinom validiert und haben prognostische Bedeutung. So stellt eine CTC-Positivität einen ungünstigen Prognosefaktor dar.13 Eine individualisierte Biomarkerbestimmung wird in der Nachsorge jedoch noch nicht generell empfohlen.10 Die genauere Charakterisierung der zirkulierenden Tumorzellen kann aber in Zukunft zu einer Abschätzung des Metastasierungsrisikos führen.
Fazit für die Praxis
-
Der Zeitraum der Tumornachsorge von fünf Jahren scheint vor dem Hintergrund verlängerter Behandlungen und individualisierter Risiken zu kurz und sollte auf zehn Jahre verlängert werden.
-
Initial sollte die Tumornachsorge während der ersten zwei Jahre alle drei Monate erfolgen, um frühzeitig therapiebedingte Nebenwirkungen zu erkennen und die Therapieadhärenz zu erhöhen. Bei reinem duktalem Carcinoma in situ (DCIS) genügt von Beginn an die halbjährliche Kontrolle.
-
Im Rahmen der Konsultation erfolgt die klinische Untersuchung des Körpers einschliesslich der Brustuntersuchung. Zudem sollte für die Tumornachsorge ausreichend Konsultationszeit eingerechnet werden, um Anliegen, Sorgen und Ängste der Betroffenen aufzufangen.
-
Trotz erhöhter Rate an Wiedereinbestellungen und Biopsien empfehlen die meisten Guidelines neben der jährlichen Mammografie auch die Durchführung der simultanen Mammasonografie. Die Magnetresonanztomografie der Brust ist bei speziellen Risikokonstellationen wie zum Beispiel bei Genmutationsträgerinnen Methode der Wahl.
Literatur:
1 Anderson SJ et al.: Prognosis after ipsilateral breast tumor recurrence and locoregional recurrences in patients treatead by breast-conserving therapy in five national surgical adjuvant breast and bowel project protocols of node-negative breast cancer. J Clin Oncol 2009; 27 (15): 2466-73 2 De Bock GH et al.: Effectiveness of routine visits and routine tests in detecting isolated locoregional recurrences after treatment for early-stage invasive breast cancer: a meta-analysis and systematic review. JClin Oncol 2004; 22 (19): 4010-8 3 Carreira H et al.: Associations between breast cancer survivorship and adverse mental health outcomes: a systematic review. Ann Surg Oncol 2018; 14 (6): 1904-8 4 Duma MN: Das Lymphödemrisiko von Mammakarzinompatientinnen nach Operation oder Strahlentherapie der Axilla. Strahlenther Onkol 2021; 197 (6): 562-4 5 Höller U, Feyer P: Management und Prophylaxe von organbezogenen Toxizitäten: Pneumotoxizität unter Strahlentherapie. Im Fokus Onkologie 2007; 9: 61-7 6 Sonnet M: Nebenwirkungen von Immuncheckpointinhibitoren: eine umfassende Metaanalyse. Arzneimitteltherapie 2019; 37(04): 133-147 7 Hershmann DL et al.: Early discontinuation and nonadherance to adjuvant hormonal therapy in a cohort of 8,769 early-stage breast cancer patients. J Clin Oncol 2010; 28 (27): 4120-8 8 Leitlinienprogramm Onkologie: S3-Leitlinie Komplementärmedizin in der Behandlung von onkologischen Patienten, online unter: https://www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/Downloads/Leitlinien/Komplement%C3%A4r/Version_1/LL_Komplement%C3%A4r_Langversion_1.1.pdf 9 CTS5 Calculator. Online unter: https://cts5-calculator.com 10 Arbeitsgemeinschaft gynäkologische Onkologie (AGO) e.V.: Kommission Mamma: Guidelines Breast, Version 2021, 1D 11 Leitlinienprogramm Onkologie: S3-Leitlinie Mammakarzinom. Online unter: https://www.leitlinienprogramm-onkologie.de/fileadmin/user_upload/Downloads/Leitlinien/Mammakarzinom_4_0/Version_4.4/LL_Mammakarzinom_Langversion_4.4.pdf 12 Loibl S, Seiler S: Schwangerschaft nach einer Tumorerkrankung. Gynäkologische Endokrinologie 2019; 17: 65-70 13 Trapp E et al.: Presence of circulating tumor cells in high-risk early breast cancer during follow-up and prognosis. J Natl Cancer Inst 2019; 111: 380-7 14 ESMO Clinical Practice Guidelines: Breast Cancer. Online unter: https://www.esmo.org/guidelines/breast-cancer
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...