Myeloproliferative Neoplasie und chronische myeloische Leukämie
Autor:
Dr. med. Nathan Cantoni
Leitender Arzt Hämatologie
Koordinator Lymphom- und Leukämiezentrum
Leiter Klinische Forschung
Kantonsspital Aarau
Medizinische Universitätsklinik
Abteilung Onkologie, Hämatologie und Transfusionsmedizin
E-Mail: nathan.cantoni@ksa.ch
Nach zwei Jahren mit nur virtuellen Meetings konnte man am Jahreskongress der European Hematology Association (EHA) 2022 wieder persönlich in Wien teilnehmen. Durch das Hybrid-Format hatte der Kongress aber gleichzeitig auch die Vorteile einer virtuellen Lösung. Wie häufig in den letzten Jahren nahmen die myeloproliferative Neoplasie (MPN) und die chronische myeloische Leukämie (CML) amEHA-Meeting einen vergleichsweise bescheidenen Platz ein. In Wien wurden hauptsächlich neue therapeutische Möglichkeiten für die Behandlung von MPN sowie die finalen Daten der Zulassungsstudie von Ropeginterferon alfa-2b für die Behandlung der Polycythaemia vera (PV) vorgestellt. Bei der CML stand Asciminib im Vordergrund.
Ropeginterferon alfa-2b für die Behandlung der PV
In der PROUD- & CONTINUATION-PV-Studie wurden 257 Patient*innen mit PV zu einer Behandlung mit Hydroxyurea (HU; Standardbehandlung) oder Ropeginterferon alfa-2b randomisiert.1 Ropeginterferon alfa-2b ist ein lang wirkendes monopegyliertes Interferon, welches initial alle zwei Wochen gespritzt werden muss. Durch diese neue Applikationsform wird eine bessere Verträglichkeit und dementsprechend eine bessere Adhärenz erwartet. Die Daten des guten Ansprechens von Ropeginterferon alfa-2b gegenüber Hydroxyurea wurden in der Vergangenheit vorgestellt und das Medikament ist für die Behandlung der PV in mehreren Ländern bereits zugelassen.
Nach einem Follow-up von mindestens 6 Jahren wurden am aktuellen EHA-Meeting die finalen Daten mit weiterhin besserem Ansprechen unter Ropeginterferon alfa-2b im Vergleich zu HU gezeigt (komplette hämatologische Remission unter Ropeginterferon alfa-2b 55% vs. Hydroxyurea 35%; p=0,02). Im Verlauf der Behandlung konnte in der interventionellen Gruppe auch eine deutliche Reduktion der JAK2-V617F-Allellastbestätigt werden (molekulares Ansprechen unter Ropeginterferon alfa-2b 66%, in der Hydroxyurea-Gruppe nur 19%; p<0,0001). Zusätzlich wurde bei 20% der Patient*innen unter Ropeginterferon alfa-2b eine komplette molekulare Remission (CMR; definiert als JAK2-V617F-Allellast <1%) erreicht, in der Standardgruppe erreichten nur 1% der Patient*innen eine CMR (p=0,0001).
Mit Ropeginterferon alfa-2b war nach 6 Jahren die Rate der Patient*innen ohne Aderlasstherapie höher (81% vs. 60%, p=0,005). Das ereignisfreie Überleben (Ereignis definiert als Tod, Progression der Grunderkrankung oder thromboembolische Komplikationen) war in der interventionellen Gruppe ebenfalls statistisch signifikant länger (p=0,04). Die Verträglichkeit war im Verlauf der Behandlung weiterhin gut und ohne neue Komplikationen.
Diese Daten bestätigen insgesamt die sehr gute Wirksamkeit von Ropeginterferon alfa-2b: Neben einem hämatologischen kann noch ein molekulargenetisches Ansprechen mit Reduktion der JAK2-V617F-Allellast erzeugt werden und das ereignisfreie Überleben ist länger.
Behandlung mit Momelotinib für Patient*innen mit einer Myelofibrose
Patient*innen mit einer primären oder sekundären Myelofibrose (MF) zeigen typischerweise eine relevante Anämie, welche sich mit den zugelassenen JAK-Inhibitoren (Ruxolitinib und Fedratinib) häufig verschlechtern kann. In dieser Situation sind die Behandlungsoptionen begrenzt.
Momelotinib inhibiert JAK1, JAK2 und ACVR1 und kann die typischen MF-Beschwerden sowie Splenomegalie und Anämie kontrollieren. Die Wirksamkeit dieser Behandlung wurde bereits in einer randomisierten Studie im Vergleich zur Standardtherapie mit Ruxolitinib bestätigt (Simplify-1 Trial mit einer JAK-Inhibitor-naïven Population). Der positive Effekt auf die Anämie lässt sich durch die Inhibition von ACVR1, einem Regulator des Eisenmetabolismus, erklären: Durch die chronische Inflammation wird ACVR1 überaktiviert mit nachfolgender Erhöhung des Hepcidin-Spiegels und Dysregulation des Eisenmetabolismus. Momelotinib kann dieser Überregulation entgegenwirken und so die Erythropoese bei einer MF positiv beeinflussen.
Im MOMENTUM Trial wurden 195 Patient*innen mit MF und signifikanter Anämie mit Momelotinib (interventionelle Gruppe) oder Danazol (Standardgruppe) behandelt (2:1-Randomisierung).2 Die geplante Behandlung von 24 Wochen wurde von 72% bzw. 59% der Teilnehmenden in der Momelotinib- bzw. Danazol-Gruppe beendet. Hauptgründe für einen Abbruch waren Nebenwirkungen oder fehlendes Ansprechen.
Der primäre Endpunkt, definiert als Verbesserung der Symptome nach 24 Wochen, wurde mit Momelotinib in 32% der Fälle erreicht, mit Danazol nur in 6% (p=0,0095). Die wichtigen sekundären Endpunkte nach 24 Wochen (Reduktion der Splenomegalie sowie Transfusionsunabhängigkeit) bestätigten ebenfalls die bessere Wirksamkeit von Momelotinib in dieser vorbehandelten Studienpopulation (Reduktion der Splenomegalie um mind. 35%: Momelotinib 23%, Danazol 3%; p=0,0006. Transfusionsunabhängigkeit: Momelotinib 31%, Danazol 20%; p=0,006).
Das Nebenwirkungsprofil war ähnlich wie in den anderen Momelotinib-Studien mit hauptsächlich Magen-Darm-Trakt-Nebenwirkungen (Durchfall, Nausea), Asthenie und Gewichtsverlust. Zusammenfassend beweisen diese Daten die gute Wirkung von Momelotinib bei vorbehandelten MF-Patient*innen, insb. bei gleichzeitiger Anämie.
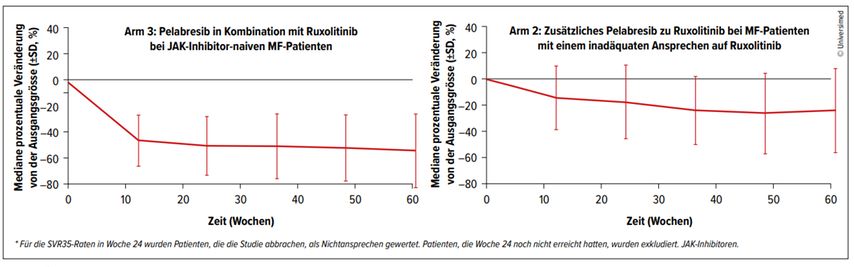
Abb. 1: Änderung der Milzgrösse (SD) in den Armen 2 und 3 der MANIFEST-Studie. Primärer Endpunkt: Reduzierung der Milzgrösse um ≥35% von der Ausgangsgrösse (SVR35)
Neue Therapieoptionen in der Behandlung von MPN
In Wien wurden zusätzlich verschiedene neue therapeutische Möglichkeiten in der Behandlung von MPN, insbesondere bei Patient*innen mit Myelofibrose und Verlust des Ansprechens bzw. ungenügendem Ansprechen auf JAK-Inhibitoren, präsentiert.
Francesco Passamonti hat den REFINE Trial, eine Phase-II-Studie mit Navitoclax in Kombination mit Ruxolitinib für die Behandlung von 32 Patient*innen mit primärer oder sekundärer Myelofibrose, vorgestellt.3 Das Ruxolitinib als zugelassene Behandlung der Myelofibrose hat eine sehr gute Wirksamkeit für die Kontrolle der Splenomegalie sowie der konstitutionellen Beschwerden. Bei ungenügendem Ansprechen oder bei Verlust des Ansprechens sind weiterhin wenige therapeutische Optionen vorhanden.
Navitoclax ist ein neuer BCL2-Inhibitor und hat bereits in präklinischen Studien eine zytotoxische Wirkung gegen MPN-Zelllinien gezeigt. Durch eine synergistische Kombination von Navitoclax mit Ruxolitinib wird eine bessere zytotoxische Wirkung gegenüber MPN-mutierten Zellen mit nachfolgender Inhibition der Fibrosierung im Knochenmark erreicht. Dementsprechend sollte so eine Resistenz gegen eine klassische Behandlung mit JAK-Inhibitoren überwunden werden.
Alle behandelten Patient*innen zeigten im Verlauf der Studie eine Reduktion der Splenomegalie. Der primäre Endpunkt, definiert als Reduktion der Splenomegalie um mindestens 35% gemessen mit MRT nach 24 Wochen, wurde von 63% der Patient*innen erreicht. Die Reduktion der Milzvergrösserung war langfristig mit einem geschätzten persistierenden Ansprechen nach 12 Monaten bei 93% der Teilnehmenden. Bei 27% der Patient*innen konnte zusätzlich eine Reduktion der Myelofibrose dokumentiert werden und bei 40% zeigte sich eine Verbesserung einer vorbestehenden Anämie. Zusammenfassend, in diesen mit Ruxolitinib vorbehandelten Patient*innen konnte man mit der Zugabe von einem BCL2-Inhibitor ein erneutes Ansprechen erreichen. Die Resultate der randomisierten, placebokontrollierten Phase-III-Studie TRANSFORM-1 mit dieser Kombination bei JAK-Inhibitor-naiven Patient*innen werden entsprechend mit grosser Spannung erwartet.
BET(Bromodomain and Extra-Terminal Domain)-Proteine regulieren wichtige onkogene Signalwege, einschliesslich der NFκB- und TGFβ-Signalwege, die eine zentrale Rolle in der Zytokinproduktion sowie der Knochenmarkfibrose spielen und so an der Pathogenese der Myelofibrose beteiligt sind. Pelabresib (CPI-0610), ein selektiver und wirksamer BET-Proteine-Inhibitor (BETi), hat in präklinischen Untersuchungen zusammen mit JAK-Inhibitoren eine synergistische Wirkung für die Behandlung der Myelofibrose gezeigt.
Claire Harrison präsentierte die laufende MANIFEST-Studie, eine Phase-II-Studie zur Überprüfung der Wirksamkeit von Pelabresib als Monotherapie oder in Kombination mit Ruxolitinib bei Patient*innen mit einer Myelofibrose oder einer essenziellen Thrombozythämie (ET).4 In Wien wurden die Daten der Gruppe 2 (Zweitlinienbehandlung mit Pelabresib und Ruxolitinib bei MF-Patient*innen) und 3 (Erstlinienbehandlung mit Pelabresib und Ruxolitinib bei MF-Patient*innen) vorgestellt.
Die meisten Patient*innen zeigten eine Reduktion der Splenomegalie sowie eine deutliche Verbesserung der konstitutionellen Beschwerden, gemessen mit dem «MPN Assessment Form Total Symptom Score (MPN-SAF TSS)». Hinweisend für eine krankheitsmodifizierende Wirkung konnten zusätzlich eine Reduktion der Fibrosierung im Knochenmark (26% bzw. 28% in der Gruppe 2 bzw. 3 nach 24 Wochen, 39% bzw. 40% in der Gruppe 2 bzw. 3 zu jedem Zeitpunkt) sowie eine Verbesserung einer vorbestehenden Anämie (55% bzw. 13% der Patient*innen mit Monotherapie bzw. Kombination mit Ruxolitinib) dokumentiert werden.
Die MANIFEST-Studie rekrutiert weiter und wir können gespannt sein auf die weiteren Resultate über Pelabresib.
Myeloproliferative Neoplasie und splanchnische Venenthrombose
Thromboembolische Ereignisse sowie Blutungen stellen eine der häufigsten Komplikationen dar und führen häufig zur Diagnosestellung der hämatoonkologischen Grunderkrankung. Am EHA-Meeting 2022 wurden die retrospektiven Daten des britischen Registers über splanchnische Venenthrombosen bei myeloproliferativen Neoplasien (MASCOT) vorgestellt.5
Insgesamt wurden zwischen 2019 und 2022 238 Patient*innen mit MPN und splanchnischer Venenthrombose eingeschlossen. Signifikant mehr Frauen (58%, p=0,01) wiesen eine splanchnische Venenthrombose auf und 70% der Patient*innen waren 49-jährig oder jünger. In 19% der Fälle wurde zuerst die MPN diagnostiziert, in 26% zuerst die splanchnische Venenthrombose und in 55% wurden beide Diagnosen praktisch gleichzeitig gestellt. Bei 97% dieser Patient*innen war eine JAK2-V617F-Mutation vorhanden, bei den restlichen 3% wurde eine CALR-Mutation dokumentiert. In ca. 1/3 der Fälle wurde eine zusätzliche nicht splanchnische Thrombose nachgewiesen, 27% der Patient*innen litten im ersten Jahr nach Diagnose der Thrombose an einer klinisch relevanten Blutung.
Diese Daten zeigen die Wichtigkeit von Registerstudien für die Erfassung sowie Charakterisierung seltener Komplikationen bei seltenen Erkrankungen und sollten auf internationaler Ebene weiterverfolgt werden.
Therapie-freie Remission bei der CML
Mittlerweile hat sich die Therapie-freie Remission (TFR) bei der chronischen myeloischen Leukämie (CML) gut etabliert und wird als wichtiges Therapieziel bei CML-Patient*innen betrachtet, die optimale Strategie zum Erreichen einer TFR wurde bisher aber noch nicht klar definiert.
Fabrizio Pane zeigte in Wien die Daten des SUSTRENIM Trial, einer internationalen randomisierten Studie mit Nilotinib versus Imatinib mit früher Umstellung auf Nilotinib bei ungenügendem Ansprechen.6 Das ungenügende Ansprechen wurde definiert als Nichterreichen der Meilensteine gemäss ELN-Richtlinien nach 3, 6 oder 12 Monaten. Insgesamt wurden 448 Patient*innen 1:1 randomisiert und behandelt, das mediane Follow-up betrug 33 Monate.
In der Gruppe mit Imatinib mussten 26% der Patient*innen früh in der Behandlung eine Umstellung auf Nilotinib vornehmen. Trotz dieser frühzeitigen Umstellung erreichten in der Imatinib-Gruppe signifikant weniger Patient*innen eine MR4.5 nach 24 Monaten (primärer Endpunkt: Nilotinib 29% vs. Imatinib 18%; p=0,02).
Diese Resultate zeigen, dass unter Imatinib mit frühzeitiger Umstellung bei ungenügendem Ansprechen weniger Patient*innen eine tiefe molekulare Remission erreichen. Dementsprechend kann man postulieren, dass mit dieser Strategie die Rate der TFR tiefer sein wird im Vergleich zu einem Tyrosinkinase-Inhibitor (TKI) der Zweitgeneration wie Nilotinib. Diese Daten wurden aber (noch) nicht vorgestellt und weitere Datenanalysen werden erwartet.
Aus Kanada wurde eine weitere Studie, der TRAD Trial, zum Absetzen der Tyrosinkinase-Inhibitoren (TKIs) bei CML vorgestellt.7 Hier wurde ein zweites Absetzen eines TKI der 2. Generation (Dasatinib) nach einem erfolglosen Absetzversuch nach Erstlinienbehandlung mit Imatinib bei 131 Patient*innen untersucht.
Die TFR1 nach Imatinib war, ähnlich wie in anderen Studien, 56%, in 58 (44%) Fällen zeigte sich dagegen ein molekulares Rezidiv mit Notwendigkeit einer Zweitlinienbehandlung mit Dasatinib. Darunter zeigte sich wieder ein gutes und tiefes Ansprechen. Von diesen 58 Patient*innen konnte die Therapie mit Dasatinib nach 12 Monaten bei 35 Patient*innen erneut gestoppt werden.
Leider zeigten im Verlauf nur 4 Teilnehmende (11,4%) eine persistierende molekulare Remission. Dementsprechend kann man hier zusammenfassend sagen, dass mit Dasatinib ein erneutes molekulares Ansprechen nach erfolglosem erstem Absetzversuch erreicht wird, die TFR bleibt aber auch mit Dasatinib nach dem 2. Absetzversuch sehr tief.
Asciminib für die Behandlung der CML
In der ASCEMBL-Studie wurde Asciminib versus Bosutinib bei CML-Patient*innen mit mind. 2 vorherigen Behandlungen mit anderen TKIs untersucht. Insgesamt wurden 233 Patient*innen eingeschlossen und mit Asciminib oder Bosutinib (2:1-Randomisierung) therapiert. Nachdem Asciminib bereits eine bessere Wirksamkeit gegenüber Bosutinib gezeigt hatte und den primären Endpunkt (MMR-Rate nach 24 Wochen) erreicht hatte, wurde am EHA-Meeting 2022 ein Update der Resultate nach einem medianen Follow-up von 120 Wochen vorgestellt.8
Asciminib ist der erste BCR-ABL1-Inhibitor, der die Kinaseaktivität der BCR-ABL1-Tyrosinkinase hemmt, indem er speziell auf das ABL Myristoyl Pocket (STAMP-Inhibitor) abzielt und nicht direkt an der ATP-Bindungsstelle des BCR-ABL1-Fusionsproteins angreift. Dadurch wird die Wirkung von Asciminib durch bekannte Mutationen der ATP-Bindungsstelle nicht beeinflusst.
Eine der wichtigsten Informationen nach diesem langen Follow-up ist die gute Verträglichkeit von Asciminib: Nach 2,3 Jahren sind noch 54% der Patient*innen unter Behandlung mit Asciminib, in der Bosutinib-Gruppe sind es nur noch 20%. Die Hauptgründe für einen Therapieabbruch waren ein Verlust des Ansprechens (24% vs. 36%) oder Unverträglichkeit (7% vs. 25%). Im Verlauf wurden keine neuen Komplikationen berichtet.
Schlussendlich bleibt aber auch die Wirksamkeit von Asciminib in dieser zum Teil stark vorbehandelten Studienpopulation konsistent höher als mit Bosutinib mit einer MMR-Rate nach 96 Wochen von 38% vs. 16%. Die MR4.0- und MR4.5-Raten nach 96 Wochen waren in der Asciminib-Gruppe auch höher. Das ereignisfreie Überleben (Ereignis definiert als Tod, fehlendes Ansprechen gem. ELN-Richtlinien, Progression der Grunderkrankung oder Abbruch aufgrund Nebenwirkungen) war in der interventionellen Gruppe mit Asciminib ebenfalls statistisch signifikant länger (nach 2 Jahren EFS: Asciminib 57%, 95% CI: 49–65%; Bosutinib 25%; 95% CI: 15–36%; p<0,0001).
Interessant werden jetzt die Daten über die Erstlinienbehandlung, aber auch über Kombinationen mit anderen TKIs sein, die Studien dazu rekrutieren gerade und wir können auf die Resultate gespannt sein.
Literatur:
1 Gisslinger H et al.: EHA 2022; Abstr. #S196 2 Verstovsek S et al.: EHA 2022; Abstr. #S195 3 Passamaonti F et al.: EHA 2022; Abstr. #S197 4 Mascarenhas J et al.: EHA 2022; Abstr. #S198 5 Hargreaves R et al.: EHA 2022; Abstr. #S199 6 Pane F et al.: EHA 2022; Abstr. #S156 7 Kim D et al.: EHA 2022; Abstr. #S158 8 Rea D et al.: EHA 2022; Abstr. #S155
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...