Drei potenziell praxisverändernde Studien
Bericht:
Dr. med. Judith Moser
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Bei Patient:innen mit metastasiertem kolorektalem Karzinom konnten die Therapieoptionen in den letzten Jahrzehnten bereits massiv erweitert werden. Dr. med. Thibaud Kössler, Genf, stellte in seinem Vortrag die Ergebnisse dreier am ASCO-Kongress 2024 präsentierter Studien vor, diein naher Zukunft zu einer weiteren Modifikation der derzeit gültigen Behandlungsalgorithmen führen könnten.
In der Studie KEYNOTE-177 verlängerte der PD-1-Inhibitor Pembrolizumab das progressionsfreie Überleben (PFS) im Vergleich zur Chemotherapie bei unbehandelten Patient:innen mit metastasiertem Kolorektalkarzinom (mCRC) und hoher Mikrosatelliteninstabilität (MSI-H)/Mismatch-Reparaturdefizienz (dMMR).1 Auf der Basis dessen wurde Pembrolizumab als Erstlinienstandard beim MSI-H/dMMR mCRC etabliert.2
Die derzeit noch laufende dreiarmige Phase-III-Studie CheckMate 8HW evaluiert ein duales Checkpoint-Inhibitor-Schema in diesem Setting. Nivolumab 240mg plus Ipilimumab 1mg/kg über vier Zyklen gefolgt von einer Nivolumab-Monotherapie alle vier Wochen wird mit Nivolumab als Monotherapie sowie einer Chemotherapie nach Wahl der Prüfärzt:innen mit oder ohne Bevacizumab bzw. Cetuximab verglichen. Am ASCO-Kongress 2024 präsentierten Lenz et al. die Ergebnisse für die Kombination (n=171) im Vergleich zur Chemotherapie (n=84). Die MSI-H/dMMR-Testung erfolgte an den örtlichen Institutionen.
CheckMate 8HW: beeindruckender PFS-Benefit
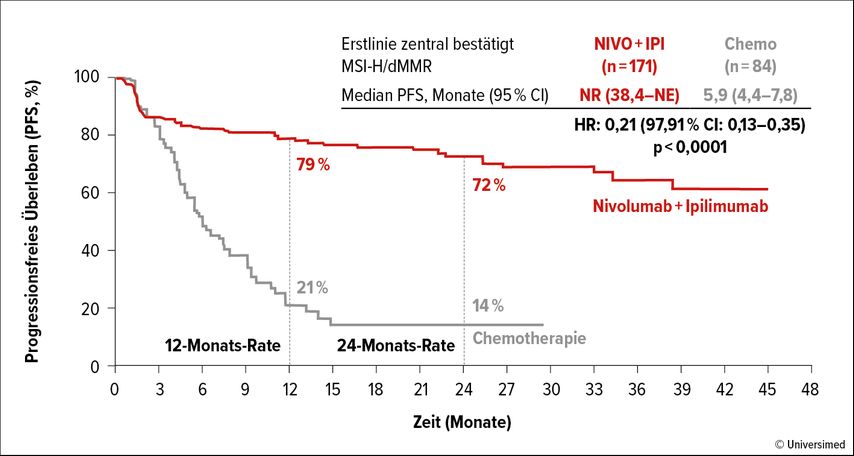
Nivolumab/Ipilimumab bewirkte in der CheckMate-8HW-Studie einen beeindruckenden PFS-Vorteil gegenüber der Chemotherapie (nicht erreicht vs. 5,9 Monate; HR: 0,21; p<0,0001; Abb. 1).3Kössler fand das verhältnismässig schlechteAbschneiden im Kontrollarm auffällig. Im Gegensatz zu KEYNOTE-177 war die Immuntherapie der Chemotherapie in den ersten Behandlungsmonaten nicht unterlegen. Die Subgruppenanalysen erbrachten konsistente PFS-Vorteile im experimentellen Arm unabhängig von Geschlecht, BRAF/KRAS/NRAS-Mutationsstatus und Vorliegen eines Lynch-Syndroms. Da in KEYNOTE-177 Unterschiede in Bezug auf diese Kohorten zwischen den Armen festgestellt worden waren, sei es beruhigend zu wissen, dass die duale Immuntherapie in allen Subgruppen effektiv zu sein scheint, so Kössler. Nivolumab/Ipilimumab werde vermutlich in naher Zukunft in die Behandlungslandschaft integriert werden.
Abb. 1: MSI-H/dMMR mCRC: progressionsfreies Überleben unter Nivolumab plus Ipilimumab vs. Chemotherapie in der Erstlinie (modifiziert nach Lenz HJ et al.)3
Dennoch müsse man die Toxizität dieses Schemas im Auge behalten, dennbehandlungsbedingte Nebenwirkungen, die zum Therapieabbruch führten, seien unter Nivolumab/Ipilimumab häufiger aufgetreten als unter der Chemotherapie (18% vs. 5%), betonte er. Nachdem die Doublette seit vielen Jahren eingesetzt wird, gebe diese anhaltend hohe Rate an unerwünschten Ereignissen zu denken, sagte der Onkologe.
Ein weiteres Thema bezieht sich auf die MSI-Testung, da die örtlich festgestellte MSI-H-Positivität bei bis zu 15% der Patient:innen der zentralen Überprüfung nicht standhielt. Somit könnte laut Kössler eine der wichtigen Schlussfolgerungen lauten, dass medizinische Onkolog:innen sich der Zuverlässigkeit der Tests absolut sicher sein müssen. Auch sollte der MSI/MMR-Status initial ermittelt werden, da die Ergebnisse die Wahl der Behandlung drastisch beeinflussen können, betonte er.
Transplantation nicht resektabler Lebermetastasen
Die TransMet-Studie prüfte die Lebertransplantation als Behandlungsoption bei definitiv inoperablen Lebermetastasen eines CRC. Infrage kommende Patient:innen wurden von lokalen Tumorboards ausgewählt und von einem unabhängigen, multidisziplinären Expert:innengremium validiert. Danach erfolgte randomisiert die Zuteilung zur Lebertransplantation plus Chemotherapie oder nur zur Chemotherapie. Die Patient:innen im Prüfarm wurden auf die Warteliste gesetzt, wobei das Ziel in der Transplantation innerhalb von zwei Monaten nach der letzten Chemotherapie bestand. Das Validierungskomitee prüfte die Fälle von insgesamt 157 Patient:innen, von denen 94 randomisiert wurden, während sich 63 (40%) nicht qualifizierten. Im Endeffekt gingen nur 36 bzw. 38 Patient:innen in der Versuchs- bzw. Kontrollgruppe in die Per-Protocol-Analyse ein.
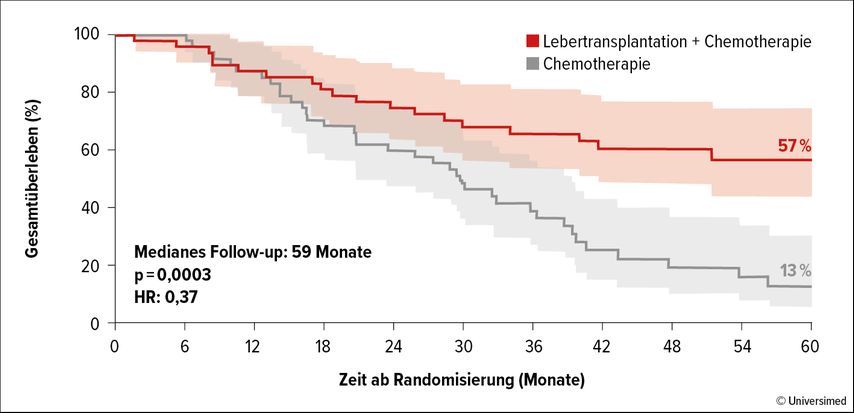
Der primäre Endpunkt der Studie wurde erreicht. Nach fünf Jahren waren 57% vs. 13% der Patient:innen am Leben (p=0,0003; Abb. 2).4 Dieser Unterschied entsprach einer Risikoreduktion um 63% (HR: 0,37). Rezidive traten im experimentellen Arm bei 72% (vs. 97%) auf, wobei die Lungen den häufigsten Manifestationsort bildeten. Fast die Hälfte dieser Patient:innen konnte jedoch einen chirurgischen Eingriff oder eine Ablation in Anspruch nehmen, sodass 42% der im Prüfarm Behandelten nach vier Jahren krankheitsfrei waren. Im Gegensatz dazu traf dies nur auf 3% der Personen in der Kontrollgruppe zu.
Abb. 2: Gesamtüberleben im Verlauf von fünf Jahren nach Lebertransplantation plus Chemotherapie vs. Chemotherapie bei mCRC mit hepatischen Metastasen (modifiziert nach Adam R et al.)4
TransMet ist die erste Studie, die die Option einer Lebertransplantation in dieser Situation in randomisierter Form untersucht hat. Die Ergebnisse sind laut Kössler hochrelevant, da sie Massstäbe in Bezug auf die Durchführbarkeit von Transplantationen bei Leberzirrhose oder hepatozellulären Karzinomen setzen. Die Durchführung einer Studie wie dieser gestalte sich schwierig, und er gratuliere den Autor:innen und dem Team, so Kössler. Zwarwerfe die Auswahl der Patient:innen unweigerlich auch ethische Fragen auf, aber vermutlich werde die Lebertransplantation dennoch Eingang in die Leitlinien finden.
dMMR-Rektumkarzinom: anhaltende CR mit Dostarlimab
Einem Teil der Rektumkarzinome liegt eine Defizienz der Mismatch-Reparatur zugrunde. Cercek et al. untersuchten in einer prospektiven Phase-II-Studie die Wirksamkeit der PD-1-Blockade mit Dostarlimab bei Patient:innen mit lokal fortgeschrittenem Rektumkarzinom (Stadium II oder III) und dMMR.
Zwölf Personen wurden in die Studie aufgenommen, von denen alle nach Abschluss der sechsmonatigen Behandlung ein vollständiges klinisches Ansprechen (cCR) erzielten.5 Zum Zeitpunkt der primären Analyse hatte noch niemand eine zusätzliche Chemoradiotherapie oder Operation erhalten und während der Nachbeobachtungszeit von 6–25 Monaten kam es in keinem Fall zum Auftreten von Progressions- oder Rezidivereignissen.
Das am ASCO-Jahrestreffen 2024 vorgestellte Update umfasste eine erweiterte Kohorte von 42 Patient:innen. Diese Ergebnisse bestätigten die ursprünglichen Beobachtungen: Nach dem Abschluss der Dostarlimab-Behandlung und einer medianen Nachbeobachtungszeit von 17,9 Monaten hatten alle Teilnehmer:innen eine cCR erreicht.6 Darüber hinaus erfassten die Autor:innen die Zeit bis zur cCR gemäss den einzelnen Untersuchungsmethoden.
Die mediane Zeit bis zur cCR war laut zirkulierender Tumor-DNA (1,38 Monate) und Biopsie (1,41 Monate) am kürzesten. Laut PET-CT betrug die mediane Zeit bis zur cCR 2,76 Monate. Die längsten Intervalle fanden sich mit 6,15 bzw. 6,18 Monaten gemäss der rektalen MRT bzw. Endoskopie. MRT und Endoskopie eigneten sich daher für die Beurteilung des frühen Ansprechens in dieser Situation möglicherweise weniger gut als ctDNA und Biopsie, sagte Kössler.
Insgesamt sei die Identifikation des idealen Verfahrens nicht einfach, aber vermutlich werde sich eine Kombination aus Liquid Biopsy plus Bildgebung und Gewebebiopsie als der praktikabelste Ansatz erweisen, vermutete der Onkologe. Er geht davon aus, dass alle drei genannten Studien die Leitlinien beeinflussen werden.
Literatur:
1 André T et al.: Pembrolizumab in microsatellite-instability-high advanced colorectal cancer. N Engl J Med 2020; 383(23): 2207-18 2 Cervantes A et al.: Metastatic colorectal cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Ann Oncol 2023; 34(1): 10-32 3 Lenz HJ et al.: Nivolumab plus ipilimumab vs chemotherapy as first-line treatment for microsatellite instability-high/mismatch repair-deficient (MSI-H/dMMR) metastatic colorectal cancer: expanded efficacy analysis from CheckMate 8HW. J Clin Oncol 2024; 42(Suppl. 16): Abstr. #3503 4 Adam R et al.: Chemotherapy and liver transplantation versus chemotherapy alone in patients with definitively unresectable colorectal liver metastases: a prospective multicentric randomized trial (TRANSMET). J Clin Oncol 2024; 42(Suppl. 16): Abstr. #3500 5 Cercek A et al.: PD-1 blockade in mismatch repair-deficient, locally advanced rectal cancer. N Engl J Med 2022; 386: 2363-76 6 Cercek A et al.: Durable complete responses to PD-1 blockade alone in mismatch repair deficient locally advanced rectal cancer. J Clin Oncol 2024; 42(Suppl. 17): Abstr. #LBA3512
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...