Melanom-Vakzine, epidemiologische Analyse bei cSCC & AK, Anti-HER2 beim EMPD
Bericht:
Dr. Judith Moser
Am 19. Kongress der European Association of Dermato-Oncology (EADO) wurden aktuelle Studiendaten zu einem breiten Spektrum an Hauttumoren – vom Melanom bis zu seltenen Neoplasien – von weltweit führenden Expert*innen diskutiert.
Immuntherapie des Melanoms
Immunmodulierende Vakzine plusNivolumab
Indolamin-2,3-Dioxygenase (IDO) zählt ebenso wie PD-L1 zu den immunsupprimierenden Proteinen, die von regulatorischen Immunzellen und Krebszellen exprimiert werden.1 Gleichzeitig bewirken diese Proteine als Antigene eine Aktivierung der T-Zellen und somit eine proinflammatorische Reaktion.2 Eine Phase-I/II-Studie prüfte eine IDO/PD-L1-gerichtete Peptidvakzine (maximal 15 Gaben in zwei- und später vierwöchigen Intervallen) in Kombination mit zweiwöchentlichem Nivolumab 3mg/kg bei Patient*innen mit lokal fortgeschrittenem oder metastasiertem Melanom (n=30).
Laut der initialen Analyse traten im Vergleich zu einer Nivolumab-Monotherapie keine zusätzlichen Toxizitäten zutage.2 Makulopapulöse Hautausschläge, Fatigue, Arthralgie und Diarrhö wurden als häufigste Nebenwirkung der Nivolumab-Gabe verzeichnet. Die Vakzinierung bewirkte in hohen Prozentsätzen Lokalreaktionen und Granulome an der Einstichstelle. Insgesamt resultierte eine Gesamtansprechrate (ORR) von 80% mit Komplettremissionen (CRs) in 43%. Das mediane progressionsfreie Überleben (PFS) betrug 27 Monate, während das mediane Gesamtüberleben (OS) noch nicht erreicht war.
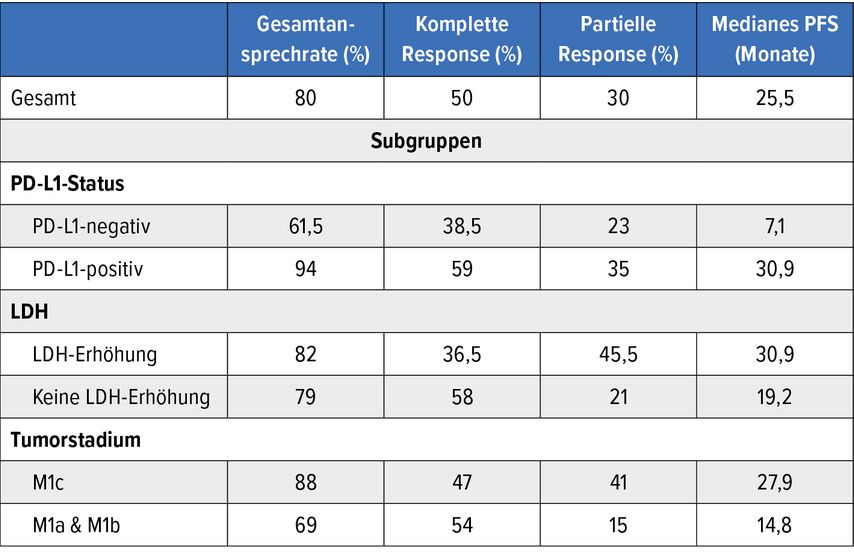
Gemäß den am EADO-Kongress präsentierten Langzeitdaten hielt das Ansprechen bei einem Drittel der Patient*innen auch nach einem Follow-up von 45,3 Monaten an.3 Nun lag das mediane PFS bei 25,5 Monaten, und das mediane OS war noch immer nicht erreicht worden. Die CR-Rate betrug mittlerweile 50% (Tab. 1). Subgruppenanalysen implizieren gute klinische Ergebnisse bei PD-L1-Positivität sowie in Kollektiven mit ungünstiger Prognose (LDH-Erhöhung, M1c-Erkrankung). Eine randomisierte multizentrische Phase-III-Studie evaluiert aktuell Pembrolizumab mit oder ohne IDO/PD-L1-gerichtete Vakzine beim fortgeschrittenen Melanom.
Tab. 1: IDO/PD-L1-gerichtete Vakzine plus Nivolumab bei Melanompatient*innen: Ansprechen im Gesamtkollektiv und in Subgruppen. Modifiziert nach Svane IM et al.3
Intratumorales Kombinationsschema
CD1c(BDCA-1)- und CD141(BDCA-3)-positive myeloische dendritische Zellen (myDCs) sind in metastasierten Tumoren defizient, während sie gleichzeitig die Voraussetzung für das Ansprechen auf die Checkpoint-Inhibitortherapie bilden.4,5 Ein klinisches Phase-I/II-Studienprogramm testet derzeit die intratumorale Injektion von myDCs bei verschiedenen Tumorentitäten. Gegenstand der am EADO-Kongress präsentierten Untersuchung war die Kombination von CD1c(BDCA-1)+/CD141(BDCA-3)+ myDCs mit Nivolumab/Ipilimumab sowie AS01B, einem Adjuvans der Herpes-Zoster-Vakzine Shingrix®, das zu einer transienten und lokalen Aktivierung des unspezifischen Immunsystems führt, in einem Kollektiv mit metastasiertem Melanom.6,7
Acht massiv vorbehandelte Patientinnen, die refraktär gegenüber Checkpoint- und BRAF/MEK-Inhibitoren waren, erhielten im Rahmen der Phase-I-Studie zuerst eine Leukapherese zwecks Gewinnung autologer myDCs. Danach kamen alle zwei Wochen Nivolumab intravenös sowie Ipilimumab und AS01B intratumoral zur Anwendung, während die myDCs einmalig am Tag 2 intratumoral injiziert wurden. Diese Behandlung erfolgte über einen Zeitraum von bis zu einem Jahr.
Die Analyse erbrachte vielversprechende frühe Ergebnisse ohne unerwartete Sicherheitssignale.8 Zwei Patientinnen entwickelten CRs als beste Response, in einem Fall kam es zur partiellen Remission (PR) und in einem weiteren zur Krankheitsstabilisierung. Bei zwei Patientinnen trat eine frühe Progression auf, und die letzten beiden konnten nicht ausgewertet werden. Pathologische CRs der behandelten Läsionen resultierten bei einer Patientin mit CR und jener mit PR; diese befinden sich nach mehr als 41 bzw. 42 Wochen am Leben und sind progressionsfrei. Das längste Überleben von mehr als 63 Monaten zeigte die zweite Patientin, die eine CR erreichte. Als häufigste Nebenwirkungen wurden Fatigue und lokale Reaktionen an der Injektionsstelle dokumentiert. Derzeit laufen translationale Untersuchungen, und eine Dosisintensivierung und Phase-II-Expansion sind geplant.
Basaliom: intraläsionale Immunzytokingabe
Die offene, multizentrische Phase-II-Studie DuNCan evaluiert die intraläsionale Gabe von NidlegyTM, einem Präparat aus den beiden synergistischen Immunzytokinen L19-IL2 and L19-TNF, bei Patient*innen mit lokal fortgeschrittenem, nicht metastasiertem Basaliom oder kutanem Plattenepithelkarzinom mit hohem Risiko. Die Teilnehmer*innen kamen für eine Operation oder Bestrahlung nicht infrage bzw. lehnten diese ab. NidlegyTM wird intraläsional einmal wöchentlich in vier aufeinanderfolgenden Wochen appliziert. Am EADO-Kongress 2023 stellten Wagner et al. die Ergebnisse der Gruppe mit Basaliom vor.9
Bei den ersten 16 Patient*innen konnte eine hohe Verträglichkeit der Therapie beobachtet werden. Influenzaartige Symptome und Pyrexie der Grade 1 und 2 ließen sich mit Standardtherapien wie Acetaminophen kontrollieren. Zwei Fälle von Infektionen an der Einstichstelle stellten die einzigen therapiebezogenen Grad-3-Ereignisse dar, Toxizitäten der Grade 4 oder 5 traten nicht auf. Da die Symptome auf 2–3 Tage begrenzt waren, musste keine Verschiebung nachfolgender Injektionen erfolgen. Fünf Patient*innen erreichten nach einer medianen Zeitspanne von 2,2 Monaten eine pathologische CR.
Insgesamt legen die Daten nahe, dass NidlegyTM bei Patient*innen mit Basaliom, die nicht operiert und bestrahlt werden möchten, eine sichere und effektive Kurzzeittherapie darstellt.
Epidemiologische Daten
Plattenepithelkarzinom bei Organtransplantatempfängern
Eine dänische Fall-Kontroll-Studie nahm Bezug auf die Prognose kutaner Plattenepithelkarzinome (cSCC) bei Empfänger*innen von Organtransplantaten.10 Die Wissenschaftler*innen werteten Daten aus vier nationalen Gesundheitsregistern von Patient*innen aus, die transplantiert worden waren und später ein cSCC entwickelten (n=287). Der Vergleich erfolgte mit gematchten cSCC-Patient*innen ohne Transplantation in der Vorgeschichte, wobei Immunsuppression und Immundefizienz als Ausschlusskriterien galten (n=1148). Die Baseline-Charakteristika waren zwischen den Gruppen ausgeglichen, allerdings fiel im transplantierten Kollektiv ein etwa doppelt so hoher Anteil an Patient*innen mit multiplen Tumoren wie in der Kontrollgruppe auf.
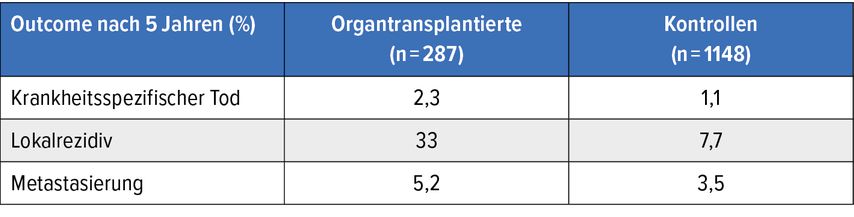
In Bezug auf alle drei untersuchten Outcome-Parameter schnitt die transplantierte Gruppe schlechter ab als die Kontrollen (Tab. 2). Jedoch erwies sich die Immunsuppression nach der statistischen Anpassung nicht als signifikanter Faktor, während die Tumorzahl signifikant ins Gewicht fiel. Es lässt sich der Schluss ziehen, dass Organtransplantat-Empfänger ein höheres Risiko für multiple cSCCs aufweisen (p<0,001), wobei die Anzahl der Läsionen das Risiko für krankheitsspezifischen Tod, Lokalrezidiv und Metastasierung erhöht. Die Immunsuppression dürfte sich daher indirekt über die Anzahl der Tumoren auf die Prognose auswirken. Gleichzeitig könnte diese Assoziation auch über das T-Stadium und nicht die Tumorzahl mediiert sein, weshalb eine entsprechende Analyse initiiert wurde.
Tab. 2: cSCC-assoziierte Outcomes bei Organtransplantierten vs. Kontrollen. Modifiziert nach Rasmussen LE et al.10
Aktinische Keratose in europäischen Ländern
Angesichts des bisherigen Mangels an epidemiologischen Daten aus Europa bestimmten Palmisano et al. die Prävalenz und die Determinanten der aktinischen Keratose (AK) in europäischen Ländern, die zwischen 2009 und 2018 in die Euromelanoma-Kampagne zur Prävention von Hautkrebs eingeschlossen worden waren.11 Teilnehmer*innen der Kampagne hatten einen Fragebogen ausgefüllt, der auf Faktoren wie Sonnenexposition, Hauttyp und Familienanamnese Bezug nahm. 310406 Personen aus 30 Ländern wurden evaluiert. Bei 64,2% handelte es sich um Frauen, das mediane Alter betrug 45 Jahre. Im Gesamtkollektiv lag die grobe AK-Prävalenz bei 10,3%, wobei die höchste Prävalenz in Mazedonien, Armenien, Serbien und Litauen festgestellt wurde.
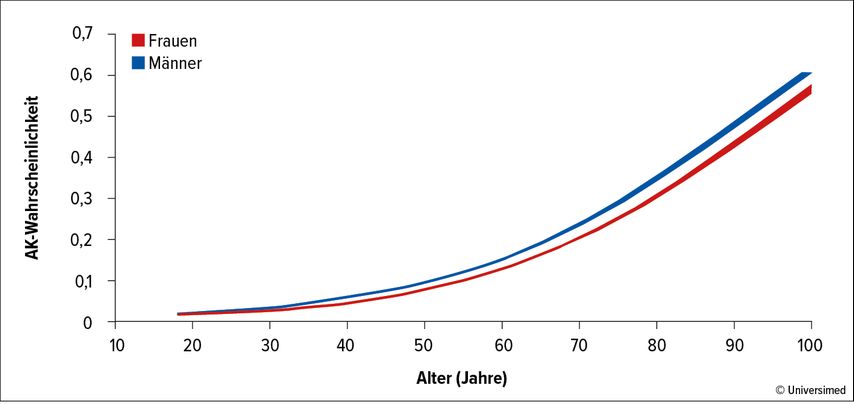
Der Breitengrad erwies sich lediglich als marginale Determinante; nach der Einteilung der Länder in drei Regionen zeigten Mittel- und Nordeuropa mit jeweils 11,2% eine etwas höhere Prävalenz als Südeuropa (7,1%). Für die AK-Häufigkeit scheint eine komplexe Interaktion zwischen Phänotyp, Verhalten und Geografie verantwortlich zu sein, dennoch ergab die multivariable Analyse einige signifikante unabhängige Prädiktoren. Alter, männliches Geschlecht (Abb. 1), geringerer Bildungsgrad, stattgehabte schwere Sonnenbrände, berufliche Tätigkeit im Freien und die Familien- und Eigenanamnese (Melanome, nichtmelanozytäre Karzinome) sowie aktuell vorhandene Läsionen erhöhten das Risiko. Als protektiv erwiesen sich dunkler Hauttyp, Verwendung von Sonnencremes und die Bereitschaft, ärztliche Kontrollen des Hautstatus durchzuführen. In jedem Land war ein heller Hauttyp ein starker, signifikanter Prädiktor.
Abb. 1: Alter und Geschlecht als Determinanten für die Entstehung aktinischer Keratosen. Modifiziert nach Palmisano G et al.11
Wie die Autor*innen festhalten, könnten unter Berücksichtigung soziodemografischer und kulturell-gesellschaftlicher Unterschiede auf einzelne Länder zugeschnittene Präventionsprogramme erstellt werden.
Dauer der Cemiplimab-Gabe beicSCC
Eine retrospektive Analyse behandelte die Frage der idealen Anwendungsdauer von Cemiplimab bei Patient*innen mit lokal fortgeschrittenem oder metastasiertem cSCC, die keine Progression zeigen.12 Den Hintergrund bildete die Tatsache, dass die Therapiedauer in den klinischen Studien unterschiedlich gehandhabt wurde und diese Art der Behandlung aufgrund ihrer hohen Tolerabilität theoretisch über Jahre zum Einsatz gelangen kann. Patient*innen, die im Zeitraum zwischen 2016 und 2021 am Dana Farber Cancer Institute oder Massachusetts General Hospital behandelt worden waren, gingen in die Analyse ein. Insgesamt wurden 93 Personen identifiziert, die Cemiplimab für <6 Monate (49%), 6–12 Monate (28%) oder ≥12 Monate (23%) erhalten hatten.
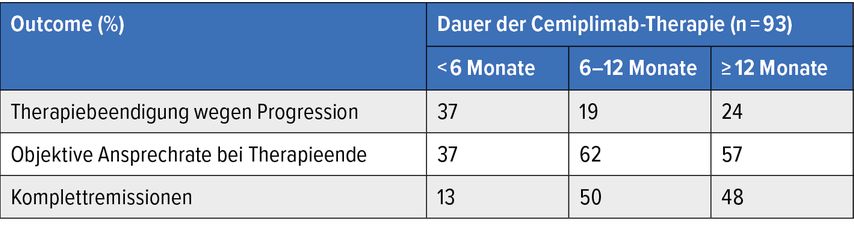
Wie sich zeigte, schnitten die länger behandelten Patient*innen besser ab, wobei zwischen 6–12 und ≥12 Monaten kein wesentlicher Unterschied bestand (Tab. 3). Ein größerer Anteil der für <6 Monate therapierten Gruppe beendete die Behandlung aufgrund einer Progression. Zum Zeitpunkt des Absetzens war die ORR in der Gruppe am höchsten, die Cemiplimab 6–12 Monate lang erhalten hatte. Auch die Wahrscheinlichkeit für Komplettremissionen nahm zu, wenn die Therapie über die Sechsmonatsgrenze hinausging. Die Kurven zum Gesamtüberleben ähnelten einander in den länger therapierten Gruppen und waren den Ergebnissen im kürzer behandelten Kollektiv sowohl in der Gesamtgruppe als auch bei den Patient*innen ohne Ansprechen überlegen.
Tab. 3: Cemiplimab beim cSCC: klinische Endpunkte in Abhängigkeit von der Therapiedauer. Modifiziert nach Ruiz E et al.12
42% der Patient*innen erzielten innerhalb von 12 Monaten eine CR. PRs resultierten in 70%; hier trat das Ansprechen bei 64% bereits innerhalb von 6 Monaten ein. 95% jener, die eine CR erreichten, zeigten ungeachtet ihrer Therapiedauer nach dem Absetzen von Cemiplimab keine Progression. Nur bei zwei Patient*innen musste eine neuerliche Behandlung eingeleitet werden, wobei in einem Fall ein Ansprechen erreicht wurde und im anderen nicht. Insgesamt scheinen von einer Therapiedauer, die 6–12 Monate übersteigt, keine Benefits auszugehen.
M. Paget: erste Resultate zu HER2-gezielter Therapie
Bei einem Drittel der Patient*innen mit metastasiertem extramammärem Morbus Paget (EMPD) konnte eine HER2-Amplifikation als potenzielles therapeutisches Target identifiziert werden.13 Die im Setting des Mammakarzinoms bewährte Erstlinienkombination aus HER2-gerichteter Therapie und Chemotherapie stand im Fokus einer einarmigen Phase-II-Studie an Patient*innen mit HER2-positivem, nicht resektablem oder metastasiertem EMPD.14 Bis zu zwei Jahre lang wurde dreiwöchentlich Trastuzumab 6mg/kg plus Docetaxel 75mg/m2 verabreicht. Zehn der eingeschlossenen 13 Patient*innen befanden sich in der Erstlinie.
Die Kombination legte gute Effektivität bei akzeptabler Verträglichkeit an den Tag. Nach drei Zyklen betrug die ORR 76,9% (primärer Endpunkt), wobei in jeweils 38,5% CRs bzw. PRs eintraten. Das mediane PFS lag bei 9,3 Monaten, während das mediane OS noch nicht erreicht worden war. Zu den Nebenwirkungen zählten Neutropenie (alle Grade: 100%), Hypalbuminämie (84,6%), Alopezie (76,9%) und mukokutane Infektionen (84,6%). Grad-4-Neutropenien wurden in 92,3% verzeichnet, zu einer febrilen Neutropenie kam es jedoch nur in einem Fall (Grad 3). Grad-5-Ereignisse wurden nicht dokumentiert.
Insgesamt liefert diese prospektive Studie erstmals hochgradige Evidenz zur Therapie des metastasierten EMPD, bei dem bisher nur anekdotische Erfahrungen zum Einsatz von Chemotherapieschemen vorlagen. Weitere Studiendaten an größeren Populationen sind notwendig, um die Wirksamkeit und Sicherheit von Trastuzumab plus Docetaxel zu bestätigen.
Quelle:
19th European Association of Dermato-Oncology Congress, 20.–22. April 2023, Rom
Literatur:
1 Andersen MH: The balance players of the adaptive immune system. Cancer Res 2018; 78(6): 1379-82 2 Kjeldsen JW et al.: A phase 1/2 trial of an immune-modulatory vaccine against IDO/PD-L1 in combination with nivolumab in metastatic melanoma. Nat Med 2021; 27(12): 2212-23 3 Svane IM et al.: Long-term follow-up and subgroup analyses of metastatic melanoma patients treated with IDO/PD-L1 targeting peptide vaccine and nivolumab. EADO 2023 4 Garris CS et al.: Successful anti-PD-1 cancer immunotherapy requires T cell-dendritic cell crosstalk involving the cytokines IFN-γ and IL-12. Immunity 2018; 49(6): 1148-61.e7 5 Spranger S et al.: Tumor-residing Batf3 dendritic cells are required for effector T cell trafficking and adoptive T cell therapy. Cancer Cell 2017; 31(5): 711-23.e4 6 Coccia M et al.: Cellular and molecular synergy in AS01-adjuvanted vaccines results in an early IFNγ response promoting vaccine immunogenicity. NPJ Vaccines 2017; 2: 25 7 Didierlaurent AM et al.: Enhancement of adaptive immunity by the human vaccine adjuvant AS01 depends on activated dendritic cells. J Immunol 2014; 193(4): 1920-30 8 Tijtgat J et al.: First-in-human intratumoral administration of AS01B in combination with autologous CD1c (BDCA-1)+/CD141 (BDCA-3)+ in myeloid dendritic cells plus ipilimumab and IV nivolumab in patients with refractory advanced melanoma. EADO 2023 9 Wagner N et al.: Intralesional administration of L19IL2/I19TNF in difficult-to-treat BCC patients shows favorable safety profile and leads to complete remission of tumor lesions. EADO 2023 10 Rasmussen LE et al.: Risk of cutaneous squamous cell carcinoma recurrence, metastasis, and disease-specific death in solid organ transplant recipients: a nationwide matched case-control study. EADO 2023 11 Palmisano G et al.: Prevalence and determinants of actinic keratosis in Europe based on the EUROMELANOMA campaign. EADO 2023 12 Ruiz E et al.: Optimal duration of cemiplimab therapy in advanced cutaneous squamous cell carcinoma. EADO 2023 13 Hirai I et al.: Assessment of the methods used to detect HER2-positive advanced extramammary Paget‘s disease. Med Oncol 2018; 35(6): 92 14 Hirai I et al.: Phase II clinical trial of docetaxel and trastuzumab for HER2-positive advanced extramammary Paget’s disease (EMPD-HER2DOC). EADO 2023
Das könnte Sie auch interessieren:
Erhaltungstherapie mit Atezolizumab nach adjuvanter Chemotherapie
Die zusätzliche adjuvante Gabe von Atezolizumab nach kompletter Resektion und adjuvanter Chemotherapie führte in der IMpower010-Studie zu einem signifikant verlängerten krankheitsfreien ...
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...